
| A.①③⑤ | B.①④⑤ | C.②③⑤ | D.①②④ |
科目:高中化学 来源:不详 题型:单选题
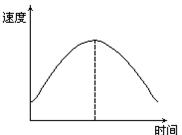
| A.①④ |
| B.③④ |
| C.①②③ |
| D.②③ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
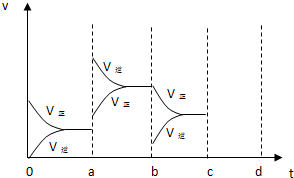
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.①②③④ | B.①③ | C.①② | D.①③④ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
| 实验序号 | 铁的质量/g | 铁的形态 | c(H2SO4) /mol?L-1 | V(H2SO4) /mL | 溶液温度 | 金属消失的时间/s | |
| 反应前 | 反应后 | ||||||
| 1 | 0.10 | 铁片 | 0.7 | 50 | 20 | 36 | 250 |
| 2 | 0.10 | 铁片 | 0.8 | 50 | 20 | 35 | 200 |
| 3 | 0.10 | 铁粉 | 0.8 | 50 | 20 | 36 | 25 |
| 4 | 0.10 | 铁片 | 1.0 | 50 | 20 | 35 | 125 |
| 5 | 0.10 | 铁片 | 1.0 | 50 | 35 | 50 | 20 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.开始时的反应速率:V(锌粒)>V(锌粉) |
| B.溶液温度升高的快慢:T(锌粒)>T(锌粉) |
| C.最后放出H2的总量:n(锌粒)>n(锌粉) |
| D.达平衡时正逆反应的速率相等 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
| 混合溶液 | A | B | C | D | E | F |
| 4mol/LH2SO4/mL | 30 | V1 | 30 | 30 | 30 | 30 |
| 饱和CuSO4溶液/mL | 0 | 0.5 | 2.5 | 5 | V2 | 20 |
| H2O/mL | 20 | 19.5 | V3 | 15 | 10 | 0 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.①③④ | B.②④⑥ | C.②⑤⑥ | D.①③⑤ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com