
| A�� | ��ӦCaO+H2O�TCa��OH��2�ܷų��������ȣ��ʿ�ͨ��ԭ���ʵ�ָ÷�Ӧ�����ѻ�ѧ��ת��Ϊ���� | |
| B�� | ��ԭ��ػ����װ���У�����ʵ�ַ�Ӧ��Cu+2H+�TCu2++H2 | |
| C�� | ��ԭ��ص������ǻ����Բ�ͬ�����ֽ���������õĽ�����һ�������� | |
| D�� | �ڸ�����Ʒ����Ƕп�鹹��ԭ����Է��θ������⣬���ַ�����������ӵ�Դ���������� |
���� A������Ƴ�ԭ��صķ�Ӧ�������Է����еķ��ȵ�������ԭ��Ӧ��
B��Cu+2H+�TCu2++H2�����Է���������ԭ��Ӧ��
C��ԭ�����ʧ���ӵ�һ��Ϊ������
D����ԭ��ص���������������������������������������
��� �⣺A������Ƴ�ԭ��صķ�Ӧ�������Է����еķ��ȵ�������ԭ��Ӧ��CaO+H2O�TCa��OH��2����������ԭ��Ӧ�����Բ�����Ƴ�ԭ��أ���A����
B��Cu+2H+�TCu2++H2�����Է���������ԭ��Ӧ�������γ�ԭ��أ���B����
C��ԭ�����ʧ���ӵ�һ��Ϊ���������õĽ�����һ����������������Ũ���ᷢ���ۻ�����ͭ��Ũ���ᷴӦ������Cu��Fe��Ũ�����γɵ�ԭ����У�Cu��������Fe����������C��ȷ��
D���ڸ�����Ʒ����Ƕп�鹹��ԭ����Է��θ������⣬Fe��ԭ��ص�����������������������������������������D����
��ѡC��
���� ���⿼����ԭ���ԭ����֪��ԭ��ط�Ӧ�ص㡢���������жϷ������ɽ���״�ѡ����C��ע�⣺���ܸ��ݽ����Ļ�����ǿ���ж���������Ҫ����ʧ���ӵ����׳̶��ж���������Ϊ�״��㣻��Ŀ�ѶȲ���


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
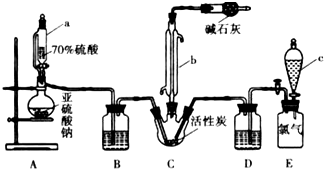 �����ȣ�SO2Cl2����һ����Ҫ�Ļ����Լ���ʵ���Һϳ������ȵ�ʵ��װ����ͼ��ʾ��
�����ȣ�SO2Cl2����һ����Ҫ�Ļ����Լ���ʵ���Һϳ������ȵ�ʵ��װ����ͼ��ʾ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
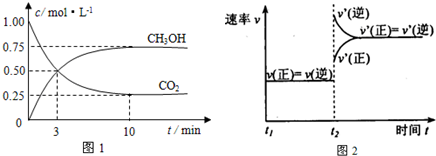
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
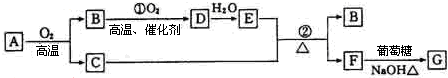
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | һ�� | B�� | ���� | C�� | ���� | D�� | ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ѡ�� | X | Y |
| A | Al | NaOH��Һ |
| B | NO2 | H2O |
| C | Na2O2 | CO2 |
| D | Cu | ŨHNO3 |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 0.25 | B�� | 0.1 | C�� | 0.5 | D�� | 0.05 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com