
【题目】某混合物A含有KAl(SO4)2、Al2O3和Fe2O3,在一定条件下可实现下图所示的物质之间的变化:

据此回答下列问题:
(1)I、II、III、IV四步中对于溶液和沉淀的分离采取的方法是____________。
(2)根据上述框图反应关系,写出下列B、D、E所含物质的化学式
固体B_________________;沉淀D __________________;
溶液E_________________________________________。
(3)写出①、④两个反应的化学方程式
①__________________________________;④_____________________________。
(4)写出②、③两个反应的离子方程式
②_________________________________;③______________________________。
(5)设计实验检验溶液F中所含溶质:______________________________________
(6)分别写出Al2O3和Fe2O3在工业上的一种主要用途:
Al2O3__________________________Fe2O3____________________________
【答案】 过滤 Al2O3 Fe2O3 K2SO4和(NH4)2SO4。 Al2O3+2NaOH=2NaAlO2+H2O 2Al(OH)3![]() Al2O3+3H2O Al3++3NH3·H2O=Al(OH)3↓+3 NH4+ AlO2-+H++H2 O=Al(OH)3↓ 取F溶液少许于两支试管中,一支中滴加KSCN溶液,若显血红色证明F溶液中含有Fe3+;在另一支试管中加入稀硝酸酸化然后再加入硝酸银溶液,若有白色沉淀生成证明F溶液中含有Cl—。 Al2O3:冶炼铝 耐火材料 Fe2O3:炼铁原料 红色油漆 涂料
Al2O3+3H2O Al3++3NH3·H2O=Al(OH)3↓+3 NH4+ AlO2-+H++H2 O=Al(OH)3↓ 取F溶液少许于两支试管中,一支中滴加KSCN溶液,若显血红色证明F溶液中含有Fe3+;在另一支试管中加入稀硝酸酸化然后再加入硝酸银溶液,若有白色沉淀生成证明F溶液中含有Cl—。 Al2O3:冶炼铝 耐火材料 Fe2O3:炼铁原料 红色油漆 涂料
【解析】本题分析:本题主要考查铝、铁等元素化合物的性质。
(1)I、II、III、IV四步中对于溶液和沉淀的分离采取的方法是过滤。
(2)固体B是氢氧化铝的受热分解产物Al2O3 ;沉淀D 是不溶于氢氧化钠溶液的 Fe2O3;溶液E含有K2SO4和(NH4)2SO4。
(3)①、④两个反应的化学方程式:①Al2O3+2NaOH=2NaAlO2+H2O;④2Al(OH)3![]() Al2O3+3H2O。
Al2O3+3H2O。
(4)②、③两个反应的离子方程式:②Al3++3NH3·H2O=Al(OH)3↓+3 NH4+ ;③ AlO2-+H++H2 O=Al(OH)3↓ 。
(5)沉淀D 是 Fe2O3,溶于适量盐酸得到氯化铁溶液,检验溶液F中所含溶质就是检验Fe 3+和Cl—。检验方法:取F溶液少许于两支试管中,一支中滴加KSCN溶液,若显血红色证明F溶液中含有F3+;在另一支试管中加入稀硝酸酸化然后再加入硝酸银溶液,若有白色沉淀生成证明F溶液中含有Cl—。
(6)Al2O3:冶炼铝 耐火材料 Fe2O3:炼铁原料 红色油漆 涂料


 开心练习课课练与单元检测系列答案
开心练习课课练与单元检测系列答案科目:高中化学 来源: 题型:
【题目】(1)已知咖啡酸的结构如图所示。关于咖啡酸的描述正确的是:(______)
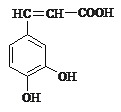
A.分子式为C9H5O4
B.1 mol 咖啡酸最多可与5 mol 氢气发生加成反应
C.与溴水既能发生取代反应,又能发生加成反应
D.1 mol 咖啡酸最多可与3 mol Na2CO3发生反应
(2)A、B、C、D1、D2、E、F、G、H均为有机化合物,请根据下列图示回答问题。
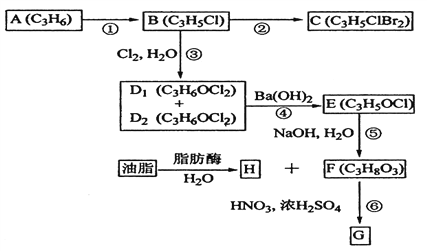
(1)直链有机化合物A的结构简式是__________________;
(2)B中官能团的名称为___________,H中含氧官能团的结构简式为____________;
(3)①的反应试剂和反应条件是___________________,③的反应类型是_____________;
(4)B生成C的化学方程式是___________________;
D1或D2生成E的化学方程式是___________________;
(5)G可应用于医疗、爆破等,由F生成G的化学方程式是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在通常条件下,下列各组物质的性质排列正确的是( )
A.熔点:Na>MgO>SiO2
B.水溶性:SO2>H2S>HCl
C.热稳定性:HF>H2O>NH3
D.沸点:HF>HCl>HBr
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镁化合物具有广泛用途。请回答有关镁的下列问题:
(1)单质镁在空气中燃烧的主要产物是白色的____,还生成少量的______(填化学式);
(2)CH3MgCl是一种重要的有机合成试剂,其中镁的化合价是___________,该化合物水解的化学方程式为____________;
(3)下图是金属镁和卤素反应的能量变化图(反应物和产物均为298K时的稳定状态)。
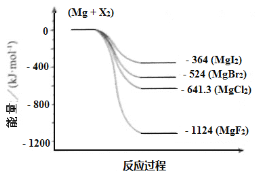
下列选项中正确的是_____________(填序号)。
① MgI2中Mg2+ 与I- 间的作用力小于MgF2中Mg2+ 与F- 间的作用力
② Mg与F2的反应是吸热反应
③ MgBr2与Cl2 反应的△H > 0
④ 化合物的热稳定性顺序为MgI2 < MgBr2 < MgCl2 < MgF2
⑤ MgF2(s) + Br2(l) = MgBr2(s) + F2(g) △H = +600 kJ · mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述中错误的是( )。
A.带相反电荷离子之间的相互吸引力称为离子键
B.金属元素与非金属元素化合时,不一定形成离子键
C.某元素的原子最外层只有一个电子,它跟卤素结合时所形成的化学键不一定是离子键
D.非金属原子间也可能形成离子键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可以充分说明反应 P(g)+Q(g)![]() R(g)+S(g)在恒温下已达到平衡的是
R(g)+S(g)在恒温下已达到平衡的是
A.反应容器内的压强不随时间改变
B.反应容器内P、Q、R、S四者浓度之比为1︰1︰1︰1
C.P的生成速率和S的生成速率相等
D.反应容器内的气体总物质的量不随时间变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】MnO2是常见的氧化剂、催化剂和活性电极材料。
(1)工业上,以惰性材料为电极,电解MaSO4溶液(含少量稀硫酸)制备MnO2。写出阳极的电极反应式:_________________________________。
(2)已知如下热化学方程式(K代表平衡常数):
①MnCO3(s)![]() Mn0(s)+CO2(g)△H1 K1
Mn0(s)+CO2(g)△H1 K1
②2MnO(s)+O2(g)![]() 2MnO2(s)△H2 K2
2MnO2(s)△H2 K2
③2MnCO3(n)+O2(g)![]() 2MnO2(s)+2CO2(g)△H3 K3
2MnO2(s)+2CO2(g)△H3 K3
△H3=________用△H1,△H2表示);K3=________用K1、K2表示)。
(3)反应②在低温条件下能自发进行,则△H3________0(填“>"“<"或“=")。
(4)在密闭容器中投入足量的MnCO3,一定条件下发生反应MnCO3(s)![]() MnO(s)+CO2(g) △H>0。在一定湿度下,达到平衡状态时ρ(CO2)=2aMPa。
MnO(s)+CO2(g) △H>0。在一定湿度下,达到平衡状态时ρ(CO2)=2aMPa。
①温度、压强对MnCO3分解率的影响如图所示:
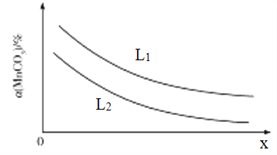
比较:L1__________L2(填“>"“<”或“=")。
②保持温度不变,将容器休积扩大至原来的2倍,则ρ(CO2)的变化范围是____________。
③保持温度不变,将容器体积压缩至原来的一半,达到新平衡时下列物理量一定不变的是____(填代号)。
A.平衡常数K B.c(CO2) C.n(CO2) D.m(MnCO3)
(5)一定温度下,在容积为2L的恒容密闭容器中加入足量的MnCO3(s)和5molO2,发生反应:2MnCO3(s)+O2(g)![]() 2MnO2(s)+2CO2(g),CO2以平均速率为0.1mol·L-1·min-1经过10min达到平衡状态,该条件下该反应的平衡常数K为______________。
2MnO2(s)+2CO2(g),CO2以平均速率为0.1mol·L-1·min-1经过10min达到平衡状态,该条件下该反应的平衡常数K为______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】环境保护是当今倍受人们关注的社会问题.下列叙述不正确的是( )
A.二氧化硫会形成酸雨
B.氮氧化物会形成光化学烟雾
C.过度使用煤作能源会引起雾霾等环境危害
D.一氧化碳是造成温室效应的主要物质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列实验事实:
(1)X+Y2+===X2++Y
(2)Z+2H2O![]() Z(OH)2+H2↑
Z(OH)2+H2↑
(3)Z2+离子的氧化性比X2+弱
(4)由Y、W作电极组成的原电池反应为:Y-2e-===Y2+
由此可知,X、Y、Z、W的还原性由强到弱的顺序是()
A. X>Y>Z>W B. Y>X>W>Z
C. Z>X>Y>W D. Z>Y>X>W
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com