
| A. | 等质量的碳酸钠和碳酸氢钠分别与足量盐酸反应,碳酸氢钠产生的二氧化碳多 | |
| B. | 等物质的量的盐酸分别与足量的碳酸钠和碳酸氢钠反应,碳酸氢钠产生的二氧化碳多 | |
| C. | 相同温度在水中的溶解度:碳酸钠大于碳酸氢钠 | |
| D. | 用氢氧化钙溶液鉴别碳酸钠和碳酸氢钠两种溶液 |
分析 A、利用n=m/M,可计算物质的量,因酸足量,利用Na2CO3~CO2,NaHCO3~CO2来分析;
B.利用等物质的量的盐酸,因盐足量,利用2HCl~CO2,HCl~CO2来分析;
C、碳酸钠较碳酸氢钠易溶;
D、氢氧化钙和碳酸钠反应生成碳酸钙沉淀,和碳酸氢钠溶液反应也发生反应生成碳酸钙沉淀.
解答 解:A、设质量都是106g,则Na2CO3和NaHCO3的物质的量分别为1mol、$\frac{106}{84}$mol,根据Na2CO3~CO2,NaHCO3~CO2,产生的CO2的物质的量分别为1mol、$\frac{106}{84}$mol,故A正确;
B、盐酸分别与足量碳酸钠和碳酸氢钠,因盐酸不足且相等,根据2HCl~CO2,HCl~CO2,前者产生二氧化碳是后者的一半,故B正确;
C、常温下相同的溶剂时,Na2CO3较NaHCO3易溶,故C正确.
D、氢氧化钙和碳酸钠反应生成碳酸钙沉淀,和碳酸氢钠溶液反应也发生反应生成碳酸钙沉淀,不能用于鉴别碳酸钠和碳酸氢钠,故D错误;
故选:D.
点评 本题考查Na2CO3和NaHCO3性质的异同,题目难度不大,注意把握Na2CO3和NaHCO3性质,注重基础知识的积累.


 口算能手系列答案
口算能手系列答案科目:高中化学 来源: 题型:选择题
| A. | 用小苏打治疗胃酸过多:2H++CO32-═H2O+CO2↑ | |
| B. | 氯化铝溶液中加入过量氨水:Al3++4NH3•H2O═AlO2-+4NH4++2H2O | |
| C. | 向NaHSO4溶液中滴加Ba(OH)2溶液至恰好为中性:2H++SO42-+Ba2++2OH-═BaSO4↓+2H2O | |
| D. | 碳酸氢钠溶液与过量的氢氧化钙溶液:Ca2++2HCO3-+2OH-═CaCO3↓+CO32-+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
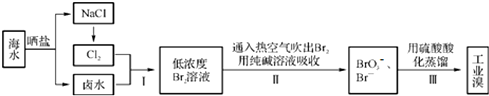
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 钠熔成光亮的小球,在液面四处游动 | |
| B. | 有气体产生 | |
| C. | 溶液底部有银白色的物质 | |
| D. | 溶液变浑浊 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 成分 | 质量(g) | 摩尔质量(g•mol-1) |
| 蔗糖 | 50.00 | 342 |
| 硫酸钾 | 0.50 | 174 |
| 阿司匹林 | 0.35 | 180 |
| 高锰酸钾 | 0.50 | 158 |
| 硝酸银 | 0.04 | 170 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com