
| A. | CH3COOH与HCN均为弱酸 | |
| B. | 常温下,等浓度CH3COONa溶液的pH小于NaCN溶液的pH | |
| C. | 在CH3COONa溶液中,c(Na+)+c(H+)═c(CH3COO-)+c(CH3COOH) | |
| D. | 在NaCN溶液中,c(Na+)>c(CN-) |
分析 常温下,已知0.1mol/L的CH3COOH和HCN溶液的pH分别为a、b,且1<a<b,说明都是弱酸,而同浓度PH值越大,酸的电离程度越小,对应的酸越弱,结合物料守恒分析解答.
解答 解:A、因为常温下,已知0.1mol/L的CH3COOH和HCN溶液的pH分别为a、b,且1<a<b,所以两种酸都弱酸,故A正确;
B、酸越弱对应酸根离子水解能力越强,所以等浓度CH3COONa溶液的水解程度小于NaCN溶液的水解程度,所以pH(NaCN)>pH(CH3COONa),故B正确;
C、根据物料守恒,在CH3COONa溶液中,钠离子的浓度与醋酸离子所有存在形式的浓度相等,所以c(Na+)═c(CH3COO-)+c(CH3COOH),故C错误;
D、在NaCN溶液中,弱离子CN-水解,导致c(Na+)>c(CN-),故D正确;
故选C.
点评 本题考查了弱电解质的电离,明确弱电解质电离程度与弱酸根离子水解程度的关系即可解答,注意两种弱酸同浓度PH值越大,酸的电离程度越小.


 一卷搞定系列答案
一卷搞定系列答案 名校作业本系列答案
名校作业本系列答案 轻巧夺冠周测月考直通名校系列答案
轻巧夺冠周测月考直通名校系列答案科目:高中化学 来源: 题型:解答题
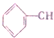 =CH2 D.
=CH2 D.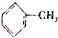
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 试管 | 操作 | 现象 |
| a | 在试管中加入NaBr溶液,滴加少量氯水,用力振荡后,再加入少量CCl4,振荡静置 | CCl4层由无色逐渐变为橙红色 |
| b | ⅰ.在试管中加入FeCl2溶液,滴加两滴KSCN溶液 ⅱ.加入少量溴水,振荡 | ⅰ.浅绿色溶液无明显变化 ⅱ.溶液变为红色 |
| 操作 | A中现象 |
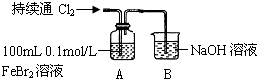 | ⅰ.开始通入100mL(折合标准状况)Cl2,溶液由浅绿色逐渐变黄 ⅱ.继续通入Cl2,溶液黄色加深,当变为棕黄色后,停止通入Cl2 |
| 试管 | 操作 | 现象 |
| c | 滴加2-3滴KSCN溶液,振荡 | 溶液变为血红色 |
| d | 加入少量CCl4,振荡,静置 | 出现分层现象,下层为四氯化碳,且呈无色 |
| 试管 | 操作 | 现象 |
| e | 在试管中加入2mL棕黄色溶液,加入少量CCl4,振荡,静置 | CCl4层由无色变为橙红色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 酸性强弱:H2SiO3<H2CO3<H2SO4 | B. | 热稳定性:HCl>HBr>HI | ||
| C. | 原子半径:Na<Mg<Al | D. | 熔点:SiO2>NaCl>CO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CO2通入可溶性硅酸盐中析出硅酸沉淀 | |
| B. | CO2溶于水形成碳酸,SiO2难溶于水 | |
| C. | 高温下SiO2与碳酸盐反应生成CO2 | |
| D. | 氯化氢通入碳酸钠溶液中放出气体,通入硅酸钠溶液中生成沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氧化铝的熔点很低,不能用于制作耐高温材料 | |
| B. | 光化学烟雾与大量排放碳氢化合物和氮氧化合物有关 | |
| C. | 无水乙醇用作医用消毒剂效果更好 | |
| D. | Na、S、C分别在氧气中点燃均可得到两种不同的氧化物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ③④ | C. | ②④ | D. | ①③ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 5.6g铁与足量稀硫酸反应转移的电子数为0.3NA | |
| B. | 标准状况下,11.2L水中含有分子的数目为0.5NA | |
| C. | 500 mL 0.2 mol•L-1 CaCl2溶液中氯离子数目为 0.1NA | |
| D. | 1.6g由氧气和臭氧组成的混合物中含有氧原子的数目为0.1NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com