
根据以下三个热化学方程式:
2H2S(g)+3O2(g)===2SO2(g)+2H2O(l)
ΔH=-Q1 kJ·mol-1
2H2S(g)+O2(g)===2S(s)+2H2O(l)
ΔH=-Q2 kJ·mol-1
2H2S(g)+O2(g)===2S(s)+2H2O(g)
ΔH=-Q3 kJ·mol-1
判断Q1、Q2、Q3三者关系正确的是( )
A.Q1>Q2>Q3 B.Q1>Q3>Q2
C.Q3>Q2>Q1 D.Q2>Q1>Q3
科目:高中化学 来源: 题型:
某有机物n g,跟足量金属钠反应生成V L H2,另取n g该有机物与足量碳酸氢钠作用生成V L CO2(相同状况下),该有机物分子中含有的官能团为( )
A.含一个羧基和一个羟基
B.含两个羧基
C.只含一个羧基
D.含两个羟基
查看答案和解析>>
科目:高中化学 来源: 题型:
新型高效的甲烷燃料电池采用铂为电极材料,两电极上分别通入CH4和O2 ,电解质为KOH溶液。某研究小组将两个甲烷燃料电池串联后作为电源,进行饱和氯化钠溶液电解实验,如图所示。
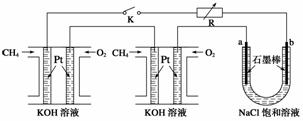
回答下列问题:
(1)甲烷燃料电池正极、负极的电极反应分别为___________________________________
________________、_______________________________________________________。
(2)闭合K开关后,a、b电极上均有气体产生,其中b电极上得到的是__________,电解氯化钠溶液的总反应方程式为_______________________________________________;
(3)若每个电池甲烷通入量为1 L(标准状况),且反应完全,则理论上通过电解池的电量为__________(法拉第常数F=9.65×104 C · mol-1,列式计算),最多能产生的氯气体积为________L(标准状况)。
查看答案和解析>>
科目:高中化学 来源: 题型:
在以下过程中发生水解反应的是( )
A.棉织物滴浓硫酸变黑
B.皮肤上沾了浓硝酸后变黄
C.氨基酸之间反应,生成多肽
D.蛋白质在适当条件下生成氨基酸
查看答案和解析>>
科目:高中化学 来源: 题型:
在下列各说法中,正确的是( )
A.ΔH>0表示放热反应,ΔH<0表示吸热反应
B.热化学方程式中的化学计量数只表示物质的量,可以是分数
C.1 mol H2SO4与1 mol Ba(OH)2反应生成BaSO4沉淀时放出的热叫做中和热
D.1 mol H2与0.5 mol O2反应放出的热就是H2的标准燃烧热
查看答案和解析>>
科目:高中化学 来源: 题型:
以铬酸钾为原料,电化学法制备重铬酸钾的实验装置示意图如下:
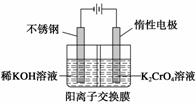
下列说法不正确的是( )
A.在阴极室,发生的电极反应为2H2O+2e-===2OH-+H2↑
B.在阳极室,通电后溶液逐渐由黄色变为橙色,是因为阳极区H+浓度增大,使平衡2CrO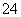 +2H+Cr2O
+2H+Cr2O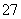 +H2O向右移动
+H2O向右移动
C.该制备过程中总反应的化学方程式为4K2CrO4+4H2O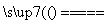 2K2Cr2O7+4KOH+2H2↑+O2↑
2K2Cr2O7+4KOH+2H2↑+O2↑
D.测定阳极液中K和Cr的含量,若K与Cr的物质的量之比(nK/nCr)为d,则此时铬酸钾的转化率为1-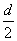
查看答案和解析>>
科目:高中化学 来源: 题型:
用如图所示的装置进行电解,在通电一段时间后,铁电极的质量增加。

(1)写出乙中两极发生的电极反应式。
阴极:________________________________________________________________________;
阳极:________________________________________________________________________。
(2)写出甲中发生反应的化学方程式:___________________________________________。
(3)C(左)、C(右)、Fe、Ag 4个电极上析出或溶解物质的物质的量之比是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
在密闭容器中,使2 mol N2和6 mol H2混合发生下列反应:N2(g)+3H2(g)2NH3(g) ΔH<0
(1)当反应达到平衡时,N2和H2的浓度比是________;N2和H2的转化率比是________。
(2)升高平衡体系的温度(保持体积不变),混合气体的平均相对分子质量__________,密度__________。(填“变大”、“变小”或“不变”)
(3)当达到平衡时,充入氩气,并保持压强不变,平衡将________(填“正向”、“逆向”或“不”)移动。
(4)若容器恒容、绝热,加热使容器内温度迅速升至原来的2倍,平衡将________(填“向左移动”、“向右移动”或“不移动”)。达到新平衡后,容器内温度________(填“大于”、“小于”或“等于”)原来的2倍。
查看答案和解析>>
科目:高中化学 来源: 题型:
汉代器物上的颜料“汉紫”至今尚没有发现其自然存在的记载。20世纪80年代科学家进行超导材料研究时,偶然发现其成分为紫色的硅酸铜钡(化学式:BaCuSi2Ox,Cu为+2价),下列有关“汉紫”的说法中不正确的是( )
A.用盐的形式表示:BaSiO3·CuSiO3 B.用氧化物形式表示:BaO·CuO·2SiO2
C.易溶于强酸、强碱 D.性质稳定,不易褪色
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com