
现有A、B、C、D、E、F、G七种核电荷数小于18的元素,它们的原子序数一次递增.其中:A原子核内无中子,B原子最外层电子数是次外层的2倍,D原子最外层电子数是其电子层数的3倍,E原子核外第一层比第三层电子数多1,F的最外层电子数等于第一层电子数,G形成的﹣1价离子与Ar原子核外电子排布相同;
由此推知:
(1)A原子符号是 ;
(2)B原子结构示意图是
(3)G元素形成的单质与A、D、E三元素形成呈碱性的化合物反应的离子方程式:
单质F分别在C单质、BD元素形成的化合物中燃烧的化学方程式: ; .
考点:
原子结构与元素的性质.
专题:
元素周期律与元素周期表专题.
分析:
A、B、C、D、E、F、G七种核电荷数小于18的元素,它们的原子序数依次递增.其中:A原子核内无中子,则A是H元素,B原子最外层电子数是次外层的2倍,则B是C元素,D原子最外层电子数是其电子层数的3倍,则D是O元素,C的原子序数大于B小于D,所以C是N元素,E原子核外第一层比第三层电子数多1,则E是Na元素,F的最外层电子数等于第一层电子数,且F的原子序数大于E,所以F是Mg元素,G形成的﹣1价离子与Ar原子核外电子排布相同,则G是Cl元素.
解答:
解:A、B、C、D、E、F、G七种核电荷数小于18的元素,它们的原子序数依次递增.其中:A原子核内无中子,则A是H元素,B原子最外层电子数是次外层的2倍,则B是C元素,D原子最外层电子数是其电子层数的3倍,则D是O元素,C的原子序数大于B小于D,所以C是N元素,E原子核外第一层比第三层电子数多1,则E是Na元素,F的最外层电子数等于第一层电子数,且F的原子序数大于E,所以F是Mg元素,G形成的﹣1价离子与Ar原子核外电子排布相同,则G是Cl元素.
(1)因A为H元素,则A原子符号是11H,故答案为:11H;
(2)B为C元素,C原子结构示意图为 ,故答案为:
,故答案为: ;
;
(3)G元素形成的单质是氯气,A、D、E三元素形成呈碱性的化合物是氢氧化钠,氯气和氢氧化钠溶液反应的离子方程式为:2OH﹣+Cl2═Cl﹣+ClO﹣+H2O,镁分别在氮气、二氧化碳中燃烧的化学方程式为:3Mg+N2 Mg3N2,2Mg+CO2
Mg3N2,2Mg+CO2 2MgO+C,故答案为:2OH﹣+Cl2═Cl﹣+ClO﹣+H2O;3Mg+N2
2MgO+C,故答案为:2OH﹣+Cl2═Cl﹣+ClO﹣+H2O;3Mg+N2 Mg3N2;2Mg+CO2
Mg3N2;2Mg+CO2 2MgO+C.
2MgO+C.
点评:
本题考查原子结构与性质的关系,正确推断元素是解本题的关键,注意镁在二氧化碳中能燃烧,为易错点.


科目:高中化学 来源: 题型:
一定条件下,在密闭容器中进行反应3SiCl4(g)+2N2(g)+6H2(g)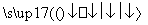 Si3N4(s)+12HCl(g),能表示上述反应达到化学平衡状态的是( )
Si3N4(s)+12HCl(g),能表示上述反应达到化学平衡状态的是( )
A.3v逆(N2)=v正(H2)
B.v正(HCl)=4v正(SiCl4)
C.混合气体密度保持不变
D.c(N2):c(H2):c(HCl)=1:3:6
查看答案和解析>>
科目:高中化学 来源: 题型:
将质量相等的铁片和铜片用导线相连浸入500mL硫酸铜溶液中构成如图1的装置:(以下均假设反应过程中溶液体积不变).
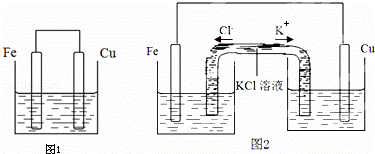
(1)铁片上的电极反应式为 .
(2)铜片周围溶液会出现 的现象.
(3)若2min后测得铁片和铜片之间的质量差为1.2g,计算:
①导线中流过的电子的物质的量为 mol;
②该段时间内用硫酸铜表示的平均反应速率为 mol•L﹣1•min﹣1
(4)若一段时间后测得铁片减少了2.4g,同时铜片增加了3.2g,计算这段时间内该装置消耗的化学能转化为电能的百分比为 .
(5)若将该装置改为如图2所示的装置也能达到和原装置相同的作用.其中KCl溶液起沟通两边溶液形成闭合回路的作用,同时又能阻止反应物直接接触.则硫酸铜溶液应该注入 (填“左侧”、“右侧”或“两侧”)烧杯中.
查看答案和解析>>
科目:高中化学 来源: 题型:
某工厂排放的工业废水中可能含有K+、Ag+、NH4+、Mg2+、SO42﹣、Cl﹣、NO3﹣、HCO3﹣等离子.经检测废水呈明显的碱性,则可确定该厂废水中肯定不含有的离子组合是( )
|
| A. | Ag+、K+、NO3﹣、HCO3﹣ | B. | K+、NH4+、NO3﹣、SO42﹣ |
|
| C. | Ag+、NH4+、Mg2+、HCO3﹣ | D. | K+、Mg2+、SO42﹣、Cl﹣ |
查看答案和解析>>
科目:高中化学 来源: 题型:
某溶液中只含有Na+、Al3+、Cl﹣、SO42﹣ 四种离子,已知前三种离子的个数比为3:2:1,则溶液中Al3+和 SO42﹣的离子个数比为( )
|
| A. | 1:2 | B. | 1:4 | C. | 3:4 | D. | 3:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列做法正确的是( )
A.将浓硝酸保存在无色玻璃瓶中
B.金属钠和钾保存在煤油中
C.Na2CO3可以保存在玻璃塞的玻璃瓶中
D.NaOH固体放在滤纸上称量
查看答案和解析>>
科目:高中化学 来源: 题型:
为除去括号内的杂质,所选用的试剂或方法不正确的是
( )
A.Na2CO3溶液(NaHCO3),选用适量的NaOH溶液
B.NaHCO3溶液(Na2CO3),应通入足量的CO2气体
C.Na2O2粉末(Na2O),将混合物在氧气中加热
D.Na2CO3溶液(Na2SO4),加入适量的Ba(OH)2溶液,过滤
查看答案和解析>>
科目:高中化学 来源: 题型:
2000K时,反应CO(g)+ O2(g)⇌CO2(g)的平衡常数为K,则相同温度下反应2CO2(g)⇌2CO(g)+O2(g)的平衡常数K′为( )
O2(g)⇌CO2(g)的平衡常数为K,则相同温度下反应2CO2(g)⇌2CO(g)+O2(g)的平衡常数K′为( )
|
| A. |
| B. | K2 | C. |
| D. |
|
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法中正确的是( )
|
| A. | 1molO的质量是16g/mol |
|
| B. | 2g H2的物质的量是 1 |
|
| C. | CO2的相对分子质量为44,1 molCO2的质量为44 g/mol |
|
| D. | NaCl的摩尔质量是58.5g/mol |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com