
ĻĀĮŠĶ¼Ź¾Óė¶ŌÓ¦ŠšŹöĻą·ūµÄŹĒ
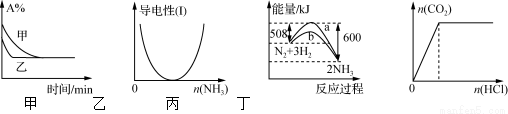
A£®Ķ¼¼×±ķŹ¾Ń¹Ēæ¶ŌæÉÄę·“Ó¦2A(g)£«2B(g) 3C(g)£«D(s)µÄÓ°Ļģ£¬ŅŅµÄŃ¹Ēæ“ó
3C(g)£«D(s)µÄÓ°Ļģ£¬ŅŅµÄŃ¹Ēæ“ó
B£®Ķ¼ŅŅ±ķŹ¾CH3COOHČÜŅŗÖŠĶØČėNH3ÖĮ¹żĮæµÄ¹ż³ĢÖŠČÜŅŗµ¼µēŠŌµÄ±ä»Æ
C£®Ķ¼±ū±ķĆ÷ŗĻ³É°±·“Ó¦ŹĒ·ÅČČ·“Ó¦£¬b±ķŹ¾ŌŚ·“Ó¦ĢåĻµÖŠ¼ÓČėĮĖ“߻ƼĮ
D£®Ķ¼¶”±ķŹ¾Ņ»¶ØÅضČNa2CO3ČÜŅŗÖŠµĪ¼ÓŃĪĖį£¬Éś³ÉCO2ÓėµĪ¼ÓŃĪĖįĪļÖŹµÄĮæµÄ¹ŲĻµ
 »„¶ÆÓ¢ÓļĻµĮŠ“š°ø
»„¶ÆÓ¢ÓļĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2017½ģɽ¶«Ź”øßČżÉĻѧʌµŚŅ»“ĪŌĀæ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
Na2O2”¢HCl”¢Al2O3 ČżÖÖĪļÖŹŌŚĖ®ÖŠĶźČ«·“Ó¦ŗó£¬ČÜŅŗÖŠÖ»ŗ¬ÓŠNa£«”¢H£«”¢ClØD”¢OHØD£»ĒŅČÜŅŗ³ŹÖŠŠŌ£¬ŌņNa2O2”¢HCl”¢Al2O3µÄĪļÖŹµÄĮæÖ®±ČæÉÄÜĪŖ ( )
A£®3:2:1 B£®2:4:1 C£®2:3:1 D£®4:2:1
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2017½ģ½Ī÷Ź”µČĮłŠ£øßČżÉĻѧʌµŚŅ»“ĪĮŖæ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗĢīæÕĢā
¢ÅŅŃÖŖĢ¼Ėį¶ž¼¶µēĄė½ĻĘ«ĀĮĖįµÄµēĄėČŻŅ×£¬¶ųŹÆĢæĖįµÄµēĄė½éÓŚĢ¼ĖįµÄŅ»¼¶µēĄėÓė¶ž¼¶µēĄėÖ®¼ä”£ĻĀĆęµÄĶĘĀŪÕżČ·µÄŹĒ_________________£ŗ
¢Ł½«CO2ĶØČėĘ«ĀĮĖįÄĘČÜŅŗÖŠ£¬ČÜŅŗ±ä»ė×Ē£¬²¢Éś³ÉĢ¼ĖįÄĘ»ņĢ¼ĖįĒāÄĘ£»¢Ś½«CO2ĶØČėC6H5ONaČÜŅŗÖŠ£¬Ąė×Ó·“Ó¦Ź½ĪŖCO2+H2O+2C6H5O”Ŗ 2 C6H5OH+CO32”Ŗ£»
2 C6H5OH+CO32”Ŗ£»
¢ŪHCO3”ŖŌŚČÜŅŗÖŠ¼ČÄÜÓėAlO2”ŖÓÖÄÜÓėAl3+·“Ó¦£¬ĒŅ¶¼·¢ÉśĖ«Ė®½ā£»¢ÜĶłŗ¬ÓŠ“óĮæCO32”ŖµÄČÜŅŗÖŠ¼ÓČėC6H5OHµĆµ½³ĪĒåČÜŅŗ£¬·Å³öCO2ĘųĢ壻¢ŻĻņAl(OH)3µÄ»ģ×ĒŅŗÖŠ¼ÓČėNa2CO3ČÜŅŗµĆ²»µ½³ĪĒåČÜŅŗ£»¢ŽĻąĶ¬ĪĀ¶Č£¬ĻąĶ¬ÅØ¶ČµÄNa2CO3”¢C6H5ONa”¢NaHCO3”¢NaAlO2µÄĻ”ČÜŅŗPHŅĄ“ĪŌö“ó”£
(2)Ē³ĀĢÉ«µÄFe(NO3)2ČÜŅŗÖŠ£¬“ęŌŚČēĻĀĘ½ŗā£ŗFe2++2H2O Fe(OH) 2+2H+ČōŌŚ“ĖČÜŅŗÖŠ¼ÓČėŃĪĖįŗó£¬ÓĆĪÄ×ÖĖµĆ÷ČÜŅŗŃÕÉ«µÄ±ä»Æ¼°ŌŅņ__________________.
Fe(OH) 2+2H+ČōŌŚ“ĖČÜŅŗÖŠ¼ÓČėŃĪĖįŗó£¬ÓĆĪÄ×ÖĖµĆ÷ČÜŅŗŃÕÉ«µÄ±ä»Æ¼°ŌŅņ__________________.
¢ĒŅ»øöĶźÕūµÄŃõ»Æ»¹Ō·“Ó¦·½³ĢŹ½æÉŅŌ²šæŖ£¬Š“³ÉĮ½øö”°°ė·“Ó¦Ź½”±£¬Ņ»øöŹĒ”°Ńõ»Æ·“Ó¦Ź½”±£¬Ņ»øöŹĒ”°»¹Ō·“Ó¦Ź½”±”£Čē2Fe3++Cu£½2Fe2++Cu2+£¬æɲšŠ“ĪŖŃõ»Æ·“Ó¦Ź½£ŗCu£2e££½Cu2+£¬»¹Ō·“Ó¦Ź½£ŗ2Fe3++2e££½2Fe2+”£¾Ż“Ė£¬»Ų“šĻĀĮŠĪŹĢā£ŗ
¢Ł½«·“Ó¦3 Cu+8H+ +2NO3££½3Cu2++2NO”ü+4H2O²šŠ“ĪŖĮ½øö”°°ė·“Ó¦Ź½”±£ŗ
»¹Ō·“Ó¦Ź½£ŗ ”£
¢ŚŅŃÖŖij·“Ó¦µÄĮ½øö”°°ė·“Ó¦Ź½”±ĪŖ£ŗ
CH4+10 OH££8e££½CO32£+7H2O£¬ O2+2H2O+4e££½ 4OH££¬
ŌņŃõ»Æ»¹Ō·“Ó¦·½³ĢŹ½ĪŖ ”£
¢Ū“ĖŌĄķæÉÓĆÓŚµē»Æѧ”£Šæ”ŖĆĢ¼īŠŌµē³Ų¹ć·ŗÓ¦ÓĆÓŚČÕ³£Éś»ī”£µē³ŲµÄ×Ü·“Ó¦Ź½ĪŖZn(s)+2MnO2(s)+2H2O(l)===Zn(OH)2(s)+2MnOOH(s)”£
øƵē³ŲµÄÕż¼«·“Ó¦Ź½ĪŖ ”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2017½ģ½Ī÷Ź”µČĮłŠ£øßČżÉĻѧʌµŚŅ»“ĪĮŖæ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
»ÆѧÓėÉē»į”¢Éś²ś”¢Éś»ī½ōĆÜĻą¹Ų”£ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ( )
A£®ŹÆÓ¢Ö»ÄÜÓĆÓŚÉś²ś²£Į§
B£®“Óŗ£Ė®ĢįČ”ĪļÖŹ²»Ņ»¶ØŅŖĶعż»Æѧ·“Ó¦²ÅÄÜŹµĻÖ
C£®¶žŃõ»Æ¹čÄÜÓėĒāŃõ»ÆÄĘČÜŅŗ·“Ó¦£¬¹Ź³£ÓĆĒāŃõ»ÆÄĘČÜŅŗ×÷ĪŖµńæĢ²£Į§µÄŹŌ¼Į
D£®ĪŖĮĖĢįøßĶĮČĄ·ŹĮ¦£¬ĶłĶł½«Ģ¼ļ§ÓėŹģŹÆ»Ņ»ģŗĻŹ¹ÓĆ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2017½ģ½ĖÕŹ”ĖÕÖŻŹŠøßČżÉĻѧʌʌ³õµ÷ŃŠ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
Ņ»¶ØĪĀ¶ČĻĀ£¬ŌŚČżøöĢå»ż¾łĪŖ2.0 LµÄŗćČŻĆܱÕČŻĘ÷ÖŠ·¢ÉśČēĻĀ·“Ó¦£ŗPCl5(g) PCl3(g)£«Cl2(g)
PCl3(g)£«Cl2(g)
±ąŗÅ | ĪĀ¶Č(”ę) | ĘšŹ¼ĪļÖŹµÄĮæ (mol) | Ę½ŗāĪļÖŹµÄĮæ (mol) | “ļµ½Ę½ŗāĖłŠčŹ±¼ä (s) | |
PCl5(g) | PCl3(g) | Cl2(g) | |||
¢ń | 320 | 0.40 | 0.10 | 0.10 | t1 |
¢ņ | 320 | 0.80 | t2 | ||
¢ó | 410 | 0.40 | 0.15 | 0.15 | t3 |
ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
A£®Ę½ŗā³£ŹżK£ŗČŻĘ÷¢ņ£¾ČŻĘ÷¢ó
B£®·“Ó¦µ½“ļĘ½ŗāŹ±£¬PCl5µÄ×Ŗ»ÆĀŹ£ŗČŻĘ÷¢ņ£¼ČŻĘ÷¢ń
C£®·“Ó¦µ½“ļĘ½ŗāŹ±£¬ČŻĘ÷IÖŠµÄĘ½¾łĖŁĀŹĪŖv(PCl5)£½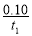 mol”¤L£1”¤s£1
mol”¤L£1”¤s£1
D£®ĘšŹ¼Ź±ĻņČŻĘ÷¢óÖŠ³äČėPCl5 0.30 mol”¢PCl3 0.45 molŗĶCl2 0.10 mol£¬Ōņ·“Ó¦½«ĻņÄę·“Ó¦·½Ļņ½ųŠŠ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2017½ģ½ĖÕŹ”ĖÕÖŻŹŠøßČżÉĻѧʌʌ³õµ÷ŃŠ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ĻĀĮŠÖø¶Ø·“Ó¦µÄĄė×Ó·½³ĢŹ½ÕżČ·µÄŹĒ
A£®ÓĆ“×Ėį³żČ„Ė®¹øÖŠµÄĢ¼ĖįøĘ£ŗCaCO3£«2H£«£½Ca2£«£«H2O£«CO2”ü
B£®ŹÆ»ŅĖ®ÖŠ¼ÓČė¹żĮ抔ĖÕ“ņČÜŅŗ£ŗHCO3££«Ca2+£«OH££½CaCO3”ż£«H2O
C£®µē½ā±„ŗĶNaCl±„ŗĶČÜŅŗ£ŗ2Cl££«2H2O 2OH££«H2”ü£«Cl2”ü
2OH££«H2”ü£«Cl2”ü
D£®ĀĮČÜÓŚĒāŃõ»ÆÄĘČÜŅŗ£ŗAl£«2OH££«H2O£½AlO2££«2H2”ü
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2016-2017ѧğŗÓ±±Ź”ø߶žÉĻ9.21ÖÜæ¼»Æѧ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗ¼ĘĖćĢā
ŅŃÖŖ·“Ó¦FeO(s)£«CO(g)  Fe(s)£«CO2(g) µÄKc£½0.5£Ø1273K£©”£ČōĘšŹ¼ÅضČc(CO)=0.05 mol”¤L£1£¬c(CO2)£½0.01 mol”¤L£1£¬Ēė»Ų“š£ŗ
Fe(s)£«CO2(g) µÄKc£½0.5£Ø1273K£©”£ČōĘšŹ¼ÅضČc(CO)=0.05 mol”¤L£1£¬c(CO2)£½0.01 mol”¤L£1£¬Ēė»Ų“š£ŗ
£Ø1£©ÅŠ¶Ļ»Æѧ·“Ó¦½ųŠŠµÄ·½Ļņ²¢¼ĘĖć·“Ó¦Īļ”¢Éś³ÉĪļµÄĘ½ŗāÅØ¶Č”£
£Ø2£©COµÄ×Ŗ»ÆĀŹŹĒ¶ąÉŁ£æ
£Ø3£©Ōö¼ÓFeOµÄĮ棬¶ŌĘ½ŗāÓŠĪŽÓ°Ļģ£æ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2016-2017ѧğŗÓ±±Ź”ø߶žÉĻ9.21ÖÜæ¼»Æѧ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ĻĀĮŠÓŠ¹ŲĖµ·Ø“ķĪóµÄŹĒ( )
A£®ĪŖ±£»¤ŗ£Āֵē¬æĒ£¬³£ŌŚ“¬æĒÉĻĻāČėŠææé
B£®“æ¼īČÜÓŚČČĖ®ÖŠ£¬Č„ĪŪŠ§¹ūŌöĒ棬ĖµĆ÷“æ¼īµÄĖ®½ā·“Ó¦ŹĒĪüČČ·“Ó¦
C£®ŅŃÖŖ¹¤ŅµŗĻ³É°±Ęų”÷H<0£¬“ļĘ½ŗāŗó£¬ÉżøßĪĀ¶Č£¬Õż·“Ó¦ĖŁĀŹ¼õŠ”£¬Äę·“Ó¦ĖŁĀŹŌö“ó£¬Ę½ŗāĻņÄę·“Ó¦·½ĻņŅʶÆ
D£®NH3(g)+ HCl(g)= NH4Cl(s)½ĻµĶĪĀ¶ČĻĀÄÜ×Ō·¢½ųŠŠ£¬ĖµĆ÷øĆ·“Ó¦µÄ”÷H<0
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2017½ģĖÄ“ØŹ”¹ćŌŖŹŠ²ŌĻŖĻŲøßČżĮćÕļĄķ×Ū»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ŌŚ10 LĆܱÕČŻĘ÷ÖŠ£¬A”¢B”¢CČżÖÖĘųĢ¬ĪļÖŹ¹¹³ÉĮĖæÉÄę·“Ó¦µÄĢåĻµ£»µ±ŌŚÄ³Ņ»ĪĀ¶ČŹ±£¬A”¢B”¢C ĪļÖŹµÄĮæÓėŹ±¼äµÄ¹ŲĻµČēĶ¼¼×£¬CµÄ°Ł·Öŗ¬ĮæÓėĪĀ¶ČµÄ¹ŲĻµČēĶ¼ŅŅ”£ĻĀĮŠ·ÖĪö²»ÕżČ·µÄŹĒ( )
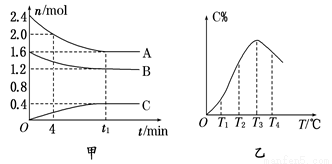
A£®0”«4 minŹ±£¬AµÄĘ½¾ł·“Ó¦ĖŁĀŹĪŖ0.02 mol”¤L£1”¤min£1
B£®øĆ·“Ó¦µÄĘ½ŗā³£Źż±ķ“ļŹ½K£½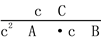
C£®ÓÉT1ĻņT2±ä»ÆŹ±£¬Õż·“Ó¦ĖŁĀŹ“óÓŚÄę·“Ó¦ĖŁĀŹ
D£®øĆ·“Ó¦Õż·“Ó¦ŹĒ·ÅČČ·“Ó¦
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com