
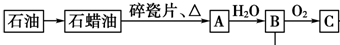
 ,它的一氯取代产物有2种.
,它的一氯取代产物有2种. 分析 A的产量通常衡量一个国家的石油化工水平,则A应为CH2=CH2,与水在一定条件下发生加成反应生成CH3CH2OH,所以B是乙醇,乙醇在Cu或Ag作催化剂条件下发生氧化反应生成C,C结构简式为CH3CHO,以此解答该题.
解答 解:A的产量通常衡量一个国家的石油化工水平,则A应为CH2=CH2,与水在一定条件下发生加成反应生成CH3CH2OH,所以B是乙醇,乙醇在Cu或Ag作催化剂条件下发生氧化反应生成C,C结构简式为CH3CHO,
(1)石蜡油在碎瓷片的作用下加热可得乙烯,碎瓷片的主要作用是催化剂,B是乙醇,B分子中官能团的名称是羟基,
故答案为:催化剂;羟基;
(2)反应B→C是乙醇的催化氧化,反应的化学方程式为2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O,
故答案为:2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O;
(3)丁丁烷的一种同分异构体中含有三个甲基,则这种同分异构体的结构简式是 ,它的一氯取代产物有(CH3)3CCl、(CH3)2CHCH2Cl,共2种,
,它的一氯取代产物有(CH3)3CCl、(CH3)2CHCH2Cl,共2种,
故答案为: ;2.
;2.
点评 本题考查有机物的合成,题目难度不大,注意根据E结合有机物的性质进行推断,学习中注意把握乙酸乙酯的制取,为中学常考查知识点.


科目:高中化学 来源: 题型:解答题
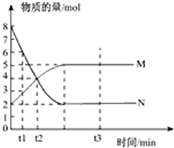 一定温度下,在容积为1L的密闭容器中进行反应:aN(g)?bM(g),M、N的物质的量随时间的变化曲线如图所示:
一定温度下,在容积为1L的密闭容器中进行反应:aN(g)?bM(g),M、N的物质的量随时间的变化曲线如图所示:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分子组成上相差一个或若干个CH2原子团的有机物一定是同系物 | |
| B. | 具有相同的通式且相差一个或若干个CH2原子团的有机物一定是同系物 | |
| C. | 互为同系物的有机物分子结构必然相似 | |
| D. | 互为同系物的有机物通式不一定相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
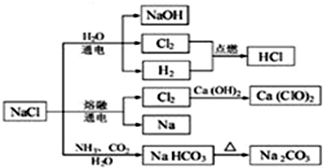
| A. | 上述转化关系图只涉及到氯碱工业、工业制漂白粉及工业制纯碱三个化工原理 | |
| B. | 上述转化关系图涉及的物质中除单质外的所有物质均为电解质 | |
| C. | 工业制纯碱的第一步应在饱和食盐水中先通氨气并达饱和后再通过量CO2 | |
| D. | 将氯气在氢气中点燃可看到产生苍白色火焰并伴有白雾 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C7H8和苯互为同系物 | |
| B. | CH3CH=CHCH3和CH2=CHCH2CH3互为同分异构体 | |
| C. | ${\;}_{2}^{3}$He和${\;}_{2}^{4}$He互为同位素 | |
| D. | 氧气和臭氧互为同素异形体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 二氧化碳能使漂白粉水溶液先变浑浊后变澄清,二氧化硫也有同样现象 | |
| B. | 加热条件下,钠与氧气反应生成过氧化钠,锂与氧气反应也生成过氧化锂 | |
| C. | 常温下,浓硝酸能使铁、铝钝化,浓硫酸也能使铁、铝钝化 | |
| D. | 铁可置换出硫酸铜溶液中的铜,钠也可置换出硫酸铜溶液中的铜 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com