
【题目】有人曾建议用AG表示溶液的酸度(acidity),AG的定义为AG=lg![]() ,下列表述正确的是
,下列表述正确的是
A. 25 ℃时,若溶液呈中性,则pH=7,AG=1
B. 25 ℃时,若溶液呈酸性,则pH<7,AG<0
C. 25 ℃时,若溶液呈碱性,则pH>7,AG>0
D. 25 ℃时,溶液的pH与AG的换算公式为AG=2(7-pH)
科目:高中化学 来源: 题型:
【题目】Ⅰ.已知25℃,NH3·H2O的Kb=1.8×105,H2SO3的Ka1=1.3×102,Ka2=6.2×108。若氨水的浓度为2.0 mol·L1,溶液中的c(OH)=_______mol·L1,0.1 mol·L1的(NH4)2SO3溶液显______(填“酸性”、“碱性”或“中性”)。
Ⅱ. 某学生用0.200mol/L的标准NaOH溶液滴定未知浓度的盐酸,其操作可分为如下几步:
①用蒸馏水洗涤碱式滴定管,并注入NaOH溶液至“0”刻度线以上
②固定好滴定管并使滴定管尖嘴充满液体
③调节液面至“0”或“0”刻度线稍下,并记下读数
④量取20.00mL待测液注入洁净的锥形瓶中,并加入3滴酚酞溶液
⑤用标准液滴定至终点,记下滴定管液面读数
请回答:
(1)以上步骤有错误的是______ (填编号)。
(2)滴定终点的现象为____________________________________________。
(3)用标准NaOH溶液滴定时,应将标准NaOH溶液注入______ 中(从图中选填“甲”或“乙”)。
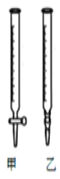
(4)下列操作会引起实验结果偏大的是______![]() 填编号
填编号![]() 。
。
A.在锥形瓶装液前,留有少量蒸馏水
B.滴定前,滴定管尖嘴有气泡,滴定后无气泡
C.滴定终点俯视读数
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中华优秀传统文化涉及到很多的化学知识,下列有关说法错误的是
A.“日照澄洲江雾开”中伴有丁达尔效应
B.古剑“沈卢”以剂钢为刃,柔铁为茎干,不尔则多断折”,剂钢指的是铁的合金
C.“粉身碎骨浑不怕,要留清白在人间”指的是物质发生了物理变化
D.“煤饼烧蛎房成灰![]() 蛎房即牡蛎壳
蛎房即牡蛎壳![]() ”中灰的主要成分为碳酸钙
”中灰的主要成分为碳酸钙
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表为元素周期表的一部分,表中列出10种元素在周期表中的位置,按要求回答下列问题。
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
二 | ⑥ | ⑧ | ⑩ | |||||
三 | ① | ③ | ⑤ | ⑦ | ⑨ | |||
四 | ② | ④ |
(1)在这10种元素中,化学性质最不活泼的元素是________ (写序号),得电子能力最强的原子是________ (用元素符号表示);元素⑦的最高价氧化物对应的水化物是________________ (写化学式)。
(2)元素④的离子结构示意图为________________。
(3span>)①⑧⑨三种元素单核离子半径由大到小的顺序是(用相应的离子符号表示) ________________。
(4)请写出:
(i)③的单质置换出⑥的单质的化学方程式: ________________________。
(ii)①和⑤两种元素最高价氧化物对应的水化物相互反应的化学方程式为____________________。
(iii)②和⑨两种元素最高价氧化物对应的水化物相互反应的离子方程式为____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2一氧代环戊羧酸乙酯(K)是常见医药中间体,聚酯G是常见高分子材料,它们的合成路线如下图所示:
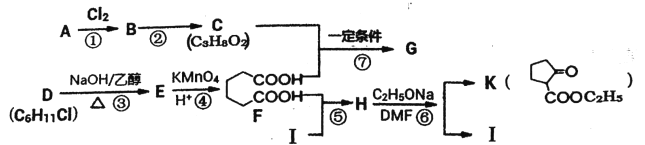
已知:①气态链烃A在标准状况下的密度为1.875g·L-1;
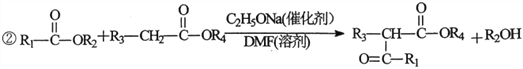
(1)B的名称为__________;E的结构简式为__________。
(2)下列有关K的说法正确的是__________。
A.易溶于水,难溶于CCl4
B.分子中五元环上碳原子均处于同一平面
C.能发生水解反应加成反应
D.1molK完全燃烧消耗9.5molO2
(3)⑥的反应类型为__________;⑦的化学方程式为__________
(4)与F官能团的种类和数目完全相同的同分异构体有__________种(不含立体结构),其中核磁共振氢谱为4组峰,且峰面积之比为1:2:3:4的是__________(写结构简式)。
(5)利用以上合成路线中的相关信息,请写出以乙醇为原料(其他无机试剂任选)制备![]()
的合成路线:__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】恒温恒容下反应:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g),能说明反应达到平衡状态的是( )
CH3OH(g)+H2O(g),能说明反应达到平衡状态的是( )
A.混合气体中H2O的体积分数保持不变
B.混合气体的密度不随时间的变化而变化
C.单位时间内消耗3 molH2,同时生成1 mol CH3OH
D.反应中CO2与CH3OH的物质的量浓度之比为1:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中国传统文化对人类文明贡献巨大,古代文献中记载了古代化学研究成果。下列叙述不正确的是
A.![]() 本草纲目
本草纲目![]() 中有“冬月灶中所烧薪柴之灰,令人以灰淋汁,取碱浣衣”的记载,“浣衣”过程中涉及水解反应
中有“冬月灶中所烧薪柴之灰,令人以灰淋汁,取碱浣衣”的记载,“浣衣”过程中涉及水解反应
B.![]() 本草衍义
本草衍义![]() 中对精制砒霜过程有如下叙述:“取砒之法,将生砒就置火上,以器覆之,令砒烟上飞着覆器,遂凝结累然下垂如乳,尖长者为胜,平短者次之。”文中涉及的操作方法是干馏
中对精制砒霜过程有如下叙述:“取砒之法,将生砒就置火上,以器覆之,令砒烟上飞着覆器,遂凝结累然下垂如乳,尖长者为胜,平短者次之。”文中涉及的操作方法是干馏
C.![]() 梦溪笔谈
梦溪笔谈![]() 中对宝剑的记载:“古人以剂钢为刃,柔铁为茎干,不尔则多断折”,“剂钢”指的是铁合金,硬度比纯铁大
中对宝剑的记载:“古人以剂钢为刃,柔铁为茎干,不尔则多断折”,“剂钢”指的是铁合金,硬度比纯铁大
D.![]() 淮南万毕术
淮南万毕术![]() 对湿法冶金术的记载:“曾青得铁则化为铜”,文中涉及置换反应
对湿法冶金术的记载:“曾青得铁则化为铜”,文中涉及置换反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)石油和煤是重要的能源物质,下列说法错误的是___。
a.石油和煤是不可再生能源
b.煤为混合物,含有苯、甲苯、二甲苯等有机物
c.煤的干馏和石油的分馏都是物理变化
d.煤燃烧及汽车尾气是造成空气污染的重要原因
e.以煤、石油为原料可生产塑料、合成橡胶、合成纤维等合成材料
(2)以煤为原料经过一系列反应可生产乙酸乙酯,其合成路线如下:
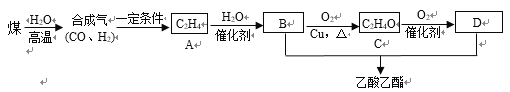
①C的名称是______;A→B的反应类型是_______。
②决定化合物B性质的基团名称是_________。
③B→C的化学方程式为_______________________________。
B+D→乙酸乙酯的化学方程式为________________________________。
(3)某化学实验小组的同学,采用如图装置制取乙酸乙酯。

①仪器B的名称是_______;仪器A中冷却水的进口是_____(填“a”或“b”)。
②观察仪器A的内层结构,与长直导管相比较,该反应装置的优点是_______。
③将乙醇和乙酸按照物质的量3∶2混合得到258g混合液,在浓硫酸作用下发生反应,乙酸乙酯的产率为50%,则生成的乙酸乙酯的质量是_______g。(相对分子质量:乙醇—46,乙酸—60,乙酸乙酯—88)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以煤为主要原料可以制备乙二醇,相关工艺流程如下:
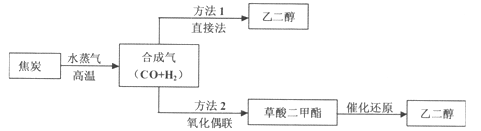
(1)写出方法l在催化剂的条件下直接制取乙二醇的化学方程式_______
(2)合成气在不同催化剂作用下,可以合成不同的物质。下列物质仅用合成气为原料就能得到且原子利用率为100%的是_____填字母)。
A.草酸( HOOC-COOH) B.甲醇(CH3OH) C.尿素[CO(NH2)2]
(3)工业上还可以利用天然气(主要成份为CH4)与C02反应制备合成气。已知:
CH4(g)+2O2(g)=CO2(g)+2H2O(l) △H=-890.3kJ/mol
2H2(g)+ O2(g)= 2H2O(l) △H=-571.6kJ/mol
2CO(g)+O2(g)=2CO2(g) △H=-566.0kJ/mol
则CH4与CO2生成合成气的热化学方程式为____________________。
(4)方法2:在恒容密闭容器中投入草酸二甲酯和H2发生如下反应:
CH3OOC—COOCH3(g)+ 4H2(g)![]() HOCH2CH2OH(g)+2CH3OH(g)△H=-34kJ/mol
HOCH2CH2OH(g)+2CH3OH(g)△H=-34kJ/mol
为提高乙二醇的产量和速率,宜采用的措施是___________(填字母)。
A.升高温度 B.增大压强 C.增大氢气浓度
(5)草酸二甲酯水解生成草酸:CH3OOC—COOCH3+ 2H2O![]() HOOC—COOH+2CH3OH
HOOC—COOH+2CH3OH
①草酸是二元弱酸,可以制备![]() (草酸氢钾),
(草酸氢钾),![]() 溶液呈酸性,用化学平衡原理解释:__________________。
溶液呈酸性,用化学平衡原理解释:__________________。
②在一定的![]() 溶液中滴加NaOH溶液至中性。下列关系一定不正确的是_______(填字母)。
溶液中滴加NaOH溶液至中性。下列关系一定不正确的是_______(填字母)。
A.![]()
B.![]()
C.![]()
(6)乙二醇、空气在KOH溶液中构成燃料电池,加入乙二醇的电极为电源的_____填“正”或“负”)极,负极反应式为_______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com