硫酸亚锡(SnSO
4)是一种重要的硫酸盐,广泛应用于镀锡工业.某研究小组设计SnSO
4制备路线如下:
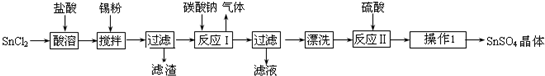
查阅资料:
Ⅰ.酸性条件下,锡在水溶液中有Sn
2+、Sn
4+两种主要存在形式,Sn
2+易被氧化.
Ⅱ.SnCl
2易水解生成碱式氯化亚锡
回答下列问题:
(1)锡原子的核电荷数为50,与碳元素属于同一主族,锡元素在周期表中的位置是
.
(2)操作Ⅰ是
.
(3)SnCl
2粉末需加浓盐酸进行溶解,请用平衡移动原理解释原因
.
(4)加入Sn粉的作用有两个:①调节溶液pH ②
.
(5)反应Ⅰ得到沉淀是SnO,得到该沉淀的离子反应方程式是
.
(6)酸性条件下,SnSO
4还可以用作双氧水去除剂,发生反应的离子方程式是
.
(7)该小组通过下列方法测定所用锡粉的纯度(杂质不参与反应):
①将试样溶于盐酸中,发生的反应为:Sn+2HCl═SnCl
2+H
2↑;
②加入过量的FeCl
3;
③用已知浓度的K
2Cr
2O
7滴定生成的Fe
2+,发生的反应为:6FeCl
2+K
2Cr
2O
7+14HCl═6FeCl
3+2KCl+2CrCl
3+7H
2O
取1.226g 锡粉,经上述各步反应后,共用去0.100mol/L K
2Cr
2O
7溶液32.0mL.锡粉中锡的质量分数是
.




 全能测控期末小状元系列答案
全能测控期末小状元系列答案 A、B、C、D、E、F六种物质的相互转化关系如图所示(反应条件均未列出).
A、B、C、D、E、F六种物质的相互转化关系如图所示(反应条件均未列出).

 氮元素可形成卤化物、氮化物、叠氮化物及配合物等许多化合物.
氮元素可形成卤化物、氮化物、叠氮化物及配合物等许多化合物.