
【题目】氧化还原滴定实验与中和滴定实验类似,现用0.1000mol/L的酸性高锰酸钾溶液滴定未
知浓度的无色亚硫酸氢钠溶液,回答下列问题:
(1)滴定前润洗滴定管的操作方法__________。
(2)某同学测得的实验数据如下表
1 | 2 | 3 | 4 | |
亚硫酸氢钠溶液体积mL | 25.00 | 25.00 | 25.00 | 25.00 |
滴定管初体积mL | 0.00 | 1.02 | 1.00 | 0.80 |
滴定管末体积mL | 40.02 | 41.00 | 41.00 | 42.90 |
求待测液亚硫酸氢钠的物质的量浓度________。
(3)滴定前平视高锰酸钾液面,达滴定终点后仰视液面,则计算值比实际值___(填“偏高”或“偏低”或“不变”) 。
(4)常温下0.1000mol/L亚硫酸溶液中H2SO3 HSO3- SO32-三者所占物质的量分数(a)随pH变化的关系如图所示,已知lg2=0.3,则原亚硫酸氢钠溶液的pH=_______:
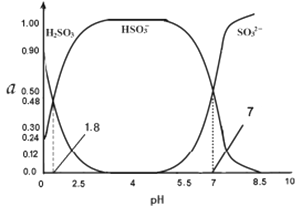
(5)取上述亚硫酸氢钠溶液1L,先加入氢氧化钠固体,使溶液的pH=10,(假定加固体后溶液的体积不变),则该溶液能溶解硫酸钡的物质的量n=______(已知该温度时KSp(BaSO4)=1.0×10-10 KSp(BaSO3)=1.0×10-8 )。
【答案】 从滴定管上口加入少量标准液(或待测液),倾斜着转动滴定管,使液体湿润内壁,然后从下部放出,重复2-3次 0.400mol/L 偏高 3.7 4×10-3
【解析】(1)滴定前润洗滴定管的操作为从滴定管上口加入少量标准液(或待测液),倾斜着转动滴定管,使液体湿润内壁,然后从下部放出,重复2-3次,故答案为:从滴定管上口加入少量标准液(或待测液),倾斜着转动滴定管,使液体湿润内壁,然后从下部放出,重复2-3次;
(2)滴定过程的方程式为6H++2MnO4-+5SO32-=2Mn2++5SO42-+3H2O,四次滴定消耗的高锰酸钾的体积分别为:40.02、39.98、40.00、42.10,很明显,第四次的滴定误差较大,删除,三次滴定消耗高锰酸钾溶液的体积平均为![]() =40.00mL,待测液中亚硫酸氢钠的物质的量浓度=
=40.00mL,待测液中亚硫酸氢钠的物质的量浓度=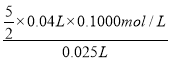 = 0.400mol/L,故答案为:0.400mol/L;
= 0.400mol/L,故答案为:0.400mol/L;
(3)滴定前平视高锰酸钾液面,达滴定终点后仰视液面,导致高锰酸钾溶液的体积偏大,则计算值比实际值偏高,故答案为:偏高;
(4)原亚硫酸氢钠的物质的量浓度= 0.400mol/L,HSO3-H++SO32-,根据图像可知,pH=7时,亚硫酸根离子与亚硫酸氢根离子浓度相等,则Ka2=10-7,则c2(H+)=0.4×10-7,解得c(H+)=![]() =2×10-4 mol/L,pH=4-0.3=3.7,故答案为:3.7;
=2×10-4 mol/L,pH=4-0.3=3.7,故答案为:3.7;
(5)取0.400mol/L亚硫酸氢钠溶液1L,先加入氢氧化钠固体,使溶液的pH=10,则反应后生成0.400mol/L的亚硫酸钠溶液,c(SO32-)=0.400mol/L,溶液中的c(Ba2+)=![]() =
=![]() =2.5×10-8,则c(SO42-)=
=2.5×10-8,则c(SO42-)=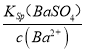 =
=![]() = 4×10-3,故答案为:4×10-3。
= 4×10-3,故答案为:4×10-3。


科目:高中化学 来源: 题型:
【题目】利用反应Cu+2FeCl3=CuCl2+2FeCl2设计成如图所示原电池,回答下列问题:
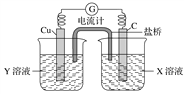
(1)写出电极反应式:正极___________________;负极_________________。
(2)图中X溶液是____________,Y溶液是____________。
(3)原电池工作时,盐桥中的________(填“阳”或“阴”)离子向X溶液方向移动。
(4)X溶液中石墨电极上发生____________(填“氧化”或“还原”)反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列行为中符合安全要求的是( )
A.进入煤矿井时,用火把照明
B.节日期间,在开阔的广场燃放烟花爆竹
C.用点燃的火柴在液化气钢瓶口检验是否漏气
D.实验时,将水倒入浓硫酸配制稀硫酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室制取、净化并收集氯气涉及以下几个主要阶段:
![]()
![]()
![]()
![]() 尾气处理
尾气处理
(1)写出实验室制取氯气的离子方程式____________________________,NA表示阿伏加德罗常数的值,若有4 mol的HCl被氧化,则转移的电子总数为______;将足量的MnO2投入含2 mol HCl的浓盐酸中,充分加热,可生成的Cl2________(填“>”“=”或“<”)0.5 mol。
(2)现有3种试剂可供选择:A.饱和食盐水 B.浓硫酸 C.NaOH溶液,则Y溶液应选用________(填字母),X溶液的作用是____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.1 mol O2的质量是32g/mol
B.阿伏伽德罗常数的准确值就是6.02×1023
C.CO2的摩尔质量是44g/mol
D.常温常压下22.4L氦气含有1 mol原子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】辣椒素是辣椒的活性成分,可在口腔中产生灼烧感,能够起到降血压和胆固醇的功效,进而在很大程度上预防心脏病,也能缓解肌肉关节疼痛。辣椒素酯类化合物的结构可以表示为:
 (R为烃基)
(R为烃基)
其中一种辣椒素酯类化合物J的合成路线如下:
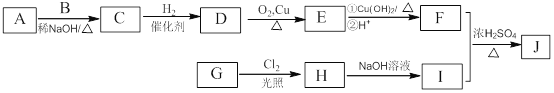
已知:
①A、B和E为同系物,其中B的相对分子质量为44,A和B核磁共振氢谱显示都有两组峰;
②化合物J的分子式为C15H22O4;
③
回答下列问题:
(1)G所含官能团的名称为 。
(2)由A和B生成C的化学方程式为 。
(3)由C生成D的反应类型为 ,D的化学名称为 。
(4)由H生成I的化学方程式为 。
(5)J的结构简式为 。
(6)G的同分异构体中,苯环上的一氯代物只有一种的共有 种(不含立体异构),核磁共振氢谱显示2组峰的是 (写结构简式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某校化学兴趣小组对以下三种品牌牙膏中摩擦剂成分进行调查,结果如下表:
牙膏品牌 | A儿童牙膏 | B防臭牙膏 | C透明牙膏 |
摩擦剂 | 氢氧化铝 | 碳酸钙 | 二氧化硅 |
(1)上述三种摩擦剂成分中属于酸性氧化物的是________(填化学式,下同);既能与强酸反应又能与强碱反应的是________。
(2)A儿童牙膏中摩擦剂成分与NaOH溶液反应的离子方程式是______________________________。
(3)从摩擦剂成分考虑,向B防臭牙膏样品中滴加少量稀盐酸,可观察到的现象是______________________________________,该反应的化学方程式为_______________________。
(4)C透明牙膏摩擦剂成分SiO2是工业制备晶体硅的原料,其反应原理是_______________(用化学反应方程式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,向一定体积0.1 mol·L-1一元弱酸HA溶液中逐滴加入等浓度的NaOH溶液,溶液中pH与pOH[pOH=-1gc(OH-)]的变化关系如图所示。 下列说法错误的是

A. 此温度下,水的离子积常数为1.0×10-2a
B. M、N两点所示的溶液中,水的电离程度相同
C. Q点消耗的NaOH溶液的体积等于HA溶液的体积
D. N点溶液加水稀释,![]() 减小
减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学实验小组的同学为探究和比较SO2和氯水的漂白性,设计了如下的实验装置。
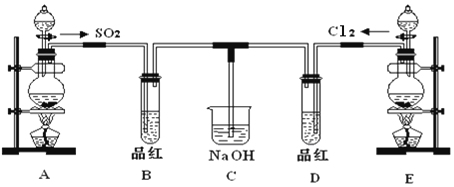
(1)实验室用装置A制备SO2。某同学在实验时发现打开A的分液漏斗活塞后,漏斗中液体未流下,你认为原因可能是__________________。
(2)实验室用装置E制备Cl2,其反应的化学方程式为__________________________;若有8mol的HCl参加反应,则转移的电子总数为________。
(3)该装置中氢氧化钠溶液的作用是___________________。
(4)通气后B、D两个试管中的现象______________。停止通气后,再给B、D两个试管分别加热,两个试管中的现象分别为B:________,D:________。
(5)另一个实验小组的同学认为SO2和氯水都有漂白性,二者混合后的漂白性肯定会更强。他们将制得的SO2和Cl2按1:1同时通入到品红溶液中,结果发现褪色效果并不像想象的那样。请你分析该现象的原因(用化学方程式表示)____________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com