
熔融盐燃料电池具有高的发电效率,因而受到重视。用Li2CO3和Na2CO3的熔融盐混合物作电解质,一极通CO气体,另一极通O2和CO2混合气体,可制得在650℃下工作的燃料电池。已知该电池总反应为:2CO+O2=2CO2。则下列说法中正确的是( )
A.通CO的一极是电池的正极,
B.该电池工作过程中需不断补充CO和O2,CO2可循环利用
C.负极反应式:O2+2CO2+4e-==2CO32-
D.该电池工作过程中有蓝色火焰产生
 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案 暑假作业安徽少年儿童出版社系列答案
暑假作业安徽少年儿童出版社系列答案科目:高中化学 来源: 题型:
化学与生产和生活密切相关,下列说法正确的是
A.金属钠可以保存在煤油或酒精中,防止在空气中变质
B.石油的裂化和煤的干馏,都属于化学变化
C.等质量的葡萄糖和果糖在人体内完全氧化释放的能量相等
D.聚氯乙烯制品易造成白色污染,可采用焚烧法处理
查看答案和解析>>
科目:高中化学 来源: 题型:
下列反应既是氧化还原反应,又是吸热反应的是
A.灼热的炭与CO2反应 B.Ba(OH)2·8H2O与NH4Cl的反应
C. 铝片与稀硫酸反应 D.甲烷在O2中的燃烧
查看答案和解析>>
科目:高中化学 来源: 题型:
依据元素周期表及元素周期律,下列推断正确的是
A.H3BO3的酸性比H2CO3的强 B.氢氧化钡的碱性比氢氧化钙的碱性强
C.硒化氢比硫化氢稳定 D.若Xm+ 和Yn- 核外电子层结构相同,则在周期表中X、Y的族序数之差一定为:(m+n)-8
查看答案和解析>>
科目:高中化学 来源: 题型:
观察下列几个装置示意图,有关叙述正确的是

A.装置①中阳极上析出红色固体 B.装置②的待镀铁制品应与电源正极相连
C.装置③中外电路电子由a极流向b极
D.装置④中的离子交换膜允许阳离子、阴离子、水分子自由通过
查看答案和解析>>
科目:高中化学 来源: 题型:
已知化合物B3N3H6(硼氮苯)与C6H6(苯)的分子结构相似,
如下图所示:则硼氮苯的二氯取代物B3N3H4Cl2的同分异
构体的数目为
A. 2 B. 3 C. 4 D. 6
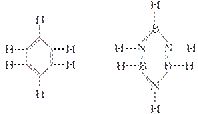
查看答案和解析>>
科目:高中化学 来源: 题型:
根据环保要求,在处理有氰电镀废水时,剧毒的CN-离子在催化剂TiO2颗粒作用下,
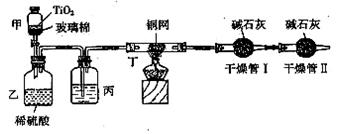
先用NaClO将CN-离子氧化成CNO-(CN-和CNO-中N元素均为-3价),再在酸性条件下继续与NaClO反应生成N2、CO2和Cl2。环保工作人员在密闭系统中用下图装置进行实验,测定
CN-被处理的百分率。
现将浓缩后含CN-离子的污水与过量NaClO溶液的混合液共200 mL(其中CN-的浓度为0.2 mol/L)倒入甲中,塞上橡皮塞,一段时间后,打开橡皮塞和活塞,使溶液全部放入乙中,关闭活塞。回答下列问题:
(1)根据题意,写出相关主要反应的离子方程式:
甲中的反应:
乙中的反应:
(2)上述实验是通过测定CO2的量来确定对CN-的处理效果。
丙装置中的试剂是 ,丁装置的目的是 ;干燥管Ⅱ的作用是 。
(3)假定上述每一个装置都充分吸收,则利用该装置测得的CN-被处理的百分率与实际值相比
__________(填“偏高”或“偏低”),简述可能的原因: 。
(4)若干燥管Ⅰ中碱石灰增重1.408 g,则该实验中测得CN-被处理的百分率为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com