
某电动汽车配载一种可充放电的锂离子电池。放电时电池的总反应为:Li1-xCoO2+ LixC6=LiCoO2+C6(x<1)。下列关于该电池的说法不正确的是( )
A.放电时,Li+在电解质中由负极向正极迁移
B.放电时,负极的电极反应式为LixC6-xe-=xLi++C6
C.充电时,若转移lmole-,石墨C6电极将增重7xg
D.充电时,阳极的电极反应式为LiCoO2-xe-= Li1-xCoO2+Li+
科目:高中化学 来源:2017届河北省高三上期中化学试卷(解析版) 题型:选择题
下列物质中不含非极性共价键的是:①Na2O2;②CCl4;③O2;④NH4Cl;⑤H2O2;⑥Ca(OH)2
A. ①②③④ B. ②④⑥ C. ④⑤⑥ D. ②③⑤
查看答案和解析>>
科目:高中化学 来源:2016-2017学年四川省高二上半期考试化学卷(解析版) 题型:填空题
已知A、B、C、D、E五种元素的原子序数依次递增,A、B、C、D位于短周期。A是原子半径最小的元素;B的基态原子中电子占据三种能量不同的原子轨道,且每种轨道中的电子总数相同;D原子的核外成对电子数是未成对电子数的3倍;E有“生物金属”之称,E4+和氩原子的核外电子排布相同。A、B、D三种元素组成的一种化合物M是新装修居室中常含有的一种有害气体,A、B两种元素组成的原子个数之比为1 : 1的化合物N是常见的有机溶剂。
请回答下列问题(答题时,A、B、C、D、E用所对应的元素符号表示):
(1)A2D2分子的电子式为____________,属于___________分子(填“极性”或“非极性”),E的基态原子的外围电子排布式为____________。
(2)B、C、D三种元素 的第一电离能由小到大的顺序为____________。
的第一电离能由小到大的顺序为____________。
(3)C元素形成含氧酸酸性强弱:HNO3____________H NO2(填“>”或“<”)NO3—的空间构型是___________,NO2—中心原子的杂化方式为___________
NO2(填“>”或“<”)NO3—的空间构型是___________,NO2—中心原子的杂化方式为___________
(4)下列叙述正确的是____________(填序号)。
A. M是极性分子,N是非极性分子
B. M和BD2分子中的中心原子均采用sp2杂化
C. N分子中含有6个σ键和1个大π键
D. BD2晶体的熔点、沸点都比二氧化硅晶体的低
(5)已知:①E的一种氧化物Q,其晶胞结构如图所示:
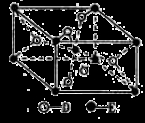
①Q(s)+2Cl2(g)=ECl4(l)+D2(g) △H=+140kJ/mol
②2B(s)+D2(g)=2BD(g) △H=-221kJ/mol
写出物质Q和焦炭、氯气反应生成液态ECl4和BD气体的热化学方程式:____________________
查看答案和解析>>
科目:高中化学 来源:2016-2017学年四川省高二上11月考试化学卷(解析版) 题型:选择题
室温下,将一元酸 HA 的溶液和 KOH 溶液等体积混合(忽略体积变化),实验数据如下表:
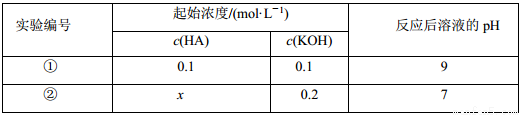
下列判断不正确的是( )
A.实验①反应后的溶液中:c(K+)>c(A-)>c(OH-)>c(H+)
B.实验①反应后的溶液中:c(OH-)=c(K+)-c(A-)=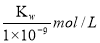
C.实验②反应后的溶液中:c(A-)+c(HA)>0.1 mol/L
D.实验②反应后的溶液中:c(K+)=c(A-)>c(OH-)=c(H+)
查看答案和解析>>
科目:高中化学 来源:2017届重庆八中高三上学期定时训练14化学试卷(解析版) 题型:填空题
化工生产的副产氢也是氢气的来源。电解法制取有广泛用途的Na2FeO4,同时获得氢气:Fe+2H2O+2OH-=FeO42-+3H2↑,工作原理如图1所示。装置通电后,铁电极附近生成紫红色的FeO42-,镍电极有气泡产生。若氢氧化钠溶液浓度过高,铁电极区会产生红褐色物质。已知:Na2FeO4只有在强碱性条件下稳定,易被H2还原。
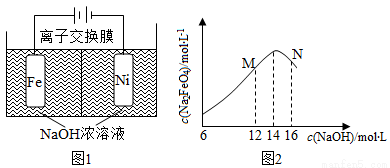
①电解一段时间后,c(OH-)降低的区域在__________(城 “阴极室”或“阳极室”)。
②电解过程中,须将阴极产生的气体及时排出,其原因是________。
③c(Na2FeO4)随初始c(NaOH)的变化如图2,任选M、N两点中的一点,分析c(Na2FeO4)低于最高值的原因:_____________。
查看答案和解析>>
科目:高中化学 来源:2017届云南省高三上第四次月考化学卷(解析版) 题型:实验题
以富含硫酸亚铁的工业废液为原料生产氧化铁的工艺如下(部分操作和条件略):
I.从废液中提纯并结晶出FeSO4·7H2O。
Ⅱ.将FeSO4·7H2O配制成溶液。
Ⅲ.FeSO4溶液与稍过量的NH4HCO3溶液混合,得到含FeCO3的浊液。
Ⅳ.将浊液过滤,用90℃热水洗涤沉淀,干燥后得到FeCO3固体。
V.煅烧FeCO3,得到Fe2O3固体。
已知:NH4HCO3在热水中分解。
(1)简述由硫酸亚铁晶体得到FeSO4·7H2O的主要操作步骤:___________________。
(2)Ⅱ中,需加一定量硫酸。同理,配制硫酸铝溶液时也需加入一定量的硫酸,请说出加入硫酸的作用,并写出相关的离子方程式:________________________。
(3)Ⅲ中,生成FeCO3的离子方程式是 ____________________。若FeCO3浊液长时间暴露在空气中,会有部分固体表面变为红褐色,该变化的化学方程式是____________________。
(4)IV中为什么用90℃热水洗涤沉淀?____________________。
(5)已知煅烧FeCO3的化学方程式是4 FeCO3+O2 2Fe2O3+4CO2。现煅烧 464.0 kg的FeCO3,得到316.8 kg产品。若产品中杂质只有FeO,则用氧气将这些FeO氧化需要标况下氧气的体积是_________L。
2Fe2O3+4CO2。现煅烧 464.0 kg的FeCO3,得到316.8 kg产品。若产品中杂质只有FeO,则用氧气将这些FeO氧化需要标况下氧气的体积是_________L。
(摩尔质量/g·mol-1:FeCO3:116g·mol-1;Fe2O3:160g·mol-1;FeO:72g·mol-1)
查看答案和解析>>
科目:高中化学 来源:2017届云南省高三上第四次月考化学卷(解析版) 题型:选择题
下列说法正确的是
A.泡沫灭火器的灭火原理是硫酸铝与苏打溶液发生反应
B.食用油反复加热会产生稠环芳烃等有害物质
C.用FeCl3腐蚀印刷电路板是因为铁的金属性强于铜
D.工业酒精浓度高于医用酒精,所以其消毒能力更强
查看答案和解析>>
科目:高中化学 来源:2017届山东省东营市高三上期中化学卷(解析版) 题型:选择题
关于电解NaCl水溶液,下列叙述正确的是( )
A.电解时在阳极得到氯气,在阴极得到金属钠
B.若在阳极附近的溶液中滴入KI试液,溶液呈棕色
C.若在阴极附近的溶液中滴入酚酞试液,溶液呈无色
D.电解一段时间后,将全部电解液转移到烧杯中,充分搅拌后溶液呈中性
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江苏省高一上期中化学卷(解析版) 题型:推断题
下图是由短周期元素组成的一些单质及其化合物之间的转化关系图。常温常压下,D、F、K均为无色无刺激性气味的气体,B是最常见的无色液体,A是由单质C在D中燃烧生成的淡黄色固体。(反应中生成的部分物质已略去)

请回答下列问题:
(1)物质A的化学式为__________。组成单质C的原子结构示意图__________。
(2)反应①的化学方程式为__________;反应②的化学方程式为__________。
(3)设计实验验证一包纯净物是H_______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com