
| A£® | ³£ĪĀĻĀ·“Ó¦2M2++Z2ØT2M3++2Z-æÉŅŌ·¢Éś | |
| B£® | ZŌŖĖŲŌŚ·“Ó¦¢ŁÖŠ±»»¹Ō£¬ŌŚ¢ŪÖŠ±»Ńõ»Æ | |
| C£® | Ńõ»ÆŠŌĒæČõĖ³ŠņĪŖ£ŗXO4-£¾Z2£¾R2£¾M3+ | |
| D£® | »¹ŌŠŌĒæČõĖ³ŠņĪŖ£ŗX2+£¼Z-£¼R-£¼M2+ |
·ÖĪö ¢Ł16H++10Z-+2XO4-ØT2X2++5Z2+8H2OÖŠ£¬ZŌŖĖŲµÄ»ÆŗĻ¼ŪÉżøߣ¬XŌŖĖŲµÄ»ÆŗĻ¼Ū½µµĶ£»
¢Ś2M2++R2ØT2M3++2R-ÖŠ£¬MŌŖĖŲµÄ»ÆŗĻ¼ŪÉżøߣ¬RŌŖĖŲµÄ»ÆŗĻ¼Ū½µµĶ£»
¢Ū2R-+Z2ØTR2+2Z-ÖŠ£¬ZŌŖĖŲµÄ»ÆŗĻ¼Ū½µµĶ£¬RŌŖĖŲµÄ»ÆŗĻ¼ŪÉżøߣ»
½įŗĻŃõ»Æ»¹Ō·“Ó¦»ł±¾øÅÄī¼°Ńõ»Æ¼ĮµÄŃõ»ÆŠŌ“óÓŚŃõ»Æ²śĪļµÄŃõ»ÆŠŌ”¢»¹Ō¼ĮµÄ»¹ŌŠŌ“óÓŚ»¹Ō²śĪļµÄ»¹ŌŠŌĄ“½ā“š£®
½ā“š ½ā£ŗA£®øł¾Ż»¹ŌŠŌĖ³Šņ£ŗZ-£¼M2+£¬³£ĪĀĻĀæÉ·¢Éś·“Ó¦2M2++Z2ØT2M3++2Z-£¬¹ŹAÕżČ·£»
B£®·“Ó¦¢Ł16H++10Z-+2XO4-=2X2++5Z2+8H2OÖŠ£¬ZŌŖĖŲ»ÆŗĻ¼ŪÉżøߣ¬±»Ńõ»Æ£¬ŌŚ·“Ó¦¢Ū2R-+Z2ØTR2+2Z-ÖŠ£¬ZŌŖĖŲ»ÆŗĻ¼Ū½µµĶ£¬±»»¹Ō£¬¹ŹB“ķĪó£»
C£®Ńõ»Æ»¹Ō·“Ó¦ÖŠŃõ»Æ¼ĮµÄŃõ»ÆŠŌĒæÓŚŃõ»Æ²śĪļµÄŃõ»ÆŠŌ£¬·“Ó¦¢Ł16H++10Z-+2XO4-=2X2++5Z2+8H2OÖŠ£¬Ńõ»ÆŠŌXO4-£¾Z2£»·“Ó¦¢Ś2M2++R2ØT2M3++2R-ÖŠ£¬Ńõ»ÆŠŌR2£¾M3+£»·“Ó¦-¢Ū2R-+Z2ØTR2+2Z-ÖŠ£¬Ńõ»ÆŠŌ£ŗZ2£¾R2£¬¼“Ńõ»ÆŠŌĖ³ŠņŹĒXO4-£¾Z2£¾R2£¾M3+£¬¹ŹCÕżČ·£»
D£®øł¾Ż·“Ó¦2M2++R2ØT2M3++2R-£¬æɵƻ¹ŌŠŌĖ³ŠņŹĒ£ŗR-£¼M2+£¬øł¾Ż·“Ó¦2R-+Z2ØTR2+2Z-£¬æɵƻ¹ŌŠŌĖ³ŠņŹĒZ-£¼R-£¬øł¾Ż·“Ó¦£ŗ16H++10Z-+2XO4-=2X2++5Z2+8H2O£¬æɵƻ¹ŌŠŌĖ³ŠņŹĒ£ŗX2+£¼Z-£¬¼“»¹ŌŠŌĒæČõĖ³ŠņĪŖ£ŗX2+£¼Z-£¼R-£¼M2+£¬¹ŹDÕżČ·£»
¹ŹŃ”B£®
µćĘĄ ±¾Ģāæ¼²éŃõ»Æ»¹Ō·“Ó¦£¬°ŃĪÕ·“Ó¦ÖŠŌŖĖŲµÄ»ÆŗĻ¼Ū±ä»ÆĪŖ½ā“šµÄ¹Ų¼ü£¬²ąÖŲŃõ»Æ»¹Ō·“Ó¦»ł±¾øÅÄī¼°Ńõ»ÆŠŌ”¢»¹ŌŠŌ±Č½ĻµÄ漲飬ĢāÄæÄŃ¶Č²»“ó£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| Ń”Ļī | ŹµŃé²Ł×÷ | ĻÖĻó | ½āŹĶ»ņ½įĀŪ |
| A | ¹żĮæµÄFe·ŪÖŠ¼ÓČėĻ”HNO3£¬³ä·Ö·“Ó¦ŗ󣬵ĪČėKSCNČÜŅŗ | ČÜŅŗ³ŹŗģÉ« | Ļ”HNO3½«FeŃõ»ÆĪŖFe3+ |
| B | Į½ŹŌ¹Üø÷¼ÓČė5ml 0.1mol/L Na2S2O3ČÜŅŗ£¬Ķ¬Ź±·Ö±šµĪČė5ml 0.1mol/LĮņĖįŗĶŃĪĖį | Į½Ö§ŹŌ¹ÜĶ¬Ź±±ä»ė×Ē | ĘäĖüĢõ¼ž²»±äŹ±£¬Cl-Ņ»¶ØÓŠ“߻Ɗ§¹ū |
| C | A1²²åČėĻ”HNO3ÖŠ | ĪŽĻÖĻó | A1²±ķĆę±»HNO3Ńõ»Æ£¬ŠĪ³ÉÖĀĆܵÄŃõ»ÆĤ |
| D | ÓĆ²£Į§°ōÕŗČ”ÅØ°±Ė®µćµ½ŗģÉ«ŹÆČļŹŌÖ½ÉĻ | ŹŌÖ½±äĄ¶É« | ÅØ°±Ė®³Ź¼īŠŌ |
| A£® | A | B£® | B | C£® | C | D£® | D |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ĀĢÉ«»ÆѧµÄŗĖŠÄŹĒŌŚ»ÆѧŗĻ³ÉÖŠ½«Ō×Ó³ä·ÖĄūÓĆ£¬×Ŗ»ÆĪŖŠĀµÄŌ×Ó | |
| B£® | ŃŠ·¢Ź¹ÓĆøߊ§“߻ƼĮ£¬æÉĢįøß·“Ó¦ÖŠŌĮĻµÄ×Ŗ»ÆĀŹ | |
| C£® | øß“æ¶ČµÄ¾§Ģ幚æÉŅŌÖʱø¾§Ģå¹ÜµČ°ėµ¼Ģ唢µēÄŌŠ¾Ę¬ | |
| D£® | ¾Ę¾«”¢NaClČÜŅŗ”¢CuSO4ČÜŅŗ”¢ÅØHNO3¶¼æÉŹ¹µ°°×ÖŹ·¢Éś±äŠŌ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| ŹµŃé | 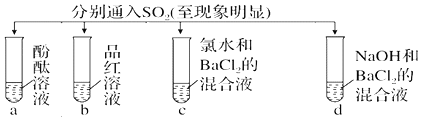 | ||||
| ĻÖĻó | A | ĪŽÉ« | ĪŽÉ« | ĪŽĻÖĻó | ĪŽÉ«ČÜŅŗ |
| B | ŗģÉ« | ĪŽÉ« | °×É«³Įµķ | °×É«³Įµķ | |
| C | ĪŽÉ« | ĪŽÉ« | ČÜŅŗ±äĪŽÉ«£¬°×É«³Įµķ | °×É«³Įµķ | |
| D | ĪŽÉ« | ĪŽÉ« | ĪŽÉ«ČÜŅŗ | ĪŽÉ«ČÜŅŗ | |
| A£® | A | B£® | B | C£® | C | D£® | D |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ŗ¬NAøöNa+µÄNa2OČܽāÓŚ1 LĖ®ÖŠ£¬Na+µÄĪļÖŹµÄĮæÅضČĪŖ1 mol•L-1 | |
| B£® | ³£ĪĀ³£Ń¹ĻĀ£¬5.6gŅŅĻ©Óė¶”Ļ©£ØC4H8£©µÄ»ģŗĻĪļÖŠĒāŌ×ÓŹżĪŖ0.8NA | |
| C£® | ±ź×¼×“æöĻĀ£¬4.48 LCl2Óė×ćĮæµÄFe·“Ó¦×ŖŅʵē×ÓŹżĪŖ0.4NA | |
| D£® | 0.1 mol H218OÓėD2OµÄ»ģŗĻĪļÖŠÖŠ×ÓŹżĪŖNA |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ŌŚ³£ĪĀ³£Ń¹ĻĀ£¬2.24L NH3Óė1.8g H2O£¬Ėłŗ¬µÄÖŹ×ÓŹż¾łĪŖNA | |
| B£® | ŌŚ³£ĪĀ³£Ń¹ĻĀ£¬1mol Cl2Óė×ćĮæµÄNaOHČÜŅŗĶźČ«·“Ó¦£¬×ŖŅʵē×Ó2NA | |
| C£® | ŌŚ±ź×¼×“æöĻĀ£¬64g SO2 ÖŠŗ¬ÓŠµÄŌ×ÓŹżĪŖ3NA | |
| D£® | ŌŚ±ź×¼×“æöĻĀ£¬11.2L H2Oŗ¬ÓŠµÄ·Ö×ÓŹżĪŖ0.5NA |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
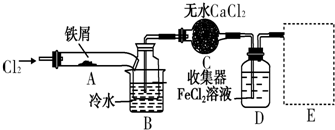
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | øß“æ¶ČµÄ¶žŃõ»Æ¹čæÉÓĆÓŚÖĘŌģ¼ĘĖ滜Š¾Ę¬ŗĶĢ«ŃōÄܵē³Ų | |
| B£® | ½ŗĢåŗĶČÜŅŗæÉŅŌĶعżĀĖÖ½½ųŠŠ·ÖĄė | |
| C£® | ĪķŹĒĘųČܽŗ£¬ŌŚŃō¹āĻĀæɹŪ²ģµ½¶”“ļ¶ūŠ§Ó¦ | |
| D£® | ²£Į§ŹĒŃõ»ÆĪļ£¬³É·ÖæɱķŹ¾ĪŖNa2O•CaO•6SiO2 |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com