
| A�� | ��ƽ��ʱ��O2��ʾ�ķ�Ӧ����Ϊ0.25 mol•L-1•min-1 | |
| B�� | �ڶ��δ�ƽ��ʱSO3�������������$\frac{2}{9}$ | |
| C�� | ��һ��ƽ��ʱ��Ӧ�ų�������Ϊ294.9 kJ | |
| D�� | ����ƽ��SO2��ת������� |
���� A�����º����£�ѹǿ֮�ȵ������ʵ���֮�ȣ���ƽ��ʱ������������ʵ���Ϊ��3mol+2mol����90%=4.5mol����
2SO2��g��+O2��g��?2SO3��g����n=1
��ʼ����mol����3 2 0
�仯����mol����1 0.5 1 5-4.5=0.5
ƽ������mol����2 1.5 1
�ٸ���v=$\frac{��c}{��t}$����v��O2����
B����ЧΪ��ʼ����6mol SO2��4mol O2����һ����Ч��ԭƽ��Ļ���������ѹǿ��ƽ�������ƶ�����ƽ��ʱSO3������������ڵ�һ��ƽ�⣻
C����һ��ƽ��ʱ�μӷ�Ӧ�Ķ�������Ϊ1mol������Ȼ�ѧ����ʽ���㣻
D����ЧΪ��ʼ����6mol SO2��4mol O2����һ����Ч��ԭƽ��Ļ���������ѹǿ��ƽ�������ƶ���
��� �⣺A�������ݻ�δ֪������ƽ��ʱ��δ֪�����ܼ��㷴Ӧ���ʣ���A����
B�����º����£�ѹǿ֮�ȵ������ʵ���֮�ȣ���ƽ��ʱ������������ʵ���Ϊ��3mol+2mol����90%=4.5mol����
2SO2��g��+O2��g��?2SO3��g����n=1
��ʼ����mol����3 2 0
�仯����mol����1 0.5 1 5-4.5=0.5
ƽ������mol����2 1.5 1
��һ��ƽ��ʱSO3���������=$\frac{1mol}{4.5mol}$=$\frac{2}{9}$������ʼ���ʵ�����Ϊ4mol SO2��3mol O2��2mol SO3��g������ЧΪ��ʼ����6mol SO2��4mol O2����һ����Ч��ԭƽ��Ļ���������ѹǿ��ƽ�������ƶ�����ƽ��ʱSO3������������ڵ�һ��ƽ�⣬���ڶ��δ�ƽ��ʱSO3�������������$\frac{2}{9}$����B��ȷ��
C����һ��ƽ��ʱ�μӷ�Ӧ�Ķ�������Ϊ1mol�����һ��ƽ��ʱ��Ӧ�ų�������Ϊ196.6kJ��$\frac{1mol}{2mol}$=98.3 kJ����C����
D����ЧΪ��ʼ����6mol SO2��4mol O2����һ����Ч��ԭƽ��Ļ���������ѹǿ��ƽ�������ƶ����ڶ���ƽ��ʱSO2��ת���ʴ��ڵ�һ�Σ���D����
��ѡ��B��
���� ���⿼�黯ѧƽ����㣬Bѡ��ע�����õ�Ч˼���𣬹ؼ��ǹ���ƽ�⽨����;�����Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
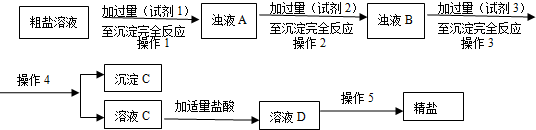
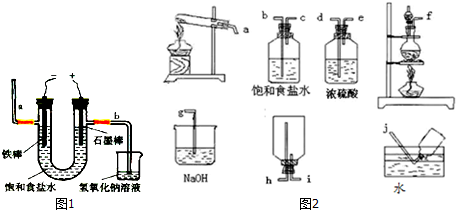
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
 ��Ϊ���ִ��л��ϳ�֮����������ֵ�����֯14�����ҵ�110λ��ѧ�ң�Эͬ���أ�̽��ά����B12�Ľṹ����ṹ��ͼ�Դ˽ṹ������˵���У���ȷ���ǣ�������
��Ϊ���ִ��л��ϳ�֮����������ֵ�����֯14�����ҵ�110λ��ѧ�ң�Эͬ���أ�̽��ά����B12�Ľṹ����ṹ��ͼ�Դ˽ṹ������˵���У���ȷ���ǣ�������| A�� | ά����B12�����л��� | B�� | ά����B12�������� | ||
| C�� | ά����B12������ | D�� | ά����B12���ڷ����廯���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ʵ����� | �� | �� | �� |
| �Ͻ�����/mg | 255 | 385 | 459 |
| �����������/mL | 280 | 336 | 336 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Fe������Ϊ2.7g��Al������Ϊ2.8g | B�� | Fe������Ϊ2.8g��Al������Ϊ2.7g | ||
| C�� | Fe������Ϊ5.4g��Al������Ϊ5.6g | D�� | Fe������Ϊ5.6g��Al������Ϊ5.4g |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ����β���е���Ҫ��Ⱦ����NO�Լ�ȼ�ϲ���ȫȼ����������CO��Ϊ�˼��������Ⱦ���������ͨ�����·�Ӧ����������β����
����β���е���Ҫ��Ⱦ����NO�Լ�ȼ�ϲ���ȫȼ����������CO��Ϊ�˼��������Ⱦ���������ͨ�����·�Ӧ����������β����| ʱ��/s | 0 | 1 | 2 | 3 | 4 | 5 |
| c��NO��/��10-4 mol•L-1 | 10.0 | 4.50 | 2.50 | 1.50 | 1.00 | 1.00 |
| c��CO��/��10-3 mol•L-1 | 3.60 | 3.05 | 2.85 | 2.75 | 2.70 | 2.70 |
| ʵ���� | T/�� | NO��ʼŨ��/mol•L-1 | CO��ʼŨ��/mol•L-1 | �����ıȱ����/m2•g-1 |
| �� | 350 | 1.20��10-3 | 5.80��10-3 | 124 |
| �� | 280 | 1.20��10-3 | 5.80��10-3 | 124 |
| �� | 280 | 1.20��10-3 | 5.80��10-3 | 82 |
| NO | N2 | CO2 | |
| ��ʼŨ��/mol•L-1 | 0.10 | 0 | 0 |
| ƽ��Ũ��/mol•L-1 | 0.04 | 0.03 | 0.03 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
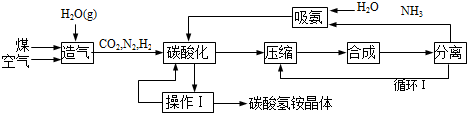

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ˮ | B�� | ʯ���� | C�� | ������������ | D�� | ţ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com