
| A. | C(s)+$\frac{1}{2}$O2(g)=CO(g)△H=-110.5 kJ/mol | |
| B. | H2(g)+Cl2(g)=2HCl(g)△H=-184.6 kJ/mol | |
| C. | H2(g)+$\frac{1}{2}$O2(g)=H2O(g)△H=-241.8 kJ/mol | |
| D. | C8H18(l)+$\frac{25}{2}$O2(g)=8CO2(g)+9H2O(l)△H=-5518 kJ/mol |
分析 在25℃,101 kPa时,1 mol可燃物完全燃烧生成稳定的化合物时所放出的热量,叫做该物质的燃烧热据此解答.
解答 解:A、根据燃烧热的含义,必须是1mol物质完全燃烧生成最稳定的产物放出的热量,应该是生成二氧化碳,不能是生成一氧化碳,故A错误;
B、燃烧热是指完全燃烧1mol物质生成稳定产物所放出的热量,该反应不是物质在氧气中的燃烧反应,故B错误;
C、根据燃烧热的含义,必须是1mol物质完全燃烧生成最稳定的产物放出的热量,该反应应该是生成液态水,不能是气态水,故C错误;
D、该热化学方程式符合燃烧热的含义:25℃,101 kPa时,1 mol庚烷完全燃烧生成稳定的化合物时所放出的热量,故D正确.
故选D.
点评 本题考查学生燃烧热的概念以及热化学方程式的书写知识,注意概念的理解和应用是解题的关键,难度中等.


科目:高中化学 来源: 题型:选择题
| A. | CS2的比例模型: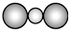 | |
| B. | H2O2的电子式: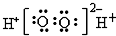 | |
| C. | 氯离子(Cl-)的结构示意图: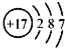 | |
| D. | 基态镁原子的电子排布图:1s22s22p63s2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 适当加热新制的氯水时,溶液的pH逐渐减小 | |
| B. | 加催化剂,使N2和H2在一定条件下转化为NH3 | |
| C. | 可用浓氨水和氢氧化钠固体快速制取氨气 | |
| D. | 增大压强,有利于SO2与O2反应生成SO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 11.2 g | B. | 5.6 g | C. | 2.8 g | D. | 1.4 g |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 (PAN)等二次污染物.
(PAN)等二次污染物.查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com