



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
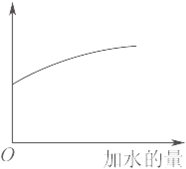
| A£®CO32-Ė®½āµÄĘ½ŗā³£Źż | B£®ČÜŅŗµÄpH |
| C£®ČÜŅŗÖŠHCO3-Ąė×ÓŹż | D£®ČÜŅŗÖŠc£ØCO32-£© |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®ČÜŅŗÖŠĢ¼ĖįĒāøłµēĄėµÄĒāĄė×ÓÅضČĪŖ10-10mol?L-1 |
| B£®c£ØNa+£©£¾c£ØOH-£©£¾c£ØHCO3-£©£¾c£ØH+£© |
| C£®ČÜŅŗÖŠĖ®µēĄėµÄĒāŃõøłĄė×ÓÅضČĪŖ10-4mol?L-1 |
| D£®c£ØNa+£©+c£ØH+£©=c£ØHCO3-£©+c£ØOH-£© |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
A£®CH2=CH2+HCl
| |||
B£®CH4+Cl2
| |||
C£® +Br2 +Br2
 +HBr +HBr | |||
D£®CH3CH2Br+NaOH
|
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®ČÜŅŗ³ŹÖŠŠŌµÄŃĪŅ»¶ØŹĒĒæĖįÓėĒæ¼īÉś³ÉµÄŃĪ |
| B£®ŗ¬ÓŠČõĖįøłĄė×ÓµÄŃĪµÄĖ®ČÜŅŗŅ»¶Ø³Ź¼īŠŌ |
| C£®ŃĪČÜŅŗµÄĖį¼īŠŌÖ÷ŅŖ¾ö¶ØÓŚŠĪ³ÉŃĪµÄĖį”¢¼īµēĄė³Ģ¶ČµÄĻą¶Ō“óŠ” |
| D£®Na2SĖ®½āµÄĄė×Ó·½³ĢŹ½ĪŖ£ŗS2-+2H2O?H2S+2OH- |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®ĪŽ·ØČ·¶Ø | B£®0.09% | C£®1.0% | D£®0.01% |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗĪŹ“šĢā
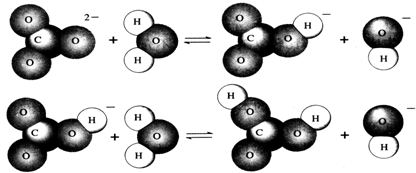
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗĢīæÕĢā
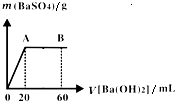
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®NaHCO3 | B£®£ØNH4£©2SO4 | C£®NaCl | D£®CH3COOK |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com