
下列图示与对应的叙述相符的是()
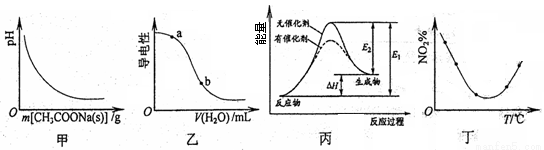
A.图甲表示向CH3COOH溶液中逐步加入CH3COONa固体后,溶液pH的变化
B.图乙表示向CH3COOH溶液中加水时溶液的导电性变化,则CH3COOH溶液的pH:a>b
C.图丙表示催化剂能改变化学反应的焓变
D.图丁表示等量NO2在容积相同的恒容密闭容器中,不同温度下分别发生反应:2NO2(g) N2O4(g),相同时间后测得NO2含量的曲线,则该反应的△H<0
N2O4(g),相同时间后测得NO2含量的曲线,则该反应的△H<0
D
【解析】
试题分析:A.CH3COOH是弱酸,在溶液中存在电离平衡,若向CH3COOH溶液中逐步加入CH3COONa固体,则增大生成物的浓度,电离平衡逆向移动,溶液中c(H+)减小后,溶液pH比原来大,错误;B.向CH3COOH溶液中加水时醋酸的电离平衡正向移动,但是由于稀释作用使离子浓度减小的趋势大于平衡移动使离子浓度增大的趋势,所以溶液的导电性逐渐减弱,由于加水b>a,所以CH3COOH溶液的离子浓度a>b,所以pH:a<b,错误;C.图丙表示催化剂能改变化学反应的活化能,但是不能改变反应的焓变,错误;D.当反应达到平衡后,升高温度,NO2的含量逐渐增加,根据平衡移动原理可知:生成O2的方向是吸热反应,所以反应:2NO2(g) N2O4(g)的正反应是放热反应,所以△H<0,正确。
N2O4(g)的正反应是放热反应,所以△H<0,正确。
考点:考查图像法在物质的电离和化学反应速率及化学平衡中的应用的知识。


 同步练习强化拓展系列答案
同步练习强化拓展系列答案科目:高中化学 来源:2015届江苏省无锡江阴市高二下学期期中考试化学试卷(解析版) 题型:填空题
按下图所示装置进行实验,并回答下列问题:
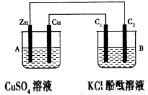
(1)判断装置的名称:A池为 ,B池为 。
(2)锌极为 极,电极反应式为 ;铜极为 极,电极反应式为 ;石墨棒C1为 极,电极反应式为 ;石墨棒C2附近发生的实验现象为 ,反应结束后,B池溶液的pH值 。(增大、减小、不变,忽略气体溶于水) 。
(3)当C2极析出224 mL气体(标准状况下),锌的质量 (增加或减少) g。
查看答案和解析>>
科目:高中化学 来源:2015届江苏省高三上学期摸底考试化学试卷(解析版) 题型:填空题
(18分) A、B、C、D、E、F是周期表中的前20号元素,原子序数逐渐增大。A元素是宇宙中含量最丰富的元素,其原子的原子核内可能没有中子。B的基态原子中电子占据三种能量不同的原子轨道,且每种轨道中的电子总数相等;C元素原子最外层p能级比s能级多1个电子;D原子p轨道上成对电子数等于未成对电子数;E的常见化合价为+3;F最高正价与最低负价的代数和为4;G+的M层电子全充满。用化学式或化学符号回答下列问题:
(1) G的基态原子的外围电子排布式为_____________________________________,在周期表中属于________区。
(2) B与F形成的一种非极性分子的电子式为_________________________;F的一种具有强还原性的氧化物分子的VSEPR模型为___________。
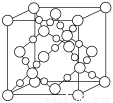
(3) BD2在高温高压下所形成的晶胞如下图所示。该晶体的类型属于______(选填“分子”、“原子”、“离子”或“金属”)晶体。
(4) 设C元素的气态氢化物为甲,最高价氧化物的水化物为乙,甲与乙反应的产物为丙。常温下,有以下3种溶液:①pH=11的甲的水溶液 ②pH=3的乙的水溶液
③pH=3的丙溶液,3种溶液中水电离出的c(H+)之比为________________。
(5) 丁、戊分别是E、F两种元素最高价含氧酸的钠盐,丁、戊溶液能发生反应。当丁、戊溶液以物质的量之比为1∶4混合后,溶液中各离子浓度大小顺序为________。
(6) A和C形成的某种氯化物CA2Cl可作杀菌剂,其原理为CA2Cl遇水反应生成一种具有强氧化性的含氧酸,写出CA2Cl与水反应的化学方程式:____________________。
(7) 往G的硫酸盐溶液中加入过量氨水,可生成一种配合物X,下列说法正确的是__。
A.X中所含化学键有离子键、极性键和配位键
B.X中G2+给出孤对电子,NH3提供空轨道
C.组成X的元素中第一电离能最大的是氧元素
D.SO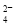 与PO
与PO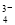 互为等电子体,空间构型均为正四面体
互为等电子体,空间构型均为正四面体
查看答案和解析>>
科目:高中化学 来源:2015届江苏省南京市高三9月学情调研卷化学试卷(解析版) 题型:实验题
[实验化学]苯亚甲基苯乙酮俗称查尔酮,淡黄色梭状晶体,熔点58℃,沸点208℃(3.3kp),易溶于醚、氯仿和苯,微溶于醇。制备原理如下:
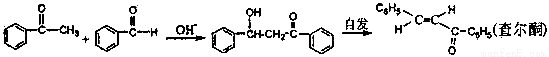

(1)制备过程中。需在搅拌下滴加苯甲酸,并控制滴加速度使反应温度维持在25~30℃,说明该反应是(填“放热”或“吸热”)反应。如温度过高时,则可采用 措施。
(2)产品结晶前,可以加入几粒成品的查尔酮,其作用是。
(3)结晶完全后,需抽滤收集产物。’抽滤装置所包含的仪器除减压系统外还有、(填仪器名称)。
(4)获得的深色粗产品加入活性炭,用95%乙醇重结晶即得查尔酮晶体,可通过法来判断原料是否反应完全以及反应的转化率和选择性。
查看答案和解析>>
科目:高中化学 来源:2015届江苏省南京市高三9月学情调研卷化学试卷(解析版) 题型:选择题
有人曾建议用AG表示溶液的酸度,AG的定义为:AG=lg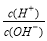 ,室温下实验室用0.01 mol·L-1的氢氧化钠溶液滴定20 mL相同浓度的醋酸溶液,滴定曲线如右图所示。下列有关叙述正确的是( )
,室温下实验室用0.01 mol·L-1的氢氧化钠溶液滴定20 mL相同浓度的醋酸溶液,滴定曲线如右图所示。下列有关叙述正确的是( )

A.A点时加入氢氧化钠溶液体积为20 mL
B.室温时0.01 mol·L-1的醋酸溶液pH=4
C.OA段溶液中:c(CH3COO-)> c(CH3COOH)
D.若B点时加入NaOH溶液40 mL,所得溶液中:c(CH3COO-)+2 c(CH3COOH) = c(OH-) - c(H+)
查看答案和解析>>
科目:高中化学 来源:2015届江苏省南京市高三9月学情调研卷化学试卷(解析版) 题型:选择题
下列关于物质性质与应用的说法正确的是()
A.碳具有还原性,高温条件下能将二氧化硅还原为硅
B.二氧化硫有漂白、杀菌性能,可在食品加工中大量使用
C.二氧化硅是半导体材料,可将太阳能直接转化为电能
D.二氧化锰具有较强的的氧化性,可作H2O2分解的氧化剂
查看答案和解析>>
科目:高中化学 来源:2015届广西桂林市高三上学期第一次月考化学试卷(解析版) 题型:实验题
(11分)实验室需要配制0.55mol·L-1 NaOH溶液220 mL。
按下列操作步骤填上适当的文字,以使整个操作完整。
(1) 选择仪器。完成本实验所必需的仪器有:托盘天平、药匙、烧杯、玻璃棒、______ ___ ____、__________________ 。
(2) 计算。配制该溶液需取NaOH晶体________g。
(3) 称量。
① 天平调平后,应将天平的游码调至某个位置,请在下图中用一根竖线标出游码左边缘所处的位置:
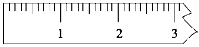
② 称量过程中NaOH晶体应放于天平的__________(填“左盘”或“右盘”)。
(4) 溶解、冷却,该步实验中需要使用玻璃棒,目的是______________________________。
(5) 转移、洗涤。在转移时应使用玻璃棒引流,应注意______
;需要洗涤烧杯2~3次是为了________________________________________________________________________。
(6)定容、摇匀。
(7)将配好的溶液静置一段时间后,倒入指定的试剂瓶,贴好标签,注明溶液名称、浓度及配制的时间。
(8)下列操作使所配溶液浓度偏大的有______________(填字母,下同);偏小的有_____________;
无影响的有_____________。
A 称量时用生锈的砝码 B 将NaOH放在纸上称量
C NaOH在烧杯中溶解后,未冷却就立即转移到容量瓶中 D 往容量瓶转移时有少量液体溅出
E、未洗涤溶解NaOH的烧杯 F、定容时仰视刻度线
G、容量瓶未干燥就用来配制溶液
查看答案和解析>>
科目:高中化学 来源:2015届广东肇庆中学高三8月考理综化学试卷(解析版) 题型:实验题
(16分)氨水是一种的常用的化学试剂。
(1)以浓氨水和生石灰为原料,用如下装置为发生装置,可制取少量氨气。已知:NH3·H2O+CaO=Ca(OH)2+NH3↑。
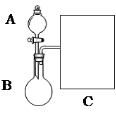
①生石灰应该装在____(填A或B)。
②试从电离平衡角度分析该实验中氨气逸出的原因:
③现要用试管和必要实验用品收集一试管氨气,请在C处补充相应收集装置。
(2)化学兴趣小组用氨水与硝酸银溶液配制好银氨溶液后,进行乙醛的银镜反应实验,但部分同学实验时间长,且效果不明显。影响乙醛银镜反应速率的因素有哪些呢?请你完成如下猜想:
①猜想:因素一:银氨溶液的pH大小;
因素二:____________________ 。
②你设计实验验证上述影响因素一,完成下表中内容。
提供试剂:乙醛、2%稀氨水、 0.25mol/L NaOH溶液、盐酸 、 2% AgNO3溶液
实验用品:烧杯(装有热水)、试管
实验步骤 | 实验操作 | 预期现象及结论(步骤1只填现象) |
1 | 在A、B两支洁净的试管中各入1mL 2%的AgNO3溶液,然后边振荡试管边逐滴滴入2%稀氨水,至最初产生的沉淀恰好完全溶解,此时制得pH均约为8的银氨溶液。 |
|
2 |
|
|
(3)吸取20.00ml 上述氨水于锥形瓶,滴加3滴甲基橙指示剂,用0.0050mol/L标准硫酸滴定,滴定至出现红色为终点,重复3次实验,平均消耗标准硫酸20.04 ml,计算上述氨水的物质的量浓度
查看答案和解析>>
科目:高中化学 来源:2015届广东省深圳市高三上学期第一次五校联考理综化学试卷(解析版) 题型:选择题
下列叙述Ⅰ和Ⅱ均正确并且有因果关系的是
编号 | 叙述I | 叙述II |
A | MgO和Al2O3的熔点都很高 | Mg(OH)2和Al(OH)3可以作阻燃剂 |
B | SO2具有漂白性 | SO2能使高锰酸钾酸性溶液褪色 |
C | AlCl3的熔融态不导电 | AlCl3是共价化合物 |
D | 硬铝是合金 | 其熔点比金属铝的熔点高 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com