
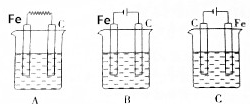
分析 (1)金属腐蚀快慢顺序是:作电解池阳极>作原电池负极>化学腐蚀>作原电池正极>作电解池阴极;
(2)Fe电极的质量过一段时间减少最快的应该是Fe作电解池阳极;
(3)Fe电极不会被腐蚀的作原电池正极或电解池阴极;
(4)A装置中Fe作负极、C作正极,负极上Fe失电子发生氧化反应、正极上氧气得电子发生还原反应;
B装置中C作阳极、Fe作阴极,阳极上氯离子放电、阴极上氢离子放电;
C装置中Fe作阳极、C作阴极,阳极上Fe失电子发生氧化反应、C电极上氢离子放电生成氢气;
(5)A装置中发生铁的吸氧腐蚀,Fe、氧气和水反应生成氢氧化铁;
B装置中电解饱和食盐水,生成氯气、氢气和NaOH.
解答 解:(1)金属腐蚀快慢顺序是:作电解池阳极>作原电池负极>化学腐蚀>作原电池正极>作电解池阴极,根据图知,金属腐蚀快慢顺序是:C>A>B,所以反应最缓慢的是B,故答案为:B;
(2)Fe电极的质量过一段时间减少最快的应该是Fe作电解池阳极,所以Fe电极质量减少最快的是C,故答案:C;
(3)Fe电极不会被腐蚀的作原电池正极或电解池阴极,B中Fe作阴极,不被腐蚀,故答案为:B;
(4)A装置中Fe作负极、C作正极,负极上Fe失电子发生氧化反应、正极上氧气得电子发生还原反应,电极反应式为Fe-2e-=Fe2+、O2+4e-+2H2O=4OH-;
B装置中C作阳极、Fe作阴极,阳极上氯离子放电、阴极上氢离子放电,电极反应式为 2Cl--2e-=Cl2↑、2H2O+2e-=2OH-+H2↑;
C装置中Fe作阳极、C作阴极,阳极上Fe失电子发生氧化反应、C电极上氢离子放电生成氢气,电极反应式为Fe-2e-=Fe2+ 2H2O+2e-=2OH-+H2↑,
故答案为:Fe-2e-=Fe2+;O2+4e-+2H2O=4OH-; 2Cl--2e-=Cl2↑;2H2O+2e-=2OH-+H2↑;Fe-2e-=Fe2+;2H2O+2e-=2OH-+H2↑;
(5)A装置中发生铁的吸氧腐蚀,Fe、氧气和水反应生成氢氧化铁,电池反应式为2Fe+O2+2H2O=2Fe(OH)2↓;
B装置中电解饱和食盐水,生成氯气、氢气和NaOH,电池反应式为 2NaCl+2H2O$\frac{\underline{\;电解\;}}{\;}$Cl2↑+H2↑+2NaOH,
故答案为:2Fe+O2+2H2O=2Fe(OH)2↓; 2NaCl+2H2O$\frac{\underline{\;电解\;}}{\;}$Cl2↑+H2↑+2NaOH.
点评 本题以电解原理为载体考查电极反应式的书写、金属腐蚀与防护等知识点,明确原电池和电解池原理及离子放电顺序是解本题关键,电极反应式的书写要结合电解质溶液酸碱性书写,题目难度不大.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | 蛋白质在体内经消化后生成碳酸.硫酸.尿酸等,故它属于酸性食物 | |
| B. | 葡萄吃起来是酸的,故它属于酸性食物 | |
| C. | 正常人人体内各体液pH总保持一定范围 | |
| D. | 食物的酸碱性与化学上所指溶液的酸碱性不同的 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 红棕色的NO2,加压后颜色先变深后变浅 | |
| B. | 高压比常压有利于合成SO3的反应 | |
| C. | 加入催化剂有利于氨的合成 | |
| D. | 工业制取金属钾的反应为:Na(l)+KCl(l)?NaCl(l)+K(g) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 空气,熟石灰,盐酸 | B. | 青铜,纯碱,水玻璃 | ||
| C. | 石英,二氧化硫,硫酸 | D. | 液氯,烧碱,漂白粉 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
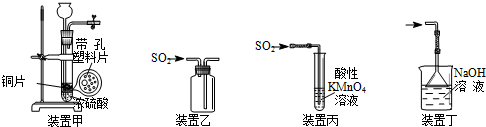
| A. | 用装置甲制取二氧化硫 | B. | 用装置乙收集二氧化硫 | ||
| C. | 用装置丙验证二氧化硫的漂白性 | D. | 用装置丁吸收二氧化硫 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
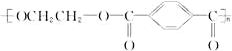
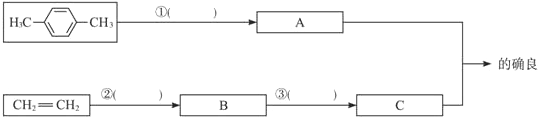
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
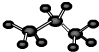
 的化学式为C8H12
的化学式为C8H12  与C8H6互为同分异构体
与C8H6互为同分异构体| A. | ①③④⑤ | B. | ①③ | C. | ②④⑥ | D. | ①② |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 6个碳原子有可能都在一条直线上 | B. | 有5个碳原子可能在一条直线上 | ||
| C. | 6个碳原子一定都在同一平面上 | D. | 6个碳原子不可能在同一平面上 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com