
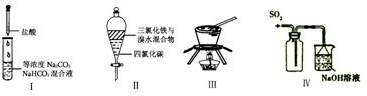
| A、实验Ⅰ:逐滴滴加盐酸时,试管中立即产生大量气泡 |
| B、实验Ⅱ:充分振荡后静置,下层溶液为橙红色,上层无色 |
| C、实验Ⅲ:从饱和食盐水中提取NaCl晶体 |
| D、装置Ⅳ:既可防止倒吸,又更加有利于SO2的充分吸收 |


 中考解读考点精练系列答案
中考解读考点精练系列答案科目:高中化学 来源: 题型:
| A、电离度可以表示弱电解质的相对强弱,它是已电离的电解质浓度占未电离分子浓度的百分比 |
| B、对同一弱电解质一般是浓度越小,温度越高,电离度越大 |
| C、pH=3的一元酸HA酸溶液稀释100倍后pH=5 |
| D、弱电解质的电离度随溶液的稀释而增大,溶液的导电性不断增强 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、标准状况下,22.4LH2O含有的分子数为1NA |
| B、常温常压下,106gNa2CO3含有的Na+离子数为2NA |
| C、通常状况下,1NA个CO2分子占有的体积为22.4L |
| D、物质的量浓度为0.5mol?/L的MgCl2溶液中,含有Cl-个数为1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、C15H27COOH |
| B、C15H31COOH |
| C、C17H31COOH |
| D、C17H33COOH |
查看答案和解析>>
科目:高中化学 来源: 题型:
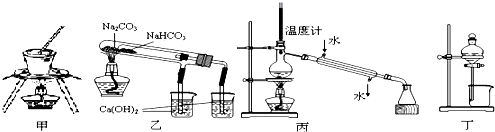
| A、用甲图装置可用于加热、灼烧固体 |
| B、用乙图装置验证NaHCO3和Na2CO3的热稳定性 |
| C、用丙图装置分离乙醇与水 |
| D、用丁图装置可由四氯化碳萃取碘水中的碘 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、二十碳五烯酸和二十二碳六烯酸是鱼油的主要成分,它们含有相同的官能团,是同系物,化学性质相似 |
B、结构简式为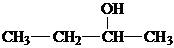 的有机物其名称为 2-丁醇 的有机物其名称为 2-丁醇 |
| C、分子式为C4H8Br2结构中含一个一CH3的同分异构体(不考虑立体异构)有4种 |
D、某有机物球棍结构模型为: ,则该有机物能发生消去反应和氧化反应 ,则该有机物能发生消去反应和氧化反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①③④⑤ | B、①③④⑤⑥ |
| C、②③④⑤ | D、①③④⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、c(N2)﹕c(H2)﹕c(NH3)=1﹕3﹕2 |
| B、N2,H2和NH3的质量分数不再改变 |
| C、气体压强的压强不再改变 |
| D、单位时间内每增加1 mol N2,同时增加3 mol H2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com