
【题目】(1)我国首艘国产航母于2017年4月顺利下水。制造航母需使用大量特种钢材、复合材料及光纤等。

①HSLA-100是一种航母甲板用钢,不属于这种钢材性质的是_________________(填字母)。
a.强度大 b.耐高温 c.密度小
②航母拦阻索最初由剑麻纤维和钢丝编织而成,现以尼龙和钢丝编织为主,下一代采用材质将是碳纤维。下列属于天然高分子材料的是__________________(填字母)。
a.剑麻纤维 b.尼龙 c.碳纤维
③航母信息系统上大量使用光导纤维,光导纤维的成分是________(填字母)。
a.3CaO·SiO2 b.SiO2 c.聚异戊二烯
(2)压缩鱼粉是由鱼粉、淀粉、水、山梨酸钾等配料加工而成,鱼粉中含有丰富的蛋白质、维生素及矿物元素钙、锌、硒、磷等。
①配料中,属于防腐剂的是___________________(填名称);钙、锌、硒、磷四种元素中属于微量元素的是___________________(填元素名称)。
②鱼粉蛋白质水解能生成多种氨基酸,写出甘氨酸的结构简式:___________________。
③配料中淀粉在人体中完全水解的化学方程式为_____________________。
(3)化学科学与污染防治及绿色发展密切相关。
①用清洁能源替代传统的化石能源是预防酸雨的有效途径之一。通常人们所说的酸雨,其主要有害成分是_____________________(填两种强酸的化学式);积极推广可降解塑料,减少使用聚乙烯等塑料,可防治的环境污染称为_____________________。
②纳米铁可修复被C2HCl3、NO![]() 污染的地下水。C2HCl3在纳米铁作用下,Cl被H取代最终转化为一种气态烃,该气态烃的结构简式为_____________________;NO3-在酸性条件下被纳米铁还原为N2(Fe被氧化为Fe2+)的离子方程式为_____________________。
污染的地下水。C2HCl3在纳米铁作用下,Cl被H取代最终转化为一种气态烃,该气态烃的结构简式为_____________________;NO3-在酸性条件下被纳米铁还原为N2(Fe被氧化为Fe2+)的离子方程式为_____________________。
③绿色合成是从源头上防治污染的前沿学科。水杨酸与(CH3CO)2O在绿色催化剂明矾催化下可生成阿司匹林和乙酸,该反应的化学方程式为_____________________。
【答案】 c a b 山梨酸钾 锌和硒 H2NCH2COOH ![]() H2SO4和HNO3 白色污染 H2C=CH2 5Fe +2NO3-+12H+ = 5Fe2++N2↑+6H2O
H2SO4和HNO3 白色污染 H2C=CH2 5Fe +2NO3-+12H+ = 5Fe2++N2↑+6H2O 
【解析】(1)①HSLA-100是一种航母甲板用钢,这种钢材的性质有强度大、耐高温,不可能具有密度小的性质,答案选c;②a.剑麻纤维属于天然高分子材料,a正确;b.尼龙是人工合成的,b错误;c.碳纤维是一种含碳量在95%以上的高强度、高模量纤维的新型纤维材料,不属于天然高分子材料,c错误,答案选a;③光导纤维的成分是SiO2,答案选b;(2)①配料中,属于防腐剂的是山梨酸钾;钙、锌、硒、磷四种元素中属于微量元素的是锌和硒。②甘氨酸的结构简式为H2NCH2COOH。③淀粉在人体中完全水解的化学方程式为![]() 。(3)①通常人们所说的酸雨,其主要有害成分是H2SO4和HNO3;积极推广可降解塑料,减少使用聚乙烯等塑料,可防治的环境污染称为白色污染。②C2HCl3在纳米铁作用下,Cl被H取代最终转化为一种气态烃,该气态烃的分子式为C2H4,所以结构简式为H2C=CH2;氮元素化合价从+5价降低到0价,铁元素化合价从0价升高到+2价,根据电子得失守恒和原子守恒以及电荷守恒可知反应的离子方程式为5Fe+2NO3-+12H+=5Fe2++N2↑+6H2O。③水杨酸与(CH3CO)2O在绿色催化剂明矾催化下可生成阿司匹林和乙酸,该反应的化学方程式为
。(3)①通常人们所说的酸雨,其主要有害成分是H2SO4和HNO3;积极推广可降解塑料,减少使用聚乙烯等塑料,可防治的环境污染称为白色污染。②C2HCl3在纳米铁作用下,Cl被H取代最终转化为一种气态烃,该气态烃的分子式为C2H4,所以结构简式为H2C=CH2;氮元素化合价从+5价降低到0价,铁元素化合价从0价升高到+2价,根据电子得失守恒和原子守恒以及电荷守恒可知反应的离子方程式为5Fe+2NO3-+12H+=5Fe2++N2↑+6H2O。③水杨酸与(CH3CO)2O在绿色催化剂明矾催化下可生成阿司匹林和乙酸,该反应的化学方程式为 。
。


 新思维假期作业暑假吉林大学出版社系列答案
新思维假期作业暑假吉林大学出版社系列答案 蓝天教育暑假优化学习系列答案
蓝天教育暑假优化学习系列答案科目:高中化学 来源: 题型:
【题目】写出下列反应的化学方程式。
(1)AlCl3水解溶液呈酸性________
(2)将TiCl4加入热水中生成TiO2.xH2O________
(3)向Na2S2O3溶液中加入稀硫酸__________
(4)在Mg(OH)2悬浊液中加入NH4Cl溶液,沉淀溶解___________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】ClO2是一种消毒杀菌效率高、二次污染小的水处理剂。实验室可通过以下反应制得ClO2:2KClO3+H2C2O4+H2SO4![]() 2ClO2↑+K2SO4+2CO2↑+2H2O,下列说法正确的( )
2ClO2↑+K2SO4+2CO2↑+2H2O,下列说法正确的( )
A. 1 molKClO3参加反应有1mole- 转移 B. ClO2是氧化产物
C. H2C2O4在反应中被还原 D. KClO3在反应中得到电子,作还原剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对金属制品进行腐蚀处理,可延长其使用寿命。
(1)以下为铝材表面处理的一种方法:
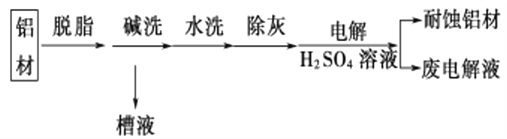
①碱洗的目的是除去铝材表面的自然氧化膜,碱洗时常有气泡冒出,原因是__________________(用离子方程式表示)。
为将碱洗后槽液中的铝以沉淀形式回收,最好向槽液中加入下列试剂中的__________。
a.NH3 b.CO2 c.NaOH d.HNO3
②以铝材为阳极,在H2SO4溶液中电解,铝材表面形成氧化膜,阳极的电极反应式为________________________________________________________________。
(2)镀铜可防止铁制品腐蚀,电镀时用铜而不用石墨作阳极的原因是______________________________________________________________。
(3)利用如图装置,可以模拟铁的电化学防护。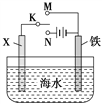
若X为碳棒,为减缓铁的腐蚀,开关K应置于______处。
若X为锌,开关K置于M处,该电化学防护法称为_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把V L含有MgSO4和K2SO4的混合溶液分成两等份,一份加入含a mol NaOH的溶液,恰好使镁离子完全沉淀为氢氧化镁;另一份加入含b mol BaCl2的溶液,恰好使硫酸根离子完全沉淀为硫酸钡,则原混合溶液中钾离子物质的量浓度为( )
A. 2(2b-a)/V mol·L-1 B. (2b-a)/V mol·L-1 C. 2(b-a)/V mol·L-1 D. (b-a)/V mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关物质的转化关系如下图所示(部分生成物和反应条件已略去)。B的焰色反应呈黄色,C、D、E、G是常见的气体, C 、D、E是单质且C呈黄绿色;H与G的组成元素相同,H的摩尔质量为32g·mol-1,I是常见的盐类,J是紫红色金属单质。
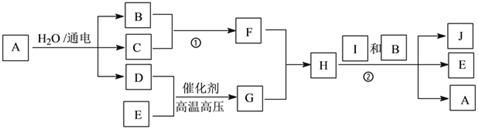
(1)D的化学式为_____________________。
(2)G的电子式为_____________________。
(3)写出反应①的离子方程式:_____________________。
(4)写出反应②的化学方程式:_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把500![]() 有
有![]() 和
和![]() 的混合溶液分成5等份,取一份加入含
的混合溶液分成5等份,取一份加入含![]()
![]() 硫酸钠的溶液,恰好使钡离子完全沉淀;另取一份加入含
硫酸钠的溶液,恰好使钡离子完全沉淀;另取一份加入含![]()
![]() 硝酸银的溶液,恰好使氯离子完全沉淀。则该混合溶液中钾离子浓度为
硝酸银的溶液,恰好使氯离子完全沉淀。则该混合溶液中钾离子浓度为
A. ![]() B.
B. ![]()
C. ![]() D.
D. ![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有甲、乙两个完全相同的装置,分别在它们的侧管中装入1.06g Na2CO3和0.84g NaHCO3,试管中各有10mL相同浓度的盐酸(如图),同时将两个侧管中的物质全部倒入各自的试管中,下列叙述正确的是
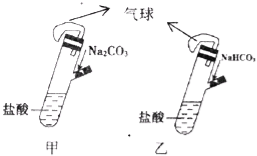
A. 甲装置的气球膨胀速率大
B. 若最终两气球体积相同,则一定有c(HCl)≥2 mol/L
C. 若最终两气球体积不同,则一定有c(HCl)≤1 mol/L
D. 最终两溶液中Na+、Cl﹣的物质的量相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 铅蓄电池放电时负极质量减轻,充电时阳极质量增加
B. 同温下,0.1 mol·L-1醋酸溶液pH=a,0.01 mol·L-1醋酸溶液pH=b,则a+1<b
C. 钢铁水闸可用牺牲阳极的阴极保护法或外加电流的阴极保护法进行防护
D. 一定条件下反应N2+3H2![]() 2NH3,当3v正(H2)=2v逆(NH3),则反应达到平衡
2NH3,当3v正(H2)=2v逆(NH3),则反应达到平衡
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com