
【题目】Na2SO3与下列物质的反应中,体现的性质与其他3个反应不同的是
A.盐酸B.Ca(OH)2C.BaCl2D.O2
 导学教程高中新课标系列答案
导学教程高中新课标系列答案 小学课时特训系列答案
小学课时特训系列答案科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分,针对表中的①~⑨种元素,填写下列空白(填写序号不得分):
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 族 |
2 | ① | ② | ③ | ④ | ||||
3 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
4 | ⑨ | ⑩ |
(1)写出元素③的离子结构示意图_________,该离子半径________S2-(填“﹥”或“﹤”) ;
(2)上述元素中最高价氧化物对应的水化物的酸性最强的是(填化学式,下同)_________;
(3)上述元素中金属性最强的是_________,写出其与水反应的化学方程式____________;
(4)由④、⑧、⑩三种元素形成的简单氢化物的沸点由高到低的顺序是_______________;
(5)②可以形成多种氧化物,其中一种是红棕色气体,试用方程式说明该气体不宜采用排水法收集的原因是______(用化学方程式来表示);标况下将一装满该气体的试管倒立于水槽中,足够时间后,水面会上升到 试管容积的________处,所得试管内溶液物质的量浓度为___________mol/L(假设溶质全部留在试管中);
(6)设计实验验证比较元素③、⑦的非金属性强弱:_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】华中科技大学一项科学研究表明:一种被称为Li-空气微型石墨烯超级电容器的电池,它充电和放电的速率是标准电池的100至1000倍。该电池由单原子层的碳构成,放电时将锂氧化产生锂离子和电子,空气中的氧分子得到电子进行还原反应,从而产生电能。则下列说法正确的是
A. Li电极是该电池的正极
B. O2在电极上发生氧化反应,其电极反应式为:O2 + 2H2O + 4e-=4OH-
C. 12g单层石墨中含有六元环的个数为0.5NA(结构示意图如图,NA表示阿伏加德罗常数的值)

D. 放电时,电池中有OH-向负极移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从薄荷中提取的薄荷醇可制成医药。薄荷醇的结构简式如下图,下列说法正确的是

A. 薄荷醇分子式为C10H20O,它是环己醇的同系物
B. 薄荷醇的分子中至少有12个原子处于同一平面上
C. 薄荷醇在Cu或Ag做催化剂、加热条件下能被O2氧化为醛
D. 在一定条件下,薄荷醇能发生取代反应、消去反应和聚合反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙酸锰可用于制造钠离子电池的负极材料。可用如下反应制得乙酸锰:4Mn(NO3)2·6H2O+26(CH3CO)2O =4(CH3COO)3Mn +8HNO2+ 3O2↑+40CH3COOH
(1)Mn3+基态核外电子排布式为______。
(2)NO中氮原子轨道的杂化类型是______。
(3)与HNO2互为等电子体的一种阴离子的化学式为______。
(4)配合物[Mn(CH3OH)6]2+中提供孤对电子的原子是______。
(5)CH3COOH能与H2O任意比混溶的原因,除它们都是极性分子外还有______。
(6)镁铝合金经过高温淬火获得一种储钠材料,其晶胞为立方结构(如图所示),图中原子位于顶点或面心。该晶体中每个铝原子周围距离最近的镁原子数目为______。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为反应2H2(g)+O2(g)===2H2O(g)的能量变化示意图,下列说法错误的是

A.拆开2molH2(g)和1molO2(g)中的化学键共吸收1368kJ能量
B.由H、O原子形成2molH2O(g),共放出1852kJ能量
C.1molH2(g)和1/2molO2(g)反应生成1molH2O(l),放出热量小于242kJ
D.2molH2(g)和1molO2(g)反应生成2molH2O(g),共放出484kJ热量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A+、B+、C-、D、E、F2- 6种微粒(分子或离子),它们分别含10个电子,其中只有B+和F2-为单核微粒,且C-和E的组成元素相同,已知它们有如下转化关系:A++C-![]() D+E,据此回答下列问题:
D+E,据此回答下列问题:
(1)写出D的结构式___________,E的结构式___________。
(2)实验室制备D物质的反应方程式________。
(3)上述六种微粒中所含有的元素原子半径从大到小的顺序是__(用元素符号表示)。
(4)B、F两元素组成的原子数目比为1:1的化合物的电子式___________、该物质中存在的化学键有__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组为探究元素性质的递变规律,设计如下系列实验。
Ⅰ.(1)将钠、钾、镁、铝各1 mol分别投入到足量的0.1 mol·L-1的盐酸中,试预测实验结果:_______与盐酸反应最剧烈,____与盐酸反应最慢。
Ⅱ. 利用如图装置可以验证非金属性的变化规律。
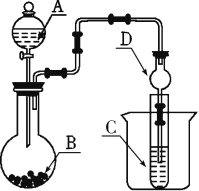
(2)仪器A的名称为_______,干燥管D的作用是_____。
(3)实验室中现有药品Na2S、KMnO4、浓盐酸、MnO2,请选择合适药品设计实验验证氯的非金属性大于硫的;装置A、B、C中所装药品分别为___、___、.____,装置C中的实验现象为有黄色沉淀生成,离子方程式为__________________。
(4)若要证明非金属性:S>C>Si,则A中加____,B中加Na2CO3,C中加_____,观察到C中溶液的现象为_____________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com