
| A. | MgCl2 NaOH | B. | HCl SiO2 | C. | NaOH NH4Cl | D. | 红磷 金刚石 |
分析 离子化合物含有离子键,可能含有共价键,共价化合物只含共价键,双原子分子或多原子分子含有共价键;离子晶体的构成微粒为离子,分子晶体的构成微粒为分子,原子晶体的构成微粒为原子,以此来解答.
解答 解:A.MgCl2中只含离子键,NaOH中含共价键和离子键,均为离子晶体,但化学家类型不完全相同,故A不选;
B.HCl是分子晶体,二氧化硅是原子晶体,HCl、二氧化硅都只含共价键,故B不选;
C.NaOH、NH4Cl均为离子晶体,并且都含共价键和离子键,则晶体类型和化学键类型完全相同,故C选;
D.红磷是分子晶体,金刚石是原子晶体,红磷、金刚石都只含共价键,故D不选;
故选C.
点评 本题考查了化学键类型和晶体类型的关系,注意判断依据为:离子晶体中阴阳离子以离子键结合,原子晶体中原子以共价键结合,分子晶体中分子之间以范德华力结合,分子内部存在化学键,题目难度不大.


科目:高中化学 来源: 题型:多选题

| A. | 当溶液pH=7时:c(NH4+)>c(H2CO3)+2c(CO32-) | |
| B. | 当溶液pH=9.5时:c(OH-)-c(H+)>c(NH4+)-3c(CO32-) | |
| C. | 若刚好是(NH4)2CO3溶液:c(OH-)+C(NH3•H2O)>c(H+)+c(H2CO3)+c(HCO3-) | |
| D. | 若刚好是NH4HCO3溶液,向其中加入等体积、等物质的量浓度的NaCl溶液,析出部分晶体,过滤所得的滤液中:c(Na+)=c(Cl-)>c(NH4+)>c(HCO3-)>c(CO32-) |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题

| A. | 反应①、②的类型分别为加成反应和取代反应 | |
| B. | 邻羟基苯甲醛分子中所有的原子不可能在同一平面内 | |
| C. | 邻羟基苯甲醛、邻羟基苯甲酸均能与FeCl3发生显色反应 | |
| D. | 1mol阿司匹林与足量NaOH溶液反应,消耗3mol的 NaOH |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
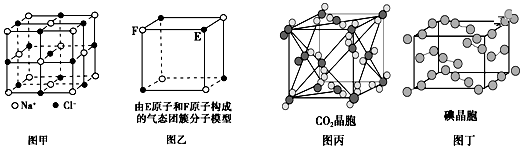
| A. | 在NaCl晶体(图甲)中,距Na+最近的Cl-形成正八面体 | |
| B. | 该气态团簇分子(图乙)的分子式为EF或FE | |
| C. | 在CO2晶体(图丙)中,一个CO2分子周围有12个CO2分子紧邻 | |
| D. | 在碘晶体(图丁)中,存在非极性共价键和范德华力 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用食醋可除去热水壶内壁的水垢 | B. | 医用酒精的浓度通常为95% | ||
| C. | 烹鱼时加适量醋和酒可以增加香味 | D. | 碘盐中的碘不可以直接用淀粉检验 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com