

分析 (1)电解食盐水生成NaOH、H2和Cl2,以此书写离子方程式;A.阴离子交换膜只有阴离子自由通过;B.根据图知,左边半室氯离子放电生成氯气,右边半室氢离子放电生成氢气,则X是氯气、Y是氢气;C.电解槽右室中氢离子放电;D.电解槽左室为阳极室;
(2)钛铁矿经氯化得到四氯化钛、氯化铁和一氧化碳;依据原子守恒配平写出,根据得失电子计算生成2 mol四氯化钛时转移的电子的物质的量;
(3)原电池中负极上燃料失电子,碱性条件下,CH3OH反应生成碳酸根离子;
(4)在Ar气中进行防止钛、镁被氧化;控制温度使TiCl4、Mg、MgCl2转化为蒸气,Ti不融化;
(5)①先根据燃烧热分别写出CO、H2、CH3OH热化学方程式后,根据盖斯定律就可得出CO和H2合成甲醇的热化学方程式;
②根据甲醇的物质的量计算需要CO、H2的物质的量,根据n(CO)计算电解中生成的n(Cl2),进而计算电解生成n(H2),据此计算解答.
解答 解:(1)电解食盐水生成NaOH、H2和Cl2,反应的离子方程式为:2Cl-+2H2O$\frac{\underline{\;电解\;}}{\;}$2OH-+H2↑+Cl2↑,
A.阴离子交换膜只有阴离子自由通过,阳离子和分子不能通过,故A错误;
B.根据图知,左边半室氯离子放电生成氯气,右边半室氢离子放电生成氢气,则X是氯气、Y是氢气,故B错误;
C.电解槽右室中氢离子放电,电极反应式为2H++2e-═H2↑,故C正确;
D.电解槽左室中电极为阳极,所以为阳极室,右室为阴极室,故D错误;
故答案为:2Cl-+2H2O$\frac{\underline{\;电解\;}}{\;}$2OH-+H2↑+Cl2↑;C;
(2)从图示可知氯化时的反应物为FeTiO3、C、Cl2,生成物为FeCl3、TiCl4、CO,再根据得失电子和原子守恒即可得出该反应的方程式为2FeTiO3+6C+7Cl2$\frac{\underline{\;高温\;}}{\;}$2FeCl3+2TiCl4+6CO,由方程式得出生成2molTiCl4转移14mol电子,所以生成2mol四氯化钛时转移电子的物质的量为14mol;
故答案为:2FeTiO3+6C+7Cl2$\frac{\underline{\;高温\;}}{\;}$2FeCl3+2TiCl4+6CO;
(3)原电池放电时,甲醇失电子被氧化,应为电池负极反应,其电极反应式为:2CH3OH+3O2+4OH-=2CO32-+6H2O,
故答案为:CH3OH+8OH--6e-=CO32-+6H2O;
(4)在Ar气中进行防止钛、镁被氧化,保护气作用,
故答案为:保护气作用;
(5)①CO燃烧的热化学方程式:H2燃烧的热化学方程式:2H2(g)+O2(g)═2H2O(l)△H=-285.8×2 kJ•mol-1 ①
CO(g)+$\frac{1}{2}$O2(g)═CO2(g)△H=-283kJ•mol-1②
CH3OH燃烧的热化学方程式:CH3OH(l)+$\frac{3}{2}$O2(g)═CO2(g)+2H2O(l)△H=-726.5kJ•mol-1 ③
根据盖斯定律将①+②+(-③)可得:CO(g)+2H2(g)═CH3OH(l)△H=-128.1KJ•mol-1,
故答案为:CO(g)+2H2(g)═CH3OH(l)△H=-128.1KJ•mol-1;
②由CO(g)+2H2(g)?CH3OH(g)可知,合成6mol甲醇需要n(CO)=6mol、n(H2)=12mol.根据2FeTiO3+6C+7Cl2$\frac{\underline{\;高温\;}}{\;}$2FeCl3+2TiCl4+6CO可知,电解中生成的n(Cl2)=$\frac{7}{6}$n(CO)=7mol,根据2NaCl+2H2O$\frac{\underline{\;电解\;}}{\;}$2NaOH+H2↑+Cl2↑可知,电解生成n(H2)=n(Cl2)=7mol,故需额外补充H2 为12mol-7mol=5mol,V=5×22.4=112L;
故答案为:112.
点评 本题以氯碱工业为载体考查了电解池原理、考查了化学方程式的书写及计算、盖斯定律等,注意(1)会根据图中物质浓度变化确定电极发生的反应为解本题关键,知道离子交换膜的作用、各个电极上发生的反应,题目难度中等.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
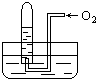 如图所示,试管中盛装的是红棕色气体,当倒扣在盛有水的水槽中时,试管内水面上升,但不能充满试管;当向试管内鼓入氧气后,可以观察到试管中水面继续上升,经过多次重复后,试管被水充满,则原来试管中盛装的气体是( )
如图所示,试管中盛装的是红棕色气体,当倒扣在盛有水的水槽中时,试管内水面上升,但不能充满试管;当向试管内鼓入氧气后,可以观察到试管中水面继续上升,经过多次重复后,试管被水充满,则原来试管中盛装的气体是( )| A. | 肯定是NO2气体 | B. | 肯定是O2与NO2的混合气体 | ||
| C. | 肯定是NO与O2的混合气体 | D. | 可能是NO与NO2的混合气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验 | 现象 | 结论 |
| A | 在 CuSO4溶液中加入一小块Na | Na溶解,生成沉淀 | 有Cu产生 |
| B | 将浓氨水滴加至烧瓶中的CaO上 | 产生的气体可使湿润的红色石蕊试纸变蓝 | 有氨气生成 |
| C | 在Fe(NO3)2溶液中加入稀H2SO4 | 溶液变为黄色 | 稀H2SO4具有氧化性 |
| D | 将氨气通入I2-淀粉溶液中 | 溶液蓝色褪去 | 氯气具有漂白性 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
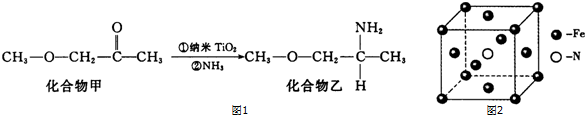
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1molFeCl3水解生成的Fe(OH)3胶粒数为1NA | |
| B. | 4.6g有机物C2H6O的分子结构中含有的C-H键数目一定为0.5NA | |
| C. | 标准状况下,11.2LCO2与足量Na2O2反应转移的电子数为0.5NA | |
| D. | 1mol•L-1AlCl3溶液中含有3NA个Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径大小为W>X>Z>Y | |
| B. | X、Y、Z的氢化物的水溶液均呈酸性 | |
| C. | W与Y形成的三原子化合物既含极性共价键又含非极性共价键 | |
| D. | Z元素的最高价氧化物对应的水化物酸性最强 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
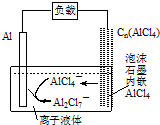
| A. | 放电时,负极发生:2AlCl4--e-=Al2Cl7-+Cl- | |
| B. | 放电时,电路中每流过3mol电子,正极减少27g | |
| C. | 充电时,泡沫石墨极与外电源的负极相连 | |
| D. | 充电时,阴极发生:4Al2Cl7-+3e-=Al+7AlCl4- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硫离子的结构示意图: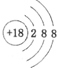 | B. | 中子数为20的氯原子:${\;}_{17}^{20}$Cl | ||
| C. | 电子转移情况: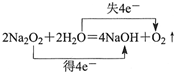 | D. | 氮分子的结构式:N≡N |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com