
| 实验步骤 | 实验操作 | 预期现象与结论 |
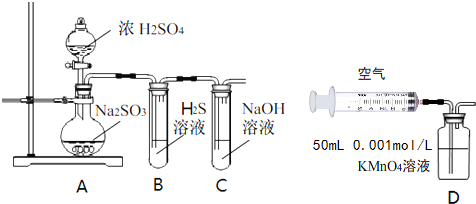
分析 装置图分析可知,A中是二氧化硫气体的发生装置,生成的二氧化硫具有还原性和氧化性,通过硫化氢溶液被硫化氢还原生成单质硫,通过氢氧化钠溶液被吸收生成硫化钠、亚硫酸钠,装置D用注射器向装置D共注入v mL实验室制备SO2的空气,当溶液刚好褪色是空气中二氧化硫和高锰酸钾溶液反应,测定空气中二氧化硫的含量,
(1)装置A中是二氧化硫气体的发生装置,亚硫酸钠和硫酸反应生成二氧化硫气体;
(2)分液漏斗中液体不能继续流下是压强的影响,可能是分液漏斗上口活塞上的凹槽没有与分液漏斗上的小孔连通或没有打开分液漏斗的上口活塞;
(3)装置B中的溶液出现浑浊是硫化氢和二氧化硫发生氧化还原反应生成单质硫,依据元素化合价变化分析判断二氧化硫的性质;
(4)实验后,测定装置C中溶液呈碱性,可能的原因是二氧化硫和氢氧化钠溶液反应,氢氧化钠剩余使溶液显碱性或恰好反应生成亚硫酸钠,溶液中亚硫酸根离子水解显碱性,设计实验验证溶液中成分是氢氧化钠和亚硫酸钠还是亚硫酸钠;
解答 解:(1)装置A中是二氧化硫气体的发生装置,亚硫酸钠和硫酸反应生成二氧化硫气体,反应的化学方程式为:Na2SO3(固)+H2SO4(浓)=Na2SO4+SO2↑+H2O;
故答案为:Na2SO3(固)+H2SO4(浓)=Na2SO4+SO2↑+H2O;
(2)实验时,旋开装置A中分液漏斗的旋塞,发现液体流出缓慢,最终停止,其可能的原因是没有打开分液漏斗的上口活塞或分液漏斗上口活塞上的凹槽没有与分液漏斗上的小孔连通,导致无法与外界大气连通;
故答案为:没有打开分液漏斗的上口活塞或分液漏斗上口活塞上的凹槽没有与分液漏斗上的小孔连通,导致无法与外界大气连通;
(3)装置B中的溶液出现浑浊是硫化氢和二氧化硫发生氧化还原反应生成单质硫,反应的化学方程式为:
2H2S+SO2=3S+2H2O,二氧化硫中硫元素化合价+4价变化为0价,化合价降低得到电子做氧化剂,所以二氧化硫在此反应中表现了氧化性;
故答案为:氧化性;
(4)分析流程可知,生成的二氧化硫气体最后通入氢氧化钠溶液,测定装置C中溶液呈碱性,可能的原因是二氧化硫和氢氧化钠溶液反应,氢氧化钠剩余使溶液显碱性或恰好反应生成亚硫酸钠,溶液中亚硫酸根离子水解显碱性,设计实验验证溶液中成分是氢氧化钠和亚硫酸钠还是亚硫酸钠,具体步骤和现象为:取少量装置C中的溶液于试管中滴入几滴酚酞,溶液显红色,然后滴入足量氯化钡溶液,若为氢氧化钠溶液和亚硫酸钡的混合溶液,出现的现象是溶液红色不变化,若为亚硫酸钠溶液,加入足量氯化钡溶液后,亚硫酸根离子全部和钡离子结合生成沉淀,溶液红色消失,具体实验操作和反应现象与结论为:取少量溶液于试管,滴入几滴酚酞,然后加入足量的BaCl2溶液,溶液先变红,然后产生沉淀,最后若红色褪去,则说明①正确;若红色不能褪去,则说明②正确;
故答案为:
| 实验步骤 | 实验操作 | 预期现象与结论 |
| I | 取少量溶液于试管,滴入几滴酚酞,然后加入足量的BaCl2溶液 | 溶液先变红,然后产生沉淀,最后若红色褪去,则说明①正确;若红色不能褪去,则说明②正确. |
点评 本题考查了物质性质的实验制备方法,物质性质和现象的分析判断,主要是物质组成的实验设计方法和步骤设计,掌握基础是解题关键,题目难度中等.


 步步高口算题卡系列答案
步步高口算题卡系列答案 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案 小学教材完全解读系列答案
小学教材完全解读系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 易形成-1价离子 | B. | 从上到下原子半径逐渐减小 | ||
| C. | 从上到下单质的氧化性逐渐减弱 | D. | 从上到下氢化物的稳定性依次减弱 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 三聚氰胺的摩尔质量为126 | |
| B. | 用三聚氰胺制造的餐具不可以放进微波炉中加热使用 | |
| C. | 三聚氰胺中C、N两种元素的质量比为3:7 | |
| D. | 三聚氰胺中氮元素的质量分数约为66.7% |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 沼气和液化石油气都是可再生能源 | |
| B. | 煤经气化、液化和干馏三个物理变化过程,可变为清洁能源 | |
| C. | PM 2.5含有的铅、铬、砷等对人体有害的元素均是重金属元素 | |
| D. | 医药中常用酒精来消毒,是因为酒精能够使细菌蛋白体发生变性 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com