
分析:先根据氧化还原反应中得失电子相等配平方程式,还原剂对应的产物是氧化产物,氧化剂对应的产物是还原产物,从而确定氧化产物和还原产物之比.
解答:该分子中铵根离子中的氮原子失电子,一个铵根离子失去3个电子生成氮原子,硝酸根离子中的氮原子得电子,一个硝酸根离子得到5个电子生成氮原子,其最小公倍数是15,所以其反应方程式为5NH4NO3=4N2+2HNO3+9H2O.所以氧化剂和还原剂都是硝酸铵,氧化产物和还原产物都是氮气,氧化产物和还原产物之比=铵根离子和参加氧化还原反应的硝酸根离子之比=5:3。
故选B.
点评:本题考查了氧化还原反应中的有关计算,难度不大,能根据得失电子守恒配平该反应方程式是解本题的关键.


科目:高中化学 来源: 题型:单选题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
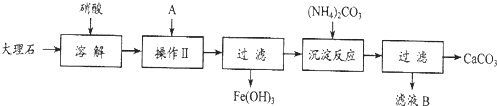
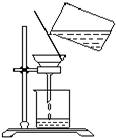
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
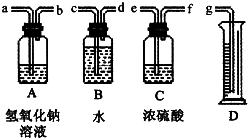 某环保部门调查指出:大气中的酸性气体有相当一部分来自全国数以万计的高校、中学的化学实验室.为此某校化学研究小组的同学拟从下面提供的实验用品中选取合适的装置和药品,组装成一套实验装置,用来粗略测定实验室里空气中全部酸性气体的体积分数.
某环保部门调查指出:大气中的酸性气体有相当一部分来自全国数以万计的高校、中学的化学实验室.为此某校化学研究小组的同学拟从下面提供的实验用品中选取合适的装置和药品,组装成一套实验装置,用来粗略测定实验室里空气中全部酸性气体的体积分数.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
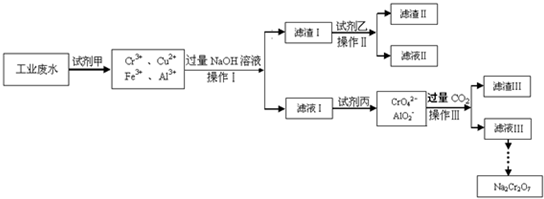
 NaCrO2
NaCrO2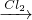 Na2CrO4
Na2CrO4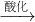 Na2Cr2O7
Na2Cr2O7查看答案和解析>>
科目:高中化学 来源: 题型:单选题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com