
从明矾[KAl(SO4)2·12H2O]制备Al、K2SO4和H2SO4的流程如下:
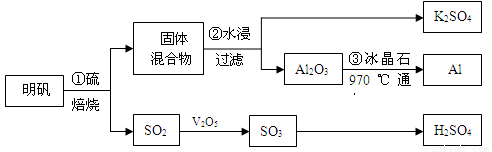
已知:明矾焙烧的化学方程式为:4[KAl(SO4)2·12H2O] + 3S=2K2SO4 + 2Al2O3 + 9SO2↑+ 48H2O
请回答下列问题:
(1)在焙烧明矾的反应中,氧化产物与还原产物的物质的量之比为: 。
(2)步骤②中,为提高浸出率,可采取的措施有_____________。
A.粉碎固体混合物 B.降低温度 C.不断搅拌 D.缩短浸泡时间
(3)明矾焙烧完全后,从步骤②的滤液中得到K2SO4晶体的方法是 。
(4)步骤③电解的化学方程式是 ,电解池的电极是用碳素材料做成,电解过程中,阳极材料需要定期更换,原因是: 。
(5)以Al和NiO(OH)为电极,NaOH溶液为电解液组成一种新型电池,放电时NiO(OH)
转化为Ni(OH)2,则该电池的正极电极反应式是 。
(6)焙烧a吨明矾(摩尔质量为b g/mol),若SO2 的转化率为96%,可生产质量分数为98%的H2SO4质量为 吨(列出计算表达式)。
科目:高中化学 来源:2016届河南省开封市高三上学期第一次模拟理综化学试卷(解析版) 题型:推断题
[化学—选修5有机化学基础]水杨酸酯E为紫外吸收剂,可用于配制防晒霜。E的一种合成路线如下。
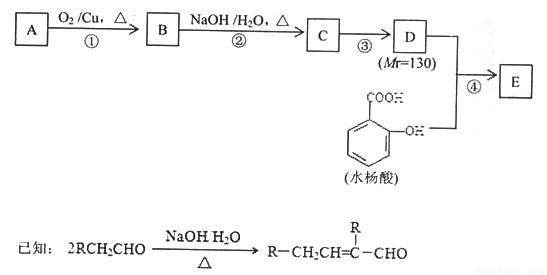
请回答下列问题。
(1)一元醇A中氧的质量分数约为21.6%,则A的分子式为______;结构分析显示A只有一个甲基,A的名称为______。F与A互为同分异构体,F的核磁共振氢谱图有2组峰,且峰面积比为9:1。则F与浓HBr溶液共热生成有机物的结构简式为 。
(2)B能与新制的Cu(OH)2发生反应,该反应的化学方程式为 。
(3)C中所含官能团的名称为 ,若要检验C中所含官能团,一次取样检验,按使用的先后顺序写出所用试剂______。
(4)第③步的反应类型为______;第④步的反应条件为______;E的结构简式为______。
查看答案和解析>>
科目:高中化学 来源:2016届湖北省枣阳市高三上学期第四次月考理综化学试卷(解析版) 题型:选择题
用 NA表示阿伏加德罗常数的值。下列说法正确的是
A.7.8 g Na2O2中含有的阴离子数目为0.2NA
B.3.2 g O2和O3的混合气中含有的氧原子数目为0.2NA
C.1mol N2与3mol H2混合充分反应,转移的电子数目为6NA
D.过氧化氢分解制得标准状况下1.12 L O2,转移电子数目为 0.2NA
查看答案和解析>>
科目:高中化学 来源:2016届江苏省南京市六校高三上学期12月联考化学试卷(解析版) 题型:推断题
化合物E是一种医药中间体,常用于制备抗凝血药,可以通过下图所示的路线合成:
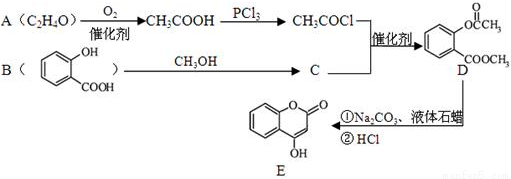
(1)B中含有的含氧官能团名称为 。
(2)C转化为D的反应类型是 。
(3)写出D与足量NaOH溶液完全反应的化学方程式 。
(4)1molE最多可与 molH2加成。
(5)写出同时满足下列条件的B的一种同分异构体的结构简式 。
A.能发生银镜反应
B.核磁共振氢谱只有4个峰
C.能与FeCl3溶液发生显色反应,水解时1mol可消耗3molNaOH
(6)已知工业上以氯苯水解制取苯酚,而酚羟基一般不易直接与羧酸酯化。甲苯可被酸性高锰酸钾溶液氧化为苯甲酸。
苯甲酸苯酚酯( )是一种重要的有机合成中间体。试写出以苯、甲苯为原料制取该化合物的合成路线流程图(无机原料任选)。
)是一种重要的有机合成中间体。试写出以苯、甲苯为原料制取该化合物的合成路线流程图(无机原料任选)。
合成路线流程图示例如下: 。
。
查看答案和解析>>
科目:高中化学 来源:2016届江西省高三上学期第三次月考化学试卷(解析版) 题型:选择题
一般情况下,前者无法决定后者的是
A.原子核外电子排布——元素在周期表中的位置
B.弱电解质的相对强弱——电离常数的大小
C.分子间作用力的大小——分子稳定性的高低
D.物质内部储存的能量——化学反应的热效应
查看答案和解析>>
科目:高中化学 来源:2016届上海市十三校高三上学期第一次联考化学试卷(解析版) 题型:填空题
空气质量日报中有一项重要检测指标是SO2的含量,结合所学知识回答下列问题。
工业制硫酸的过程中,SO2催化氧化的原理为:2SO2(g)+O2(g) 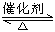 2SO3(g) + Q
2SO3(g) + Q
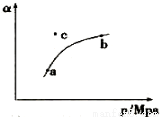
某温度下,测得SO2(g)的平衡转化率(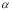 )与体系总压强( p )的关系如上图所示。
)与体系总压强( p )的关系如上图所示。
28.a、b两点对应的平衡常数K(a) K(b) (填“>”、 “<”或“=”,下同),SO3浓度c(a) c(b)。c点时,反应速率υ(正) υ(逆)。
将一定量的SO2(g)和O2(g)分别通入到体积为2L的恒容密闭容器中,在不同温度下进行反应得到如下表中的两组数据:
实验编号 | 温度/℃ | 起始量/mol | 平衡量/mol | ||
SO2 | O2 | SO2 | O2 | ||
1 | T1 | 4 | 2 | x | 0.8 |
2 | T2 | 4 | 2 | 0.4 | y |
29.实验1从开始到反应达到化学平衡时,用去时间t 分钟,则υ(SO2)表示的反应速率为 ,温度T1大于T2的理由是 。
30.制取SO2的尾气用NaOH溶液吸收,可得到Na2SO3和NaHSO3两种盐。
①0.1 mol/L的NaHSO3溶液中c(H+) >c(OH-),用水解和电离理论的角度解释其原因 ,若往溶液中加入氨水至中性,则c(Na+) c(HSO3-)+c(SO32-)+c(H2SO3) (填“>”、 “﹤”或 “=”)。
②往0.1 mol/L 的Na2SO3溶液加入少量NaOH固体,完全溶解后溶液中c(Na+) : c(SO32-)的比值 (填“变大”、“变小”或“保持不变”)。
查看答案和解析>>
科目:高中化学 来源:2016届浙江省高三上学期第三次月考化学试卷(解析版) 题型:选择题
下列有关物质的性质与应用不相对应的是
A.SO2具有氧化性,可用于漂白纸浆
B.淀粉溶液遇碘变成蓝色,可用于检验碘单质的存在
C.Fe在常温下遇浓硫酸发生钝化,可用铁制容器盛放冷的浓硫酸
D.Zn具有还原性和导电性,可用作锌锰干电池的负极材料
查看答案和解析>>
科目:高中化学 来源:2016届河北省张家口市四校高三上学期联考化学试卷(解析版) 题型:选择题
有机物X和Y可作为“分子伞”给药载体的伞面和中心支撑架(未表示出原子或原子团的空间排列)。
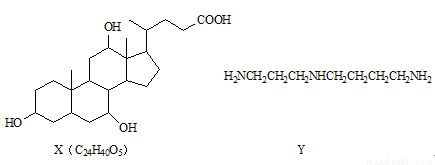
下列叙述错误的是
A.1mol X在浓硫酸作用下发生消去反应,最多生成3mol H2O
B.1mol Y发生类似酯化的反应,最多消耗2mol X
C.X与足量HBr反应,所得有机物的分子式为C24H37O2Br3
D.Y和癸烷的分子链均呈锯齿形,但Y的极性较强
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com