
| A. | 单质Z可用海水作原料获得 | |
| B. | W的简单气态氢化物比Y的简单气态氢化物稳定 | |
| C. | 原子半径由大到小的顺序:Z、Y、X、W | |
| D. | WX与ZX中的化学键类型相同 |
分析 短周期元素W、X、Y、Z的原子序数依次增大,W的单质是空气体积分数最大的气体,W为N元素;W与Y最外层电子数之和为X最外层电子数的2倍,设Y的最外层电子数为y,X的最外层电子数为x,则5+y=2x,y=1时x=3,y=3时x=4,y=7时x=6,结合X、Y、Z简单离子的电子层结构相同,Z最外层电子数等于最内层电子数,Z为Mg,由原子序数可知只有y=7时x=6符合,即Y为F,X为O,以此来解答.
解答 解:由上述分析额裤子,W为N,X为O,Y为F,Z为Mg,
A.海水中含氯化镁,电解熔融氯化镁可得到Mg,故A正确;
B.非金属性F>N,则Y的简单气态氢化物比W的简单气态氢化物稳定,故B错误;
C.电子层越多,原子半径越大,同周期从左向右原子半径减小,则原子半径由大到小的顺序:Z、W、X、Y,故C错误;
D.WX与ZX中的化学键类型不同,分别为共价键、离子键,故D错误;
故选A.
点评 本题考查原子结构与元素周期律,为高频考点,把握原子结构、原子序数、元素的位置来推断元素为解答的关键,侧重分析与应用能力的考查,X、Y为推断的难点,注意规律性知识的应用,注重思维的严密性训练,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | ①②③④ | B. | ①②④ | C. | ①② | D. | ①③ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Ca(HCO3)2溶液与足量NaOH溶液反应:Ca2++2HCO3-+2OH-═CaCO3↓+CO32-+H2O | |
| B. | NaHSO4溶液与Ba(OH)2溶液反应至中性:2H++SO42-+Ba2++2OH-═BaSO4↓+2H2O | |
| C. | 过量SO2通入到NaClO溶液中:SO2+H2O+ClO-═HClO+HSO3- | |
| D. | NaAlO2溶液和过量的HCl溶液反应:AlO2-+H++H2O═Al(OH)3↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. |  用图所示装置可比较硫、碳、硅三种元素的非金属性强弱 | |
| B. |  用图所示装置可降低金属铁的腐蚀速率 | |
| C. |  用图所示装置可测量强酸强碱的中和热 | |
| D. |  用图所示装置可制备Fe(OH)2并能较长时间观察其颜色 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢氧化钡与稀硫酸反应:H++OH-═H2O | |
| B. | 澄清的石灰水与稀盐酸反应:Ca(OH)2+2H+═Ca2++2H2O | |
| C. | 碳酸氢钠溶液与少量石灰水反应:HCO3-+Ca2++OH-═CaCO3↓+H2O | |
| D. | Ba(OH)2与少量NaHSO4溶液混合:Ba2++OH-+H++SO42-═BaSO4↓+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
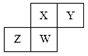 短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,其中W原子的质子数是其最外层电子数的三倍,下列说法不正确的是( )
短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,其中W原子的质子数是其最外层电子数的三倍,下列说法不正确的是( )| A. | 原子半径:Z>W>X>Y | |
| B. | 最高价氧化物对应水化物的酸性:X>W>Z | |
| C. | 最简单气态氢化物的热稳定性:Y>X>W>Z | |
| D. | 沸点:XH3<WH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 离子半径:Ca2+>Cl->S2- | B. | 第一电离能:Si>C>N | ||
| C. | 电负性:F>S>Mg | D. | 热稳定性:CH4>H2S>NH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 四种元素原子半径大小为:X>Y>Z>W | |
| B. | 氧化物的水化物的酸性:Z>W | |
| C. | W与Y可形成一种硬度很大的化合物 | |
| D. | W、X、Y三种元素均可以与Z元素形成共价化合物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com