
【题目】下列有关实验操作的说法正确的是( )。
A. 可用25mL碱式滴定管量取20.00mL KMnO4溶液
B. 用pH试纸测定溶液的pH时,需先用蒸馏水润湿试纸
C. 将金属钠在研钵中研成粉末,使钠与水反应的实验更安全
D. 蒸馏时蒸馏烧瓶中液体的体积不能超过容积的![]() ,液体也不能蒸干
,液体也不能蒸干
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】纳米ZnO在催化、医药及橡胶等新材料方面有广阔的应用前景,下面是制备纳米ZnO的相关工艺流程,试回答有关问题:
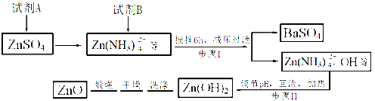
已知:Ksp[Zn(OH)2]=4.5×10-17,且Zn(OH)2具有两性。
(1) 试剂A是_____,试剂B是______,步骤I生成BaSO4的离子方程式是 。
(2)步骤II中,pH应调节至 (填序号)。
a.3~5 b.5 c.8~9 d.12~14
(3)步骤II中“回流”时必须用到下列仪器中的 (填序号)。
a.分液漏斗 b.温度计 c.空气冷凝管 d.球形冷凝管
(4)已知,在实验室中用200 mL 0.25 mol/L ZnSO4溶液与50 mL 8mol/L的试剂A反应,则加入固体试剂B的质量为 (计算结果保留小数点后一位)。
(5)步骤II在加热回流的同时,要蒸出 (填物质名称),该物质可循环使用。
(6)纳米ZnO也可以用以下流程制备(其中反应②生成了两种碳的化合物)。
![]() 书写相关的化学方程式① ,② 。
书写相关的化学方程式① ,② 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2015年,我国科学家屠呦呦因发现青蒿素而荣获诺贝尔奖。由青蒿素合成衍生药物蒿甲醚的合成路线如下:下列说法正确的是( )
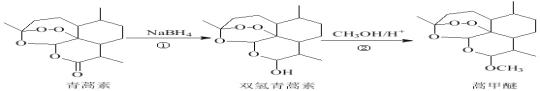
A.①、②反应依次为还原反应、取代反应
B.上述三种有机物的含氧官能团完全相同
C.青蒿素因含酯基具有氧化性和杀菌功能
D.蒿甲醚的化学式为C16H24O5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】无水三氯化铁易升华,有强烈的吸水性,是一种用途比较广泛的盐。
(1)实验室中可将FeCl3溶液 、 、过滤、洗涤干燥得FeCl3·6H2O;再 ,得到无水FeCl3。
(2)室温时在FeCl3溶液中滴加NaOH溶液,当溶液pH为2.7时,Fe3+开始沉淀;当溶液pH为4时,c(Fe3+)= mol·L-1(已知:Ksp[Fe(OH)3]= 1.1×10-36)。
(3)利用工业FeCl3制取纯净的草酸铁晶体[Fe2(C2O4)3·5H2O]的实验流程如下图所示:
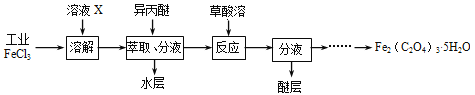
①为抑制FeCl3水解,溶液X为 。
②上述流程中FeCl3能被异丙醚萃取,其原因是 ;检验萃取、分液后所得水层中是否含有Fe3+的方法是 。
③所得Fe2(C2O4)3·5H2O需用冰水洗涤,其目的是 。
④为测定所得草酸铁晶体的纯度,实验室称取a g样品,加硫酸酸化,用KMnO4标准溶液滴定生成的H2C2O4,KMnO4标准溶液应置于右图所示仪器 (填“甲”或“乙”)中;下列情况会造成实验测得Fe2(C2O4)3·5H2O含量偏低的是 。
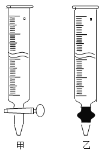
a.盛放KMnO4的滴定管水洗后未用标准液润洗
b.滴定管滴定前尖嘴部分有气泡,滴定后消失
c.滴定前仰视读数,滴定后俯视读数
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高分子材料PET聚酯树脂和PMMA的合成路线如下:

已知:
Ⅰ.R1COOR2+ R318OH![]() R1CO18OR3+R2OH(R1、R2、R3代表烃基)
R1CO18OR3+R2OH(R1、R2、R3代表烃基)
![]() Ⅱ.
Ⅱ. (R4、R5代表烃基)
(R4、R5代表烃基)
(1)①的反应类型是 。
(2)②的化学方程式为 。
(3)PMMA单体的官能团名称是 、 。
(4)F的核磁共振氢谱显示只有一组峰,⑤的化学方程式为 。
(5)G的结构简式为 。
(6)下列说法正确的是 (填字母序号)。
a.⑦为酯化反应
b.B和D互为同系物
c.1 mol  与足量NaOH溶液反应时,最多消耗4 mol NaOH
与足量NaOH溶液反应时,最多消耗4 mol NaOH
(7)J的某种同分异构体与J具有相同官能团,且为顺式结构,其结构简式是 。
(8)写出由PET单体制备PET聚酯并生成B的化学方程式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.氢能的存储是氢能应用的主要瓶颈,配位氢化物、富氢载体化合物是目前所采用的主要储氢材料。
(1)Ti(BH4)2是一种过渡元素硼氢化物储氢材料。在基态Ti2+中,电子占据的最高能层符号为 ,该能层具有的原子轨道数为 。
(2)液氨是富氢物质,是氢能的理想载体,利用![]() 2NH3实现储氢和输氢。下列说法正确的是 。
2NH3实现储氢和输氢。下列说法正确的是 。
a.NH3分子中氮原子的轨道杂化方式为sp2杂化 b.电负性顺序:C<N<O<F
c.由于氨分子间存在氢键,所以稳定性:NH3>PH3 d.[Cu(NH3)4]2+中N原子是配位原子
(3)已知NF3与NH3的空间构型相同,但NF3不易与Cu2+形成配离子,其原因是 。
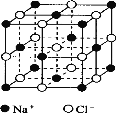
Ⅱ.氯化钠是生活中的常用调味品,也是结构化学中研究离子晶体时常用的代表物,其晶胞结构如图所示:
(1)设氯化钠晶体中Na+与跟它最近邻的Cl-之间的距离为r,则该Na+与跟它次近邻的Cl-的个数为 ,该Na+与跟它次近邻的Cl-之间的距离为 。
(2)已知在氯化钠晶体中Na+的半径为a pm,Cl-的半径为b pm,它们在晶体中是紧密接触的,则在氯化钠晶体中离子的空间利用率为 (用含a、b的式子表示)。
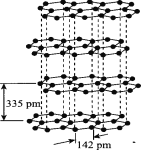
(3)硅与碳是同主族元素,其中石墨为混合型晶体,已知石墨的层间距为335 pm,C--C键长为142 pm,则石墨晶体密度约为 (列式并计算,结果保留三位有效数字,NA为6.02×1023 mol-)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氧化锰是常用的催化剂、氧化剂和活性电极材料。海底蕴藏着丰富的锰结核矿,其主要成分是MnO2。1991年由Allen等人研究,用硫酸淋洗后使用不同的方法可制备纯净的MnO2,其制备过程如下图所示:

已知:反应Ⅱ以石墨为电极,电解硫酸锰溶液制二氧化锰;反应Ⅲ可以是高锰酸钾氧化硫酸锰,也可以是氯酸钾氧化硫酸锰。下列推断不正确的是( )
A.反应Ⅰ的离子方程式为MnO2+H2O2+2H+===Mn2++2H2O+O2↑
B.反应Ⅱ中阴极反应式为Mn2+-2e-+2H2O===MnO2↓+4H+
C.若加入KClO3,则反应Ⅲ为2ClO+5Mn2++4H2O===5MnO2↓+Cl2↑+8H+
D.若加入KMnO4,则反应Ⅲ为3Mn2++2MnO+2H2O===5MnO2↓+4H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素W、X、Y、Z在元素周期表中的位置如图所示。下列说法中正确的是( )
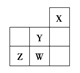
A. Y的原子半径在同周期主族元素中最大
B. W的非金属性比Z的弱
C. Z的气态氢化物的稳定性在同主族元素中最强
D. W的最高价氧化物对应的水化物是强酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物A分子中含苯环,相对分子质量136,分子中碳、氢原子个数相等,其含碳质量分数为70.6%,其余为氧、氢。
(1)A的分子式是__________________。
(2)若A分子中能发生银镜反应,且有弱酸性,则A的同分异构体有_______种,请任写一种符合条件的A的结构简式: 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com