
【题目】现有四种短周期元素A,B,C,D,已知:①C,D在同一周期,A,B在同一主族;②它们可以组成化合物A2C、B2C2、DC2、D2A4等;③B的阳离子与C的阴离子的核外电子排布相同;④B2C2同A2C或DC2反应都生成气体C2,B与A2C反应生成气体A2,A2与气体C2按体积比2∶1混合后点燃发生爆炸,其产物是一种常温下常见的无色无味的液体。请回答:
(1)写出元素符号:A________、B________、C________、D________。
(2)在A2C、B2C2、DC2和D2A4中,同时含有离子键和非极性共价键的化合物的电子式为__________;按原子轨道重叠方式,其非极性键的类型是________。化合物DC2的结构式__________。
(3)A2C分子的电子式____________,按原子轨道重叠方式,其共价键的类型是____________。D2A4是平面形分子,其分子中含有______个σ键,______个π键。
(4)写出化学方程式或离子方程式:
B2C2与A2C反应的化学方程式:___________________________________________;
B2C2与DC2反应的化学方程式:___________________________________________;
B与A2C反应的离子方程式:______________________________________________。
【答案】H Na O C ![]() ppσ键 O=C=O
ppσ键 O=C=O ![]() spσ键 5 1 2Na2O2+2H2O=4NaOH+O2↑ 2Na2O2+2CO2=2Na2CO3+O2 2Na+2H2O=2Na++2OH-+H2↑
spσ键 5 1 2Na2O2+2H2O=4NaOH+O2↑ 2Na2O2+2CO2=2Na2CO3+O2 2Na+2H2O=2Na++2OH-+H2↑
【解析】
根据题中信息可知:气体A2与C2按体积比2:1混合后点燃发生爆炸,其产物是一种常温下常见的无色无味的液体可知该液体为H2O,则A为H元素,C为O元素;B与H2O生成气体H2,B与A同一主族又是短周期元素,B的阳离子与C的阴离子的核外电子排布相同,则B为Na元素,DC2能与Na2O2反应生成O2,则D为C元素。
(1)A的元素符号为H;B的元素符号为Na;C的元素符号为O;D的元素符号为C;答案:H 、 Na 、O、 C。
(2)A2C为H2O,B2C2为Na2O2,DC2为CO2,D2A4为C2H4,则既有离子键又有非极性共价键的是Na2O2,其电子式为![]() ;由于其非极性键是O-O,是由O原子的p轨道上的单电子配对形成的共价键则为p-p σ键;DC2为CO2,其结构式为O=C=O;答案:
;由于其非极性键是O-O,是由O原子的p轨道上的单电子配对形成的共价键则为p-p σ键;DC2为CO2,其结构式为O=C=O;答案:![]() 、 ppσ键、 O=C=O。
、 ppσ键、 O=C=O。
(3)A2C为H2O,其电子式为![]() ,由H的s轨道单电子与O的p轨道单电子配对形成共价键为s-p σ键;C2H4分子中,C-H均为σ键,C=C中有一个σ键,一个π键,故其分子中含有5个σ键,1个π键;答案:s-p σ、5 、1。
,由H的s轨道单电子与O的p轨道单电子配对形成共价键为s-p σ键;C2H4分子中,C-H均为σ键,C=C中有一个σ键,一个π键,故其分子中含有5个σ键,1个π键;答案:s-p σ、5 、1。
(4)Na2O2与H2O反应生成NaOH和O2,反应的化学方程式为:2Na2O2+2H2O=4NaOH+O2↑;Na2O2与CO2反应生成Na2CO3和O2,反应的化学方程式为:2Na2O2+2CO2=2Na2CO3+O2;Na与H2O反应的离子方程式为:2Na+2H2O=2Na++2OH-+H2↑。答案:2Na2O2+2H2O=4NaOH+O2↑ 、 2Na2O2+2CO2=2Na2CO3+O2 、2Na+2H2O=2Na++2OH-+H2↑。


科目:高中化学 来源: 题型:
【题目】下列叙述中,正确的是
A. H2SO4的摩尔质量是98
B. 等质量的O2和O3中所含的氧原子数相同
C. 等质量的CO与CO2中所含碳原子数之比为7︰11
D. 98g H2SO4溶解于500mL水中,所得溶液中硫酸的物质的量浓度为2 mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】绚丽多彩的无机颜料的应用曾创造了古代绘画和彩陶的辉煌。硫化镉(CdS)是一种难溶于水的黄色颜料,其在水中的沉淀溶解平衡曲线如图所示。下列说法错误的是
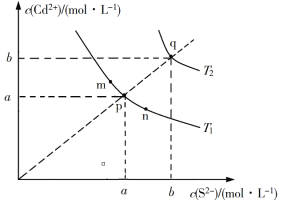
A. 图中a和b分别为T1、T2温度下CdS在水中的溶解度
B. 图中各点对应的Ksp的关系为:Ksp(m)=Ksp(n)<Ksp(p)<Ksp(q)
C. 向m点的溶液中加入少量Na2S固体,溶液组成由m沿mpn线向p方向移动
D. 温度降低时,q点的饱和溶液的组成由q沿qp线向p方向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,![]() 和
和![]() 的电离常数分别为
的电离常数分别为![]() 和
和![]() 。将
。将![]() 和体积均相同的两种酸溶液分别稀释,其
和体积均相同的两种酸溶液分别稀释,其![]() 随加水体积的变化如图所示。下列叙述正确的是( )
随加水体积的变化如图所示。下列叙述正确的是( )

A. 曲线Ⅰ代表![]() 溶液
溶液
B. 溶液中水的电离程度:b点>c点
C. 从c点到d点,溶液中 保持不变(其中
保持不变(其中![]() 、
、![]() 分别代表相应的酸和酸根离子)
分别代表相应的酸和酸根离子)
D. 相同体积a点的两溶液分别与![]() 恰好中和后,溶液中
恰好中和后,溶液中![]() 相同
相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】多晶硅是制作光伏电池的关键材料。以下是由粗硅制备多晶硅的简易过程。

回答下列问题:
Ⅰ.硅粉与![]() 在300℃时反应生成
在300℃时反应生成![]() 气体和
气体和![]() ,放出
,放出![]() 热量,该反应的热化学方程式为________________________。
热量,该反应的热化学方程式为________________________。![]() 的电子式为__________________。
的电子式为__________________。
Ⅱ.将![]() 氢化为
氢化为![]() 有三种方法,对应的反应依次为:
有三种方法,对应的反应依次为:
①![]()
![]()
②![]()
![]()
③![]()
![]()
(1)氢化过程中所需的高纯度![]() 可用惰性电极电解
可用惰性电极电解![]() 溶液制备,写出产生
溶液制备,写出产生![]() 的电极名称______(填“阳极”或“阴极”),该电极反应方程式为________________________。
的电极名称______(填“阳极”或“阴极”),该电极反应方程式为________________________。

(2)已知体系自由能变![]() ,
,![]() 时反应自发进行。三个氢化反应的
时反应自发进行。三个氢化反应的![]() 与温度的关系如图1所示,可知:反应①能自发进行的最低温度是____________;相同温度下,反应②比反应①的
与温度的关系如图1所示,可知:反应①能自发进行的最低温度是____________;相同温度下,反应②比反应①的![]() 小,主要原因是________________________。
小,主要原因是________________________。
(3)不同温度下反应②中![]() 转化率如图2所示。下列叙述正确的是______(填序号)。
转化率如图2所示。下列叙述正确的是______(填序号)。
a.B点:![]() b.
b.![]() :A点
:A点![]() 点 c.反应适宜温度:
点 c.反应适宜温度:![]() ℃
℃
(4)反应③的![]() ______(用
______(用![]() ,
,![]() 表示)。温度升高,反应③的平衡常数
表示)。温度升高,反应③的平衡常数![]() ______(填“增大”、“减小”或“不变”)。
______(填“增大”、“减小”或“不变”)。
(5)由粗硅制备多晶硅过程中循环使用的物质除![]() 、
、![]() 和
和![]() 外,还有______(填分子式)。
外,还有______(填分子式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金晶体的最小重复单元(也称晶胞)是面心立方体,如图所示,即在立方体的8个顶点各有一个金原子,各个面的中心有一个金原子,每个金原子被相邻的晶胞所共有。金原子的直径为d,用NA表示阿伏加德罗常数,M表示金的摩尔质量。请回答下列问题:

(1)金晶体每个晶胞中含有________个金原子。
(2)欲计算一个晶胞的体积,除假定金原子是刚性小球外,还应假定_______________。
(3)一个晶胞的体积是____________。
(4)金晶体的密度是____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学小组用如下方法测定经处理后的废水中苯酚的含量(废水中不含干扰测定的物质)。
Ⅰ.用已准确称量的KBrO3固体配制一定体积的a mol·L1 KBrO3标准溶液;
Ⅱ.取v1 mL上述溶液,加入过量KBr,加HSO4酸化,溶液颜色呈棕黄色;
Ⅲ.向Ⅱ所得溶液中加入v2 mL废水;
Ⅳ.向Ⅲ中加入过量KI;
Ⅴ.用b mol·L1 Na2S2O3标准溶液滴定Ⅳ中溶液至浅黄色时,滴加2滴淀粉溶液,继续滴定至终点,共消耗Na2S2O3溶液v2 mL。
已知:I2+2Na2S2O3=2NaI+ Na2S4O6
Na2S2O3和Na2S4O6溶液颜色均为无色
(1)Ⅰ中配制溶液用到的玻璃仪器有烧杯、玻璃棒、胶头滴管和____________。
(2)Ⅰ中发生反应的离子方程式是_______________________________。
(3)Ⅲ中发生反应的化学方程式是_________________________________。
(4)Ⅳ中加KI前,溶液颜色须为黄色,原因是______________________________。
(5)KI与KBrO3物质的量关系为n(KI)≥6n(KBrO3)时,KI一定过量,理由是________。
(6)Ⅴ中滴定至终点的现象是_____________________________。
(7)废水中苯酚的含量为___________g·L1(苯酚摩尔质量:94 g·mol 1)。
(8)由于Br2具有____________性质,Ⅱ~Ⅳ中反应须在密闭容器中进行,否则会造成测定结果偏高。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列指定反应的离子方程式正确的是
A. 室温下用稀NaOH溶液吸收Cl2:Cl2+2OH![]() ClO+Cl+H2O
ClO+Cl+H2O
B. 用铝粉和NaOH溶液反应制取少量H2:Al+2OH![]()
![]() +H2↑
+H2↑
C. 室温下用稀HNO3溶解铜:Cu+2![]() +2H+
+2H+![]() Cu2++2NO2↑+H2O
Cu2++2NO2↑+H2O
D. 向Na2SiO3溶液中滴加稀盐酸:Na2SiO3+2H+![]() H2SiO3↓+2Na+
H2SiO3↓+2Na+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组欲选用下列装置和药品制取纯净乙炔并进行有关乙炔性质的探究,试回答下列问题。

(1)A中制取乙炔的化学方程式为_______________________________________________。
(2)制乙炔时,旋开分液漏斗的活塞,使水缓慢滴下的原因是________________________,分液漏斗里的液体通常用___________________。
(3)用电石制得的乙炔中常含有H2S、PH3等杂质,除去杂质应选用________(填字母,下同)装置,气体应从________进;干燥乙炔最好选用________装置。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com