
【题目】A、B、C、D是元素周期表中前36号元素,它们的核电荷数依次增大。第二周期元素A原子的核外成对电子数是未成对电子数的2倍且有3个能级,B原子的最外层p轨道的电子为半充满结构,C是地壳中含量最多的元素。D是第四周期元素,其原子核外最外层电子数与氢原子相同,其余各层电子均充满。请回答下列问题:
(1)A、B、C的第一电离能由小到大的顺序是________(用对应的元素符号表示);基态D原子的价电子排布式为______________________。
(2)A的最高价氧化物分子中,其中心原子采取________杂化;BC3-的立体构型为________(用文字描述)。
(3)1 mol AB-中含有的π键个数为________。
(4)化合物CH3COO[Cu(NH3)3·CO]中与Cu+形成配离子的配体为____________(填化学式)。
(5) CH3COOH中C原子杂化轨道类型为_________________。
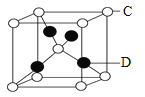
(6)元素D与元素C形成一种化合物其晶胞结构如图所示,该化合物的化学式为______.
【答案】C<O<N 1s22s22p63s23p63d104s1 sp 平面三角形 2NA NH3和CO sp3、sp2 Cu2O
【解析】
A、B、C、D是元素周期表中前36号元素,它们的核电荷数依次增大;第二周期元素A原子的核外成对电子数是未成对电子数的2倍且有3个能级,则A是C元素;C是地壳中含量最多的元素,则C是O元素;B原子的最外层p轨道的电子为半充满结构,且原子序数大于A而小于C,则B是N元素;D是第四周期元素,其原子核外最外层电子数与氢原子相同,其余各层电子均充满,则D是Cu元素,据此分析解题。
由分析知:A为C元素、B为N元素、C为O元素、D是Cu元素;
(1)同一周期元素,元素第一电离能随着原子序数增大而增大,但第IIA族、第VA族元素第一电离能大于其相邻元素,所以C、N、O元素第一电离能从小到大顺序是C<O<N;基态D原子核外有29个电子,根据构造原理可知基态Cu原子的电子排布式为1s22s22p63s23p63d104s1;
(2)A的最高价氧化物为CO2,C和O形成2个δ键,没有孤电子对,为直线形结构,C原子采取sp方式杂化;NO3-中心原子N价层电子对个数=3+![]() =3,且不含孤电子对,为sp2杂化,立体构型为平面三角形;
=3,且不含孤电子对,为sp2杂化,立体构型为平面三角形;
(3)CN-与N2互为等电子体,则每个CN-中含有2个π键,则1mol CN-中含有的π键个数为2NA;
(4) 化合物CH3COO[Cu(NH3)3CO]中与Cu+形成配离子的配体为NH3和CO;
(5) CH3COOH中CH3-上的C原子形成4个共价键,则采用sp3杂化,羧基上碳原子形成3个共价键,且无孤对电子,则采用sp2杂化;
(6)元素D为Cu,晶胞中Cu个数为4,C元素为O,O原子个数为8×![]() +1=2,Cu与O的原子数目比为4:2=2:1,则该化合物的化学式为Cu2O。
+1=2,Cu与O的原子数目比为4:2=2:1,则该化合物的化学式为Cu2O。


 优等生题库系列答案
优等生题库系列答案科目:高中化学 来源: 题型:
【题目】金刚烷是一种是重要的化工原料,工业上可通过下列途径制备:

(1)环戊二烯分子中最多有________个原子共面。
(2)金刚烷的分子式为________,其分子中的CH2基团有________个;
(3)下面是以环戊烷为原料制备环戊二烯的合成路线

其中,反应①还需要的反应试剂是______,反应类型是____,反应③的反应类型是_________;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E是五种短周期主族元素,其中A是元素周期表中原子半径最小的元素;B是形成化合物种类最多的元素;C是地壳中含量最多的元素;D的气态氢化物的水溶液显碱性;E金属制成金属板后,经加工可制成一种高质量的反光镜,该金属粉末和氧化铁混合常用于焊接钢轨.
(1)写出C、E的元素符号______、______。
(2)B元素位于周期表中的位置为______,BC2的电子式为______(用元素符号表示)。
(3)A、B、C、D的原子半径由大到小的顺序为______(用元素符号表示)。
(4)E的最高价氧化物对应的水化物与短周期元素中最高价氧化物对应水化物碱性最强的物质在溶液中反应的离子方程式______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铜是人类最早使用的金属之一,其单质及化合物具有广泛的用途。
(1)基态铜原子核外有________对自旋相反的电子。
(2)青铜是铜与锡或铅等元素按一定比例熔铸而成的合金。第一电离能I1(Sn)____________I1(Pb)(填“大于”或“小于”)。
(3)新制的Cu(OH)2能够溶解于浓氨水中,反应的离子方程式是____________________________________;
(4)利用铜片表面催化反应,我国研究人员用六炔基苯为原料,在世界上首次通过化学方法获得全碳材料—石墨炔薄膜(结构片段如图所示),开辟了人工化学合成碳同素异形体的先例。石墨炔中碳原子_________________________的杂化方式。

(5)CuCl的盐酸溶液能吸收CO形成氯化羰基亚铜(I),可用于定量测定气体混合物中CO的含量。氯化羰基亚铜(I)中含___________σ键数目。
(6)Cu2O可用于半导体材料。
①Cu2O晶胞(如图所示)中,O原子的配位数为________________;a位置Cu+坐标为(0.25,0.25,0.75),则b位置Cu+坐标_______________________。
②Cu2S与Cu2O具有相似晶体结构,则两者的熔点是Cu2O比Cu2S的_________(填“高”或“低”),请解释原因___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高温下超氧化钾晶体呈立方体结构,晶体中氧的化合价部分为0价,部分为2价.如图所示为超氧化钾晶体的一个晶胞(晶体中最小的重复单元),则下列说法中正确的是( )
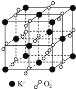
A. 超氧化钾的化学式为KO2,每个晶胞含有4个K+和4个O2-
B. 晶体中每个K+周围有8个O2-,每个O2-周围有8个K+
C. 晶体中与每个K+距离最近的K+有8个
D. 晶体中,0价氧与2价氧的数目比为2:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫及其化合物有许多用途。相关物质的物理常数如表所示:
H2S | S8 | FeS2 | SO2 | SO3 | H2SO4 | |
熔点/℃ | -85.5 | 115.2 | >600(分解) | 75.5 | 16.8 | 10.3 |
沸点/℃ | -60.3 | 444.6 | -10.0 | 45.0 | 337.0 |
回答下列问题:
(1)基态Fe原子价层电子的电子排布图(轨道表达式)为______,基态S原子电子占据最高能级的电子云轮廓图为______形。
(2)根据价层电子对互斥理论,H2S,SO2,SO3的气态分子中,中心原子价层电子对数不同于其他分子的是______。
(3)图(a)为S8的结构,其熔点和沸点要比二氧化硫的熔点和沸点高很多,主要原因为____。
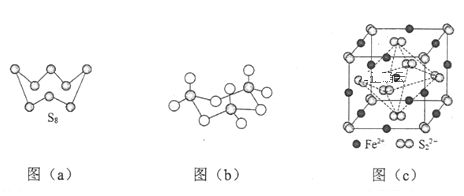
(4)气态三氧化硫以单分子形式存在,其分子的立体构型为______形,其中共价键的类型有______种;固体三氧化硫中存在如图(b)所示的三聚分子。该分子中S原子的杂化轨道类型为______。
(5)FeS2晶体的晶胞如图(c)所示,该晶胞中FeS2个数___________,晶胞边长为anm,FeS2相对式量为M、阿伏加德罗常数的值为NA,其晶体密度的计算表达式为_____g/cm3.(写出表达式) ;晶胞中Fe2+位于S22-所形成的八面体的体心,该正八面体的边长为______nm。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】胃舒平主要成分是氢氧化铝,同时含有三硅酸镁(![]() )等化合物。
)等化合物。
(1)铝单质与同周期中非金属性最强的元素的气态氢化物的水溶液之间发生反应的离子方程式为:____________
(2)某元素与铝元素同周期且原子半径比镁原子半径大,写出该元素符号______,该元素的最高价氧化物的水化物与铝元素的最高价氧化物的水化物之间发生反应的离子方程式为:______________
(3)![]() 、MgO和
、MgO和![]() 都可以制耐火材料,其原因是______
都可以制耐火材料,其原因是______
a. ![]() 、MgO和
、MgO和![]() 都是白色固体
都是白色固体
b. ![]() 、MgO和
、MgO和![]() 都是氧化物
都是氧化物
c. ![]() 、MgO和
、MgO和![]() 都有很高的熔点
都有很高的熔点
(4)氢氧化铝在强酸溶液中的电离方程式________。
(5)明矾常用作净水剂,结合相关理论解释其净水原理__________。
(6)用于治疗胃酸过多的药物还有多种,请写出其中一种的化学式_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组中两种物质无论以何种比例混合,只要混合的总物质的量一定,则完全燃烧时生成水的质量和消耗O2的质量均不变的是( )
A.C3H6、C3H8OB.C2H4、C2H6O
C.CH4O、C2H4O3D.C2H2、C6H6
查看答案和解析>>
科目:高中化学 来源: 题型:
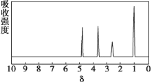
【题目】化合物A 经李比希法和质谱法分析得知其相对分子质量为 136,分子式为 C8H8O2。A 的核磁共振氢谱有 4 个峰且面积之比为 1:2:2:3,A 分子中只含一个苯环且苯环上只有一个取代基,其红外光谱与核磁共振氢谱如下图。关于A 的下列说法中,正确的是( )
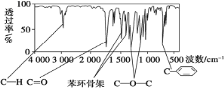
A.与 A 属于同类化合物的同分异构体只有 2 种
B.符合题中A 分子结构特征的有机物只有 1 种
C.A 分子属于酯类化合物,在一定条件下不能发生水解反应
D.A 在一定条件下可与 4molH2 发生加成反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com