
【题目】CH3OCH3(二甲醚)常用作有机合成的原料,也用作溶剂和麻醉剂。CO2与H2合成CH3OCH3涉及的相关热化学方程式如下:
Ⅰ.CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) ΔH1=-49.1kJ·mol-1
CH3OH(g)+H2O(g) ΔH1=-49.1kJ·mol-1
Ⅱ.2CH3OH(g)![]() CH3OCH3(g)+H2O(g) ΔH2=-24.5kJ·mol-1
CH3OCH3(g)+H2O(g) ΔH2=-24.5kJ·mol-1
Ⅲ.CO2(g)+H2(g)![]() CO(g)+H2(g) ΔH3
CO(g)+H2(g) ΔH3
Ⅳ.2CO2(g)+6H2(g)![]() CH3OCH3(g)+3H2O(g) ΔH4
CH3OCH3(g)+3H2O(g) ΔH4
回答下列问题:
⑴ΔH4=__kJ·mol-1。
⑵体系自由能变ΔG=ΔH-TΔS,ΔG<0时反应能自发进行。反应Ⅰ、Ⅱ、Ⅲ的自由能变与温度的关系如图a所示,在298~998K下均能自发进行的反应为__(填“Ⅰ”“Ⅱ”或“Ⅲ”)。
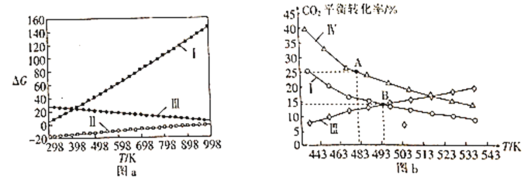
⑶在三个完全相同的恒容密闭容器中,起始时均通入3molH2和1molCO2,分别只发生反应Ⅰ、Ⅲ、Ⅳ时,CO2的平衡转化率与温度的关系如图b所示。
①ΔH3__0(填“>”或“<”)。
②反应Ⅳ,若A点总压强为pMPa,则A点时CO2的分压为p(CO2)__pMPa(精确到0.01)。
③在B点对应温度下, K(Ⅰ)__(填“大于”“小于”或“等于”)K(Ⅲ)。
⑷向一体积为1L的密闭容器中通入H2和CO2,只发生反应Ⅳ。CO2的平衡转化率与压强、温度及氢碳比m[m=![]() ]的关系分别如图c和图d所示。
]的关系分别如图c和图d所示。
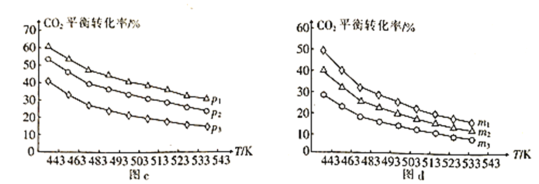
①图c中压强从大到小的顺序为__,图d中氢碳比m从大到小的顺序为__。
②若在1L恒容密闭容器中充入0.2molCO2和0.6molH2,CO2的平衡转化率为50%,则在此温度下该反应的平衡常数K=__(保留整数)。
【答案】-122.54 Ⅱ > 0.21 小于 p1>p2>p3 m1>m2>m3 23
【解析】
⑴第Ⅰ个方程式的2倍加上第Ⅱ个方程式。
⑵根据图中信息得到298~998K下只有Ⅱ的ΔG<0。
⑶①升高温度,CO2的平衡转化率增大,说明平衡正向移动,正向是吸热反应;②三段式式建立关系,根据公式求出压强;③根据平衡常数分析产物与反应物的关系。
⑷①利用转化率分析压强,利用一个量不变,另一个量变化来分析。
②建立三段式建立再求平衡常数。
⑴将第Ⅰ个方程式的2倍加上第Ⅱ个方程式得到ΔH4=-122.54 kJ·mol1;故答案为:-122.54。
⑵体系自由能变ΔG=ΔH-TΔS,ΔG<0时反应能自发进行,在298~998K下只有Ⅱ的ΔG<0,因此均能自发进行的反应为Ⅱ;故答案为:Ⅱ。
⑶①升高温度,CO2的平衡转化率增大,说明平衡正向移动,正向是吸热反应,即ΔH3>0;故答案为:>。
②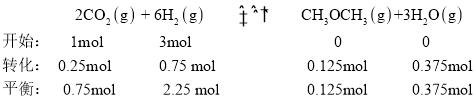 ,反应Ⅳ,若A点总压强为pMPa,则A点时CO2的分压为
,反应Ⅳ,若A点总压强为pMPa,则A点时CO2的分压为![]() ;故答案为:0.21。
;故答案为:0.21。
③在B点对应温度下,根据Ⅰ.CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g)和Ⅲ.CO2(g)+H2(g)
CH3OH(g)+H2O(g)和Ⅲ.CO2(g)+H2(g)![]() CO(g)+H2(g)的反应,CO2转化率相等,产物的量相等,但Ⅰ中氢气平衡时量较少,但是大于1的值,由于是浓度三次方,因此平衡常数小,平衡常数K(Ⅰ)小于K(Ⅲ);故答案为:小于。
CO(g)+H2(g)的反应,CO2转化率相等,产物的量相等,但Ⅰ中氢气平衡时量较少,但是大于1的值,由于是浓度三次方,因此平衡常数小,平衡常数K(Ⅰ)小于K(Ⅲ);故答案为:小于。
⑷①该反应是体积减小的反应,图c中定温度,从下到上看,转化率增大,说明平衡正向移动,向体积减小方向移动即加压,压强从大到小的顺序为p1>p2>p3,图d中可以理解为二氧化碳物质的量不变,氢气量不断增加,平衡正向移动,二氧化碳转化率不断增大,因此氢碳比m从大到小的顺序为m1>m2>m3;故答案为:m1>m2>m3。
②若在1L恒容密闭容器中充入0.2molCO2和0.6molH2,CO2的平衡转化率为50%, ,则在此温度下该反应的平衡常数
,则在此温度下该反应的平衡常数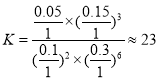 ;故答案为:23。
;故答案为:23。


 新题型全程检测期末冲刺100分系列答案
新题型全程检测期末冲刺100分系列答案科目:高中化学 来源: 题型:
【题目】常温下,在27.5 g水中溶解12.5 g CuSO45H2O,恰好达到饱和,该溶液密度为1.18 g·cm-3,求:
(1)该溶液中阴阳离子的总物质的量._________________
(2)该溶液中CuSO4的物质的量浓度(保留二位小数)。________________
(3)取出20.0 mL该溶液,加入足量Ba(OH)2溶液,反应后可得到沉淀质量多少克?(保留一位小数)____________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有标准状况下四种气体①8.96L![]() ; ②
; ②![]() 个
个![]() ; ③30.6g
; ③30.6g![]() ; ④
; ④![]() 。下列关系从小到大表示不正确的是( )
。下列关系从小到大表示不正确的是( )
A.体积:④<①<②<③B.密度:①<④<③<②
C.质量:④<①<③<②D.氢原子数:②<④<①<③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】盐酸是中学化学常用的试剂,以下两个实验均和盐酸有关。
I.用密度为1.25 g·mL-1,质量分数36.5%的浓盐酸配制500 mL 0.20 mol·L-1盐酸溶液,请回答下列问题:
(1)浓盐酸的物质的量浓度为____________。
(2)配制500 mL 0.20 mol·L-1盐酸需要用量筒量取上述浓盐酸_______mL。
(3)对配制的盐酸测定,发现物质的量浓度小于0.2 mol·L-1,引起该误差的操作___(填序号)
A.容量瓶用蒸馏水洗涤后未干燥,含有少量蒸馏水
B.用量筒量取浓盐酸时,仰视刻度线量取浓盐酸
C.定容时,仰视容量瓶刻度线进行定容
D.定容后,把容量瓶倒置摇匀后发现液面低于刻度线,又滴加水至刻度处
Ⅱ.某学生设计如下图所示的实验装置,利用浓盐酸与高锰酸钾反应产生的氯气与熟石灰反应制取少量漂白粉,并探究氯、溴、碘的相关性质。请回答下列问题:

(4)A装置名称为________。
(5)漂白粉将在C装置的U形管中产生,写出生成漂白粉的化学方程式_______________。
(6)E装置中装有KI与CCl4混合液,向D中缓缓通入一定量氯气后,打开D装置中活塞,将D中少量溶液滴加入E装置中,振荡,观察到下层呈紫红色,由此得出结论:Br2置换出了I2,有同学对该结论提出异议,可能的理由是__________________________。
(7)F装置的作用是_____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于平衡常数K的说法中,正确的是( )
A. 在任何条件下,化学平衡常数K是一个恒定值
B. 平衡常数K只与温度有关,与反应物浓度、压强无关
C. 从平衡常数K的大小不能推断一个反应进行的程度
D. 对于可逆反应C(s)+H2O(g) ![]() CO(g)+H2(g)在一定温度下达到平衡时,其平衡常数表达式为
CO(g)+H2(g)在一定温度下达到平衡时,其平衡常数表达式为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】50 mL 0.50 mol·L-1盐酸与50 mL 0.55 mol·L-1 NaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热。回答下列问题。

(1)从实验装置上看,图中有一处仪器未画出的是_____________________。
(2)在其他操作正确的前提下,提高中和热测定准确性的关键是____________。大烧杯上如不盖硬纸板,求得的中和热数值___(填“偏大”“偏小”或“无影响”)
(3)如用0.5 mol/L的盐酸与NaOH固体进行实验,则实验中测得的“中和热”数值将______(填“偏大”、“偏小”、“不变”);原因是___________________。
(4)用相同浓度和体积的氨水代替NaOH溶液进行上述实验,测得的生成1 mol液态水时放出热量的数值_______________(填“偏大”、“偏小”、“不变”)。
(5)实验中NaOH过量的目的是___________。
(6)若某同学利用上述装置做实验有些操作不规范,造成测得中和热偏小,请分析可能原因(________)。
A.测量盐酸的温度后,温度计没有用水冲洗干净
B.用量筒中的氢氧化钠溶液倒入小烧杯时动作缓慢
C.在量取盐酸时仰视读书
D.大烧杯的盖板中间小孔太大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】复旦大学王永刚的研究团队制得一种柔性水系锌电池,该可充电电池以锌盐溶液作为电解液,其原理如图所示。下列说法不正确的是( )
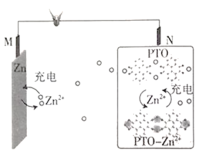
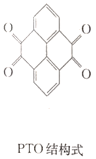
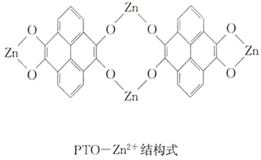
A.放电时,N极发生还原反应
B.充电时,Zn2+向M极移动
C.充电时,N极的电极反应式为2PTO+8e-+4Zn2+==PTO-Zn2+
D.放电时,每生成1molPTO-Zn2+,M极溶解![]() 的质量为260g
的质量为260g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国化工专家侯德榜的“侯氏制碱法”曾为世界制碱工业做出了突出贡献。他以NaCl、NH3、CO2等为原料先制得NaHCO3,进而生产出纯碱。有关反应的化学方程式为:NH3+CO2+H2O=NH4HCO3;NH4HCO3+NaCl=NaHCO3↓+NH4Cl;2NaHCO3![]() Na2CO3+CO2↑+H2O。
Na2CO3+CO2↑+H2O。
回答下列问题:
(1)碳酸氢铵与饱和食盐水反应,能析出碳酸氢钠晶体的原因是___(填字母标号)。
a.碳酸氢钠难溶于水
b.碳酸氢钠受热易分解
c.碳酸氢钠的溶解度相对较小,所以在溶液中首先结晶析出
(2)某探究活动小组根据上述制碱原理,进行碳酸氢钠的制备实验,同学们按各自设计的方案实验。
①一位同学将二氧化碳气体通入含氨的饱和食盐水中制备碳酸氢钠,实验装置如图所示(图中夹持、固定用的仪器未画出)。
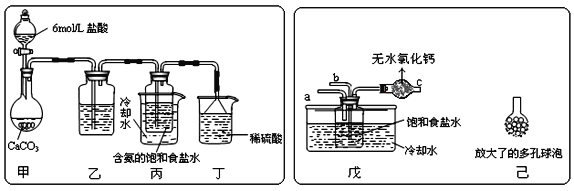
试回答下列有关问题:
(Ⅰ)乙装置中的试剂是___;
(Ⅱ)丁装置中稀硫酸的作用是___;
(Ⅲ)实验结束后,分离出NaHCO3晶体的操作是___(填分离操作的名称)。
②另一位同学用图中戊装置(其它装置未画出)进行实验。
(Ⅰ)实验时,须先从___管通入___气体,再从___管中通入___气体;
(Ⅱ)有同学建议在戊装置的b管下端连接己装置,理由是___;
(3)请你再写出一种实验室制取少量碳酸氢钠的方法:___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铜是重要的工业原材料,现有铜、氧化亚铜组成的混合物,某研究性学习小组为了探究其组成情况,取35.2 g混合物加入0.5 L 3.4 mol·L-1的稀硝酸,固体物质完全反应,生成一氧化氮4.48 L(标准状况)。向所得溶液中加入aL 2.0 mol·L-1氢氧化钠溶液,恰好使溶液中的铜离子沉淀完全。
(1)氧化亚铜与稀硝酸反应的化学方程式为_______________。
(2)混合物中,铜的物质的量为____________;氧化亚铜的物质的量为______________。
(3)所加氢氧化钠溶液的体积是____________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com