
| A. | 用pH试纸测氯水的pH | |
| B. | 保存液溴时液面覆盖一层水,并装在带玻璃塞的试剂瓶中 | |
| C. | 用稀盐酸清洗做过银镜反应的试管内壁 | |
| D. | 除去NaBr溶液中的NaI,可先加氯水,再用CCl4萃取分液 |
分析 A.氯气与水反应,发生Cl2+H2O=H++Cl-+HClO,氯水中含有HClO、Cl2,具有氧化性;
B.溴单质具有挥发性,需要用水液封,防止挥发,且溴能够氧化胶塞,应该用玻璃塞;
C.盐酸不与银单质反应,应该用稀硝酸清洗;
D.氯气能够以后溴离子和碘离子,应该用溴单质氧化.
解答 解:A.氯气可与水反应生成盐酸和次氯酸,其中盐酸可使pH变成红色,次氯酸具有强氧化性,可漂白试纸,最后使试纸变成白色,所以无法用PH试纸测氯水的PH值,故A错误;
B.保存液溴时液面覆盖一层水,可防止液溴挥发,另外溴具有强氧化性,不能使用胶塞,可装在带玻璃塞的试剂瓶中,故B正确;
C.由于稀盐酸不与银反应,无法洗去银单质,可用稀硝酸洗去,故C错误;
D.氯水能够将溴化钠氧化,应该用溴水,故D错误;
故选B.
点评 本题考查滴定操作方法、除杂方法、试剂的存放等知识,题目难度不大,明确常见物质的性质为解答关键,注意掌握pH试纸的使用方法、常见试剂的保存方法,试题培养了学生的灵活应用能力.


 名师点拨卷系列答案
名师点拨卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 将铁粉加入稀硫酸反中:2Fe+6H+═2Fe3++3H2↑ | |
| B. | 将铜屑加入氯化铁溶液中:Fe3++Cu═Cu2++Fe2+ | |
| C. | 将过量的石灰水加入小苏打溶液中:Ca2++OH-+HCO3-═CaCO3↓+H2O | |
| D. | 将氢氧化钡溶液滴加入稀硫酸中:Ba2++OH-+H++SO42-═BaSO4↓+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该物质属于氢氧化物 | |
| B. | 该物质的摩尔质量是160g•mol-1 | |
| C. | 该物质的碱性不强 | |
| D. | 将1molNaAl(OH)2CO3溶于足量1mol•L-1HCl中时,共收集到2.5molCO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 9种 | B. | 12种 | C. | 15种 | D. | 18种 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
物质 物质的量/mol 温度/℃ | NO | H2O |
| T1 | 1.6 | 2.4 |
| T2 | 1.2 | 1.8 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
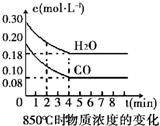 在850℃时发生如下反应:CO(g)+H2O(g)?CO2(g)+H2 (g)△H<0.CO和H2O浓度变化如右图,t℃(高于850℃)时,在相同容器中发生上述反应,容器内各物质的浓度变化如表.
在850℃时发生如下反应:CO(g)+H2O(g)?CO2(g)+H2 (g)△H<0.CO和H2O浓度变化如右图,t℃(高于850℃)时,在相同容器中发生上述反应,容器内各物质的浓度变化如表.| 时间(min) | CO | H2O | CO2 | H2 |
| 0 | 0.200 | 0.300 | 0 | 0 |
| 2 | 0.138 | 0.238 | 0.062 | 0.062 |
| 3 | C1 | C2 | C3 | C3 |
| 4 | C1 | C2 | C3 | C3 |
| 5 | 0.116 | 0.216 | 0.084 | |
| 6 | 0.096 | 0.266 | 0.104 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com