
 硫酸厂用煅烧黄铁矿(FeS2)制取硫酸,实验室利用硫酸厂烧渣(主要成分是Fe2O3及少量FeS、SiO2制备绿矾。
硫酸厂用煅烧黄铁矿(FeS2)制取硫酸,实验室利用硫酸厂烧渣(主要成分是Fe2O3及少量FeS、SiO2制备绿矾。
(一)SO2和O2反应制取的反应原理为:
2SO2+O2 2SO3,在一密闭容器中一定时间内达到平衡。
2SO3,在一密闭容器中一定时间内达到平衡。
(1)该反应的平衡常数表达式为______。
(2)该反应达到平衡状态的标志是______。
A.v(SO2)=v(SO3) B.混合物的平均相对分子质量不变
C.混合气体质量不变 D.各组分的体积分数不变
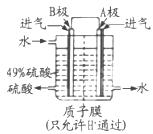
(二)某科研单位利用原电池原理,用SO2和O2制备硫酸,装置如图,电极为多孔的材料,能吸附气体,同时也能使气体与电解质溶液充分接触。
(3)B电极的电极反应式为______;溶液中H+的移动方向由______极到______极;电池总反应式为______。
(三)利用烧渣制绿矾的过程如下

测定绿矾产品中含量的实验步骤:
a.称取5.7 g产品,溶解,配成250 mL。溶液。
b.量取25 ml。待测液于锥形瓶中。
c.用硫酸酸化的0. 01 mol/LKMnO4 溶液滴定至终点,消耗KMnO4溶液体积40 mL。根据上述步骤同答下列问题。
(4)滴定时发生反应的离子方程式为(完成并配平离子反应方程式)。
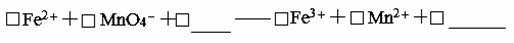
(5)用硫酸酸化的KMnO4滴定终点的标志是
(6)计算上述产品中的FeSO4.7H2O质量分数为______。
 课时训练江苏人民出版社系列答案
课时训练江苏人民出版社系列答案科目:高中化学 来源: 题型:
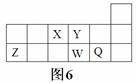 短周期元素X、Y、Z、W、Q在元素周期表中的相对位置如
短周期元素X、Y、Z、W、Q在元素周期表中的相对位置如
图6所示。下列说法不正确的是
A.离子半径的大小顺序为:r(W2—)>r(Q—)>r(Y2—)>r(Z3+)
B.元素W的最高价氧化物对应水化物的酸性比Q的强
C.元素X的氢化物与Q的氢化物化合的产物中既含共价键又含离子键
D.X、Z、W、Q四种元素的最高价氧化物对应水化物均能与强碱反应
查看答案和解析>>
科目:高中化学 来源: 题型:
我国的“神舟五号”载人飞船已发射成功,“嫦娥”探月工程也已正式启动。据科学家预测,月球的土壤中吸附着数百万吨的 ,每百吨
,每百吨 核聚变所释放出的能量相当于目前人类一年消耗的能量。在地球上,氮元素主要以
核聚变所释放出的能量相当于目前人类一年消耗的能量。在地球上,氮元素主要以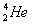 的形式存在。下列说法正确的是( )
的形式存在。下列说法正确的是( )
A.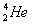 原子核内含有4个质子 B.
原子核内含有4个质子 B. 和
和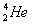 互为同位素
互为同位素
C. 原子核内含有3个中子
原子核内含有3个中子
D.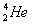 的最外层电子数为2,所以
的最外层电子数为2,所以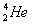 具有较强的金属性
具有较强的金属性
查看答案和解析>>
科目:高中化学 来源: 题型:
有5 种短周期元素的原子序数按E、D、B、A、C的顺序依次增大;A、C同周期,B、C同主族;A与B可形成离子化合物A2B,A2B中所有粒子的电子数相同,且电子总数为30;D和E可形成4核10电子的分子。试回答下列问题:
(1)写出五种元素的名称:A B C D E 。
(2)用电子式表示离子化合物A2B的形成过程:
(3)写出下列物质的电子式:
D元素形成的单质 ;B与E形成的化合物 ;
A、B、E形成的化合物 ;D、E形成的化合物 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是
A.0.1 mol/L溶液中的(NH4)2SO4,溶液中的c(NH4+)<c(SO42-)
B.相同温度下,0.6 mol/L氨水溶液与0.3 mol/l氨水溶液中c(OH-)之比是2:1
C.向0.1 mol/LNaNO3溶液中滴加硝酸使溶液pH=5,此时混合液中的c(Na+)<c(NO3-)
D.向醋酸钠溶液中加入适量醋酸,使混合液的pH=7,此时混合液中c(Na+)<c(CH3COO-)
查看答案和解析>>
科目:高中化学 来源: 题型:
用图所示装置进行下列实验,实验结果与预测的现象不一致的是
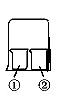
| ①中的物质 | ②中的物质 | 预测①的现象 | |
| A | 酚酞溶液 | 浓氨水 | 溶液变红色 |
| B | 酚酞溶液 | 浓硝酸 | 无明显变化 |
| C | 饱和CuSO4溶液 | 浓硫酸 | 无明显变化 |
| D | FeCl3溶液 | KSCN溶液 | 无明显变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验操作不正确的是( )
A.用盐酸酸化过的FeCl3溶液,除去H2还原CuO实验中留在试管内的铜
B.分液时,分液漏斗中下层液体从下口放出,上层液体从上口倒出
C.蒸馏时,将温度计的水银球靠近蒸馏烧瓶支管口
D.用稀硫酸洗涤长期存放石灰水的试剂瓶
查看答案和解析>>
科目:高中化学 来源: 题型:
NA代表阿伏加德罗常数,下列叙述错误的是( )
A.1mol任何物质所含有的原子数为NA
B.在H2O2+Cl2=2HCL+O2反应中,每生成32g氧气,则转移2NA个电子
C.标准状况下,分子数为NA的CO、C2H4混合气体体积约为22.4L,质量为28g
D.17克氨气所含的电子数为10NA
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:
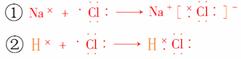
下列说法不正确的是
A.①和②变化过程中都会放出热量
B.氯原子吸引电子的能力强于钠原子和氢原子
C.①和②中的氯原子均得到1个电子达到8电子稳定结构
D. NaCl中含有离子键,HCl中含有共价键
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com