
【题目】某仅由碳、氢、氧三种元素组成的有机化合物,经测定其相对分子质量为90。取有机物样品1.8 g,在纯氧中完全燃烧,将产物先后通过浓硫酸和碱石灰,两者分别增重1.08 g和2.64 g。试求该有机物的分子式。
【答案】已知m(H)=1.08g×2÷18=0.12g,m(C)=2.64g×12÷44=0.72g
则m(O)=1.8g―0.12g―0.72g=0.96g
则n(C)∶n(H)∶n(O)=0.72÷12∶0.12÷1∶0.96÷16=1∶2∶1
则其实验式为CH2O
故可设其分子式为 (CH2O)n
则有30n=90
解之得:n=3
故分子式为C3H6O3
【解析】试题分析:浓硫酸吸收的是水
则水的物质的量是![]()
碱石灰吸收的是CO2
则CO2的物质的量是![]()
其中碳、氢原子的质量分别是
m(H)=0.06mol×1g/mol=0.12g
m(C)=0.006mol×12g/mol=0.72g
所以根据质量守恒定律可知,有机物中氧原子的质量是
m(O)=1.8g―0.12g―0.72g=0.96g
其物质的量是![]()
所以n(C)∶n(H)∶n(O)=0.06∶0.12∶0.06=1∶2∶1
因此其实验式为CH2O
所以可设其分子式为 (CH2O)n
则有30n=90
解之得n=3
所以分子式为C3H6O3


 能考试期末冲刺卷系列答案
能考试期末冲刺卷系列答案科目:高中化学 来源: 题型:
【题目】现有反应:CO(g)+H2O(g)![]() CO2(g)+H2(g) △H=-QkJ/mol (Q>0) 在850℃时,K=1。
CO2(g)+H2(g) △H=-QkJ/mol (Q>0) 在850℃时,K=1。
①写出该反应的化学平衡常数的表达式K=__________。
②若升高温度到950℃,达到平衡时K____1 (填“大于”“ 小于”或“等于”),理由是__________。
③ 850℃时,若向一容积可变的密闭容器中同时充入1.0molCO,3.0molH2O,1.0molCO2和xmolH2,则:当x=5.0时,上述反应向_______________方向进行(填“正反应”或“逆反应”)。
④上述反应达平衡后,扩大该容器体积,平衡___________(正向移动、逆向移动或不移动)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】草酸亚铁晶体是一种淡黄色粉末,常用于照相显影剂及制药工业,也是电池材料的制备原料。某化学兴趣小组对草酸亚铁晶体的一些性质进行探究。
(1)甲组同学用如图所示装置测定草酸亚铁晶体(FeC2O4·xH2O)中结晶水含量,将石英玻璃管(带两端开关K1和K2)(设为装置A)称重,记为ag。将样品装入石英玻璃管中,再次将装置称重,记为b g。按图连接好装置进行实验。
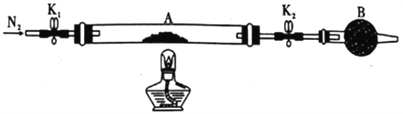
a.打开K1和K2,缓缓通入N2; b.点燃酒精灯加热; c.熄灭酒精灯;d.冷却至室温;e.关闭K1和K2; f.称重A;g.重复上述操作,直至A恒重,记为cg。
①仪器B的名称是__________ ,通入N2的目的是___________。
②根据实验记录,计算草酸亚铁晶体化学式中的x =____________(列式表示);若实验时a、b次序对调,会使x值______________ (填“偏大” “无影响”或“偏小”)。
(2)乙组同学为探究草酸亚铁的分解产物,将(1)中已恒重的装置A接入图14所示的装置中,打开K1和K2,缓缓通入N2,加热。实验后装置A中残留固体为黑色粉末。

①装置C、G中的澄清石灰水均变浑浊,说明分解产物中有____________(填化学式)。
②装置F中盛放的物质是___________(填化学式)。
③将装置A中的残留固体溶于稀盐酸,无气泡,滴入KSCN溶液无血红色,说明分解产物中A的化学式为________。
④写出草酸亚铁(FeC2O4)分解的化学方程式:______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】明矾石的主要成分是K2SO4Al2(SO4)32Al2O36H2O,还含有杂质Fe2O3 . 利用明矾石来制取纯净的Al2O3、K2FeO4和H2SO4的工艺流程如图所示. 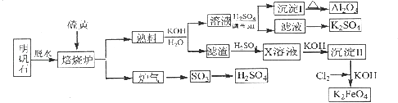
请回答下列问题:
(1)焙烧炉中发生反应的化学方程式为2Al2(SO4) ![]() 2Al2O3+6SO2↑+3O2↑,若生成102gAl2O3 , 转移的电子数目为 .
2Al2O3+6SO2↑+3O2↑,若生成102gAl2O3 , 转移的电子数目为 .
(2)生成沉淀I的离子方程式为 , 沉淀II的化学式为 .
(3)溶液经加硫酸调节pH后,过滤,洗涤,可得沉淀I,证明沉淀I已洗涤干净的实验操作和现象是
(4)写出Cl2将沉淀Ⅱ氧化为K2FeO4的化学方程式: .
(5)从滤液中得到K2SO4晶体的方法是 .
(6)K2FeO4也可以铁为电极,通过电解浓的KOH溶液来制取,写出电解法制取K2FeO4的阳极反应式: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上以锂辉石为原料生产碳酸锂的部分工业流程如下:
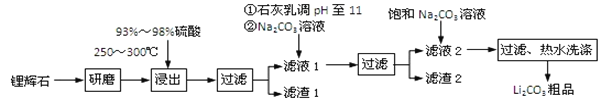
已知:
①锂辉石的主要成分为Li2O·Al2O3·4SiO2,其中含少量Ca、Mg元素。
②Li2O·Al2O3·4SiO2 + H2SO4(浓) ![]() Li2SO4 + Al2O3·4SiO2·H2O
Li2SO4 + Al2O3·4SiO2·H2O
③某些物质的溶解度(s)如下表所示。
T/℃ | 20 | 40 | 60 | 80 |
s(Li2CO3)/g | 1.33 | 1.17 | 1.01 | 0.85 |
s(Li2SO4)/g | 34.2 | 32.8 | 31.9 | 30.7 |
(1)从滤渣Ⅰ中分离出Al2O3的流程如下图所示。请写出生成沉淀的离子方程式______。
![]()
(2)已知滤渣2的主要成分有Mg(OH)2和CaCO3。向滤液1中加入石灰乳的作用是(运用化学平衡原理简述)________________________________________________。
(3)最后一个步骤中,用“热水洗涤”的原因是______________________________。
(4)工业上,将Li2CO3粗品制备成高纯Li2CO3的部分工艺如下:
a.将Li2CO3溶于盐酸作电解槽的阳极液,LiOH溶液做阴极液,两者用离子选择透过膜隔开,用惰性电极电解。
b.电解后向LiOH溶液中加入少量NH4HCO3溶液并共热,过滤、烘干得高纯Li2CO3。
①a中,阳极的电极反应式是_________________________
②电解后,LiOH溶液浓度增大的原因_________________,b中生成Li2CO3反应的化学方程式是___________________________________________。
(5)磷酸亚铁锂电池总反应为:FePO4+Li![]() LiFePO4,电池中的固体电解质可传导Li+,试写出该电池放电时的正极反应:__________________。
LiFePO4,电池中的固体电解质可传导Li+,试写出该电池放电时的正极反应:__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于沉淀溶解平衡的说法中不正确的是( )
A.难溶电解质在水中存在沉淀溶解平衡,且是一种动态平衡
B.Ksp只与难溶电解质的性质和温度有关,而与沉淀的量和溶液中离子的浓度无关
C.Ksp反映了物质在水中的溶解能力,可直接根据Ksp的数值大小比较电解质在水中的溶解能力大小
D.Ksp改变,可使沉淀溶解平衡移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某新型药物H合成路线如图所示:

已知:
①A的分子式为C9H10,其苯环上只有一个取代基,且取代基上只有两种不同化学环境的氢原子;
②E的分子式为C9H8O2,能使溴的四氯化碳溶液褪色;
③H的结构简式为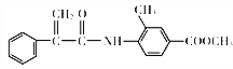 ;
;
④![]() ;
;
⑤![]() 。
。
请回答下列问题:
(1)E的官能团名称为_______________,上述反应中属于取代反应的有____________(填序号)。
(2)下列有关说法正确的是_____________ (填字母) 。
A.A没有顺反异构
B.C可发生的反应类型有取代、加成、消去、氧化、聚合等
C.E中所有碳原子可能在同一个平面上
D.1 mol H最多可以和2 mol NaOH反应
(3)G的结构简式为_________________。
(4)D在一定条件下可以聚合形成高分子,写出该反应的化学方程式_______________________。
(5)E有多种同分异构体,同时满足下列条件的E的同分异构体有_______种。
①能发生银镜反应 ②能发生水解反应
(6)参照H的上述合成路线,设计一条由乙醛和NH2CH(CH3)2为起始原料制备医药中间体CH3CONHCH(CH3)2的合成路线。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com