
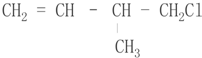
 .
.分析 ①该有机物中的官能团是碳碳双键和氯原子;
②该物质中含有碳碳双键,所以一定条件下能发生加聚反应生成高分子化合物;
③该有机物中的碳碳双键在一定条件下能和氢气发生加成反应生成饱和氯代烃;
④该有机物和NaOH的醇溶液在加热条件下能发生消去反应.
解答 解:①该有机物中的官能团是碳碳双键和氯原子,故答案为:碳碳双键、氯原子;
②该物质中含有碳碳双键,所以一定条件下能发生加聚反应生成高分子化合物,该聚合物结构简式为 ,故答案为:
,故答案为: ;
;
③该有机物中的碳碳双键在一定条件下能和氢气发生加成反应生成饱和氯代烃,反应方程式为CH2=CHCH(CH3)CH2Cl+H2$\stackrel{一定条件下}{→}$CH2ClCHClCH(CH3)CH2Cl,
故答案为:CH2=CHCH(CH3)CH2Cl+H2$\stackrel{一定条件下}{→}$CH2ClCHClCH(CH3)CH2Cl;
④该有机物和NaOH的醇溶液在加热条件下能发生消去反应,反应方程式为CH2=CHCH(CH3)CH2Cl+NaOH$→_{△}^{NaOH/醇}$CH2=CHC(CH3)=CH2+NaCl+H2O,
故答案为:CH2=CHCH(CH3)CH2Cl+NaOH$→_{△}^{NaOH/醇}$CH2=CHC(CH3)=CH2+NaCl+H2O.
点评 本题考查有机物结构和性质,为高频考点,侧重考查学生分析判断及知识运用能力,明确官能团及其性质关系是解本题关键,涉及卤代烃和烯烃性质,注意卤代烃发生消去反应和水解反应的反应条件区别,题目难度不大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:解答题


查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 ,D中官能团的名称为羧基.
,D中官能团的名称为羧基.
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | K+、H+、SO42-、OH- | B. | Na+、Ca2+、CO32-、NO3- | ||
| C. | Na+、H+、Cl-、HCO32- | D. | Na+、Cu2+、Cl-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铜与稀硫酸反应生成氢气 | |
| B. | 铁与水反应生成氢氧化铁和氢气 | |
| C. | 钠投入CuSO4溶液中,可以置换出铜 | |
| D. | 某溶液与铝反应产生氢气,该溶液不一定是酸性溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
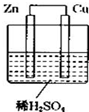 如图所示是 Zn 和 Cu 形成的原电池,某实验兴趣小组做完实验后,在读书卡上的记录卡如下,则卡片上的描述合理的是( )
如图所示是 Zn 和 Cu 形成的原电池,某实验兴趣小组做完实验后,在读书卡上的记录卡如下,则卡片上的描述合理的是( )| A. | ②④⑤ | B. | ②③④⑤ | C. | ①④⑥ | D. | ③④⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③②④⑤ | B. | ②①④⑤③ | C. | ②④①⑤③ | D. | ④⑤②①③ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com