
| A. | 2 g 氦气所含有的原子数目是0.25 NA | |
| B. | 常温常压下,0.5 mol Cl2所占有的体积约为11.2 L | |
| C. | 标准状况下,0.9 mL水的质量约为0.9 g | |
| D. | 0.5 mol/L Na2SO4 溶液中Na+ 的物质的量是1 mol |
分析 A、氦气为单原子分子;
B、常温常压下,气体的摩尔体积不知;
C、标准状况下,水的密度为1g/mL;
D、体积不知,无法由物质的量浓度求物质的量.
解答 解:A、2g氦气的物质的量n=$\frac{2g}{4g/mol}$=0.5mol,而氦气为单原子分子,故0.5mol氦气中含1mol氦原子即0.5NA个,故A错误;
B、常温常压下,气体的摩尔体积不知,而标准状况下0.5 mol Cl2所占有的体积约为11.2 L,故B错误;
C、标准状况下,水的密度为1g/mL,所以标准状况下,0.9 mL水的质量约为0.9 g,故C正确;
D、体积不知,无法由物质的量浓度求物质的量,故D错误;
故选C.
点评 本题考查阿伏加德罗常数的有关计算和判断,题目难度中等,注意明确标况下气体摩尔体积的使用条件;阿伏加德罗常数是高考的“热点”,它既考查了学生对物质的量、粒子数、质量、体积等与阿伏加德罗常数关系的理解,又可以涵盖多角度的化学知识内容.


科目:高中化学 来源: 题型:实验题
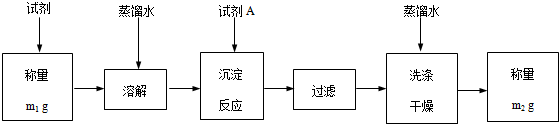
| 实验步骤 | 预期现象和结论 |
| 步骤1:取适量试剂于洁净烧杯中,加入足量蒸馏水,充分搅拌,静置,过滤,得滤液和沉淀 | / |
| 步骤2:取适量步骤1滤液于试管中,滴加稀硫酸 | 生成白色沉淀,说明该试剂中含有Ba2+ |
| 步骤3:取适量步骤1中的沉淀于是试管中,… | …,说明该试剂中含有BaCO3 |
| 步骤4:… | … |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
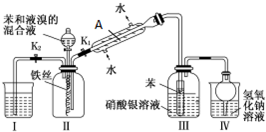
| 物质 | 丙酮 | 乙酸乙酯 | 乙醇 | 乙酸 |
| 沸点/℃ | 56.2 | 77.06 | 78 | 117.9 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 稳定性:HF>HCl>HBr>HI | B. | 酸性:H4SiO4<H3PO4<H2SO4<HClO4 | ||
| C. | 粒子半径:Al3+>Mg2+>Na+>F- | D. | 碱性:Al(OH)3<Mg(OH)2<Ca(OH)2<KOH |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cu和浓硫酸在加热的条件下可以反应,体现浓硫酸的强氧化性和酸性 | |
| B. | 将SO2通入盛有品红溶液的试管中红色褪去,给试管加热无明显变化 | |
| C. | 将干燥的Cl2通入装有红色鲜花的试管中,红花褪色,说明Cl2具有漂白性 | |
| D. | 将蘸有浓氨水和浓硫酸的玻璃棒靠近,会产生白烟 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 热稳定性:HF>H2O>NH3 | B. | 原子半径:F>O>N | ||
| C. | 沸点:乙烷>戊烷>丁烷 | D. | 酸性:H2SO4>H3PO4>HClO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该反应850℃的选择是基于熔沸点的考虑 | |
| B. | 该反应不能在空气中进行 | |
| C. | 该反应属于置换反应的类型 | |
| D. | 该反应表明钠比钾的活动性强 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com