
| A. | 亚硫酸的电离方程式:H2SO3?2H++SO32- | |
| B. | 乙炔的分子结构模型示意图: | |
| C. | H2O2的电子式: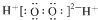 | |
| D. | 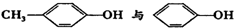 互为同系物 互为同系物 |
分析 A.亚硫酸存在电离平衡,以第一步电离为主;
B.乙炔为直线结构;
C.H2O2为共价化合物;
D.对甲基苯酚与苯酚的结构相似,相差1个CH2原子团.
解答 解:A.亚硫酸存在电离平衡,以第一步电离为主,电离方程式为H2SO3?H++HSO3-,故A错误;
B.乙炔为直线结构,炔的分子结构模型示意图为: ,故B错误;
,故B错误;
C.H2O2为共价化合物,电子式为 ,故C错误;
,故C错误;
D.对甲基苯酚与苯酚的结构相似,相差1个CH2原子团,则二者互为同系物,故D正确;
故选D.
点评 本题考查化学用语,为高频考点,把握电子式、结构模型、电离方程式等为解答的关键,侧重分析与应用能力的考查,注意化学用语的规范使用,题目难度不大.


 培优三好生系列答案
培优三好生系列答案科目:高中化学 来源: 题型:多选题
| A. | 向溶解有Na2O2的水溶液中滴入2滴酚酞试液,溶液先变红振荡后褪色 | |
| B. | 氯气的性质活泼,它与氢气混合后立即发生爆炸 | |
| C. | 铁在纯氧中燃烧或高温下和水蒸气反应均能得到黑色Fe3O4 | |
| D. | 新制的氯水加入有色布条褪色,说明溶液中有Cl2存在 |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 若每消耗2n mol HI的同时生成n mol H2,表明该反应已达平衡 | |
| B. | 容器内的压强不发生变化,表明该反应已达平衡 | |
| C. | 平衡时,若其他条件不变,再充入一定量HI,重新达平衡后,I2的百分含量增大 | |
| D. | 平衡时,若其他条件不变,升高温度,混合气体的颜色加深 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题

 .
.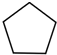 .
. .
.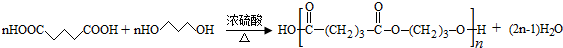 .
. (写结构简式):
(写结构简式):查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | m-13=n | B. | n+5=m | C. | m+8=n | D. | n-11=m |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 编号 | 实验内容 | 实验原理 | 气体发生装置 |
| ① | 制备氧气 | H2O2→O2 | Ⅲ |
| ② | 制备二氧化硫 | Na2SO3→SO2 | Ⅲ |
| ③ | 制备氯气 | HCl→Cl2 | Ⅰ或Ⅲ |
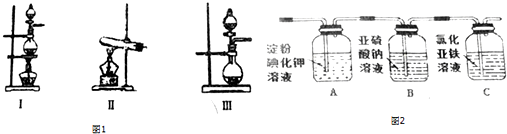
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
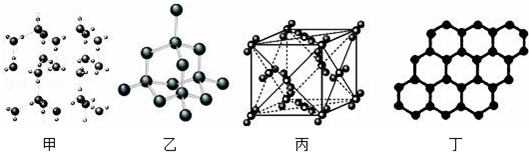
| A. | 18g 冰(图甲)中含 O-H 键数目为 4NA | |
| B. | 28g 晶体硅(图乙)中含有σ键数目为 2NA | |
| C. | 44g 干冰(图丙)中含有 NA个晶胞结构单元 | |
| D. | 石墨烯(图丁)是碳原子单层片状新材料,12g 石墨烯中含π键数目为 1.5NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com