
”¾ĢāÄæ”æĻÖÓŠA”¢B”¢CČżÖÖĢž£¬ĘäĒņ¹÷Ä£ŠĶĻĀĶ¼£ŗ

£Ø1£©µČÖŹĮæµÄŅŌÉĻĪļÖŹĶźČ«Č¼ÉÕŹ±ŗÄČ„O2µÄĮæ×ī¶ąµÄŹĒ £ØĢī¶ŌÓ¦×ÖÄø£¬ĻĀĶ¬£©£»
£Ø2£©Ķ¬×“æö”¢Ķ¬Ģå»żµÄŅŌÉĻČżÖÖĪļÖŹĶźČ«Č¼ÉÕŹ±ŗÄČ„O2µÄĮæ×ī¶ąµÄŹĒ £»
£Ø3£©µČÖŹĮæµÄŅŌÉĻČżÖÖĪļÖŹČ¼ÉÕŹ±£¬Éś³É¶žŃõ»ÆĢ¼×ī¶ąµÄŹĒ £¬Éś³ÉĖ®×ī¶ąµÄŹĒ £®
£Ø4£©ŌŚ120”ę”¢1.01”Į105 PaĻĀŹ±£¬ÓŠĮ½ÖÖĘųĢ¬ĢžŗĶ×ćĮæµÄŃõĘų»ģŗĻµćČ¼£¬ĻąĶ¬Ģõ¼žĻĀ²āµĆ·“Ó¦Ē°ŗóĘųĢåĢå»żĆ»ÓŠ·¢Éś±ä»Æ£¬ÕāĮ½ÖÖĘųĢåŹĒ £®
”¾“š°ø”æ£Ø1£©A £Ø2£©C £Ø3£©B A £Ø4£©A”¢B
”¾½āĪö”æ
ŹŌĢā·ÖĪö£ŗ¾ŻĒņ¹÷Ä£ŠĶæÉÖŖAĪŖCH4£¬BĪŖC2H4£¬CĪŖC2H6£¬øł¾Żø÷ÓŠ»śĪļµÄ·Ö×Ó×é³ÉŅŌ¼°ÓėŃõĘų·“Ó¦µÄ»Æѧ·½³ĢŹ½½ųŠŠ¼ĘĖćŗĶÅŠ¶Ļ£®
½āĪö£ŗ¾ŻĒņ¹÷Ä£ŠĶæÉÖŖAĪŖCH4£¬BĪŖC2H4£¬CĪŖC2H6£®
£Ø1£©µČÖŹĮæµÄĢžCxHyĶźČ«Č¼ÉÕŹ±£¬ĒāŌŖĖŲµÄÖŹĮæ·ÖŹżŌ½“ó£¬ŗÄŃõĮæŌ½“ó£¬
CH4”¢C2H4”¢C2H6ÖŠµÄ![]() ŅĄ“ĪĪŖ
ŅĄ“ĪĪŖ![]() ”¢
Ӣ![]() Ӣ
”¢![]() £¬
£¬
¹ŹCH4ŗÄO2×ī¶ą£»
£Ø2£©µČĪļÖŹµÄĮæµÄĢžCxHyĶźČ«Č¼ÉÕŹ±£¬£Øx+![]() £©µÄÖµŌ½“ó£¬ŗÄŃõĮæŌ½“ó£¬
£©µÄÖµŌ½“ó£¬ŗÄŃõĮæŌ½“ó£¬
CH4”¢C2H4”¢C2H6µÄx+![]() ŅĄ“ĪĪŖ1+
ŅĄ“ĪĪŖ1+![]() =2”¢2+
=2Ӣ2+![]() =3Ӣ2+
=3”¢2+![]() =3.5£¬¹ŹC2H6ŗÄO2×ī¶ą£»
=3.5£¬¹ŹC2H6ŗÄO2×ī¶ą£»
£Ø3£©ÉčÓŠ»śĪļ¶¼ĪŖ1g£¬ŌņÉś³ÉµÄCO2·Ö±šĪŖ£ŗ
n£ØCO2£©=n£ØC£©=![]() ”Į1”¢
”Į1”¢![]() ”Į2”¢
”Į2”¢![]() ”Į2£¬
”Į2£¬![]() ”Į2×ī“󣬹ŹC2H4Éś³ÉµÄCO2×ī¶ą£»
”Į2×ī“󣬹ŹC2H4Éś³ÉµÄCO2×ī¶ą£»
Éś³ÉµÄĖ®·Ö±šĪŖ£ŗ
n£ØH2O£©=![]() n£ØH£©=
n£ØH£©=![]() ”Į
”Į![]() ”Į4”¢
”Į4”¢![]() ”Į
”Į![]() ”Į4”¢
”Į4”¢![]() ”Į
”Į![]() ”Į6£¬
”Į6£¬![]() ”Į
”Į![]() ”Į4×ī“󣬹ŹCH4Éś³ÉµÄH2O×ī¶ą£®
”Į4×ī“󣬹ŹCH4Éś³ÉµÄH2O×ī¶ą£®
£Ø4£©ĪĀ¶Č”Ż100”ęĢõ¼žĻĀ£¬µ±Ģž·Ö×ÓÖŠŗ¬ÓŠ4øöĒāŌ×ÓŹ±£¬øĆĢžĶźČ«Č¼ÉÕĒ°ŗóĘųĢåĢå»ż²»±ä£¬y=4µÄĪŖCH4”¢C2H4£¬
¹ŹĪŖCH4”¢C2H4£®
¹Ź“š°øĪŖ£ŗ£Ø1£©A £Ø2£©C £Ø3£©B A £Ø4£©A”¢B£®


 ĆūŠ£æĪĢĆĻµĮŠ“š°ø
ĆūŠ£æĪĢĆĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĢĒĄą”¢ÓĶÖ¬”¢µ°°×ÖŹĪŖ¶ÆĪļŠŌŗĶÖ²ĪļŠŌŹ³ĪļÖŠµÄ»ł±¾ÓŖŃųĪļÖŹ”£ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
A£®µ°°×ÖŹÖŠÖ»ŗ¬C”¢H”¢OČżÖÖŌŖĖŲ
B£®ÓĶÖ¬ŌŚČĖĢåÖŠ·¢ÉśĖ®½āµÄ²śĪļŹĒ°±»łĖį
C£®Å£ÓĶ”¢“ó¶¹ÓĶµÄÖ÷ŅŖ³É·Ö¶¼ŹĒøß¼¶Ö¬·¾ĖįøŹÓĶÖ¬
D£®ĢĒĄą”¢ÓĶÖ¬”¢µ°°×ÖŹŅ»¶Ø¶¼ÄÜ·¢ÉśĖ®½ā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŅŅ“¼·Ö×ÓÖŠø÷»Æѧ¼üČēĶ¼ĖłŹ¾¶ŌŅŅ“¼ŌŚø÷ÖÖ·“Ó¦ÖŠÓ¦¶ĻĮŃµÄ¼üĖµĆ÷²»ÕżČ·µÄŹĒ£Ø £©
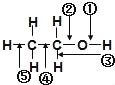
A£®ŗĶ½šŹōÄĘ×÷ÓĆŹ±£¬¼ü¢Ś¶ĻĮŃ
B£®ŗĶÅØĮņĖį¹²ČČÖĮ170”ꏱ£¬¼ü¢ŚŗĶ¢Ż¶ĻĮŃ
C£®ŗĶHBr¹²ČČŹ±£¬¼ü¢Ü¶ĻĮŃ
D£®ŌŚĶ“ß»ÆĻĀŗĶŃõĘų·“Ó¦Ź±£¬¼ü¢ŁŗĶ¢Ū¶ĻĮŃ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ1Ģå»żÄ³ĘųĢ¬ĢžŗĶ2Ģå»żĀČ»ÆĒā·¢Éś¼Ó³É·“Ó¦ŗó£¬×ī¶ą»¹ÄÜŗĶ6Ģå»żĀČĘų·¢ÉśČ”“ś·“Ó¦£®ÓÉ“ĖæÉŅŌ¶Ļ¶ØŌĘųĢ¬ĢžŹĒ£ØĘųĢåĢå»ż¾łŌŚĻąĶ¬Ģõ¼žĻĀ²ā¶Ø£©£Ø £©
A£®ŅŅČ² B£®±ūČ² C£®¶”Č² D£®¶”¶žĻ©
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
A£®Ąė×Ó»ÆŗĻĪļµÄČŪµćŅ»¶Ø±Č¹²¼Ū»ÆŗĻĪļČŪµćøß
B£®¼×ĶéµÄ±ź×¼Č¼ÉÕČČĪŖ890.3KJ/mol£¬Ōņ¼×ĶéČ¼ÉÕµÄČČ»Æѧ·½³ĢŹ½æɱķŹ¾ĪŖ£ŗCH4(g)+2O2(g)=CO2(g)+2H2O(g) ”÷H=-890.3kJ”¤mol-1
C£®500”ę”¢30MPaĻĀ£¬½«0.5mol N2ŗĶ1.5molH2ÖĆÓŚĆܱյÄČŻĘ÷ÖŠ³ä·Ö·“Ӧɜ³ÉNH3(g)£¬·ÅČČ19.3kJ£¬ĘäČČ»Æѧ·½³ĢŹ½ĪŖN2(g)+3H2(g) ![]() 2NH3(g) ”÷H=£38.6kJ”¤mol-1
2NH3(g) ”÷H=£38.6kJ”¤mol-1
D£®Ķ¬ĪĀĶ¬Ń¹ĻĀ£¬H2(g)+Cl2(g)=2HCl(g)ŌŚ¹āÕÕĢõ¼žŗĶµćČ¼Ģõ¼žĻĀµÄ”÷HĻąĶ¬
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĖę×Å“óĘųĪŪČ¾µÄČÕĒ÷ŃĻÖŲ£¬¹ś¼ŅÄāÓŚ”°Ź®¶žĪå”±ĘŚ¼ä£¬½«¶žŃõ»ÆĮņ(SO2)ÅÅ·ÅĮæ¼õÉŁ 8%£¬µŖŃõ»ÆĪļ(NOx)ÅÅ·ÅĮæ¼õÉŁ 10%”£ÄæĒ°£¬Ļū³ż“óĘųĪŪČ¾ÓŠ¶ąÖÖ·½·Ø”£
£Ø1£©ÓĆ CH4 “߻ƻ¹ŌµŖŃõ»ÆĪļæÉŅŌĻū³żµŖŃõ»ÆĪļµÄĪŪČ¾”£
ŅŃÖŖ£ŗ¢ŁCH4(g) + 4NO2(g) = 4NO(g) + CO2(g) + 2H2O(g)”÷H =£574 kJ/mol
¢ŚCH4(g) + 4NO(g) = 2N2(g) + CO2(g) + 2H2O(g)”÷H =£1160 kJ/mol
¢ŪH2O(g) = H2O(l) ”÷H =£44.0 kJ/mol
Š“³ö CH4(g)Óė NO2(g)·“Ӧɜ³É N2(g)”¢CO2(g)ŗĶ H2O(l)µÄČČ»Æѧ·½³ĢŹ½£ŗ__________”£
£Ø2£©ĄūÓĆ Fe2+”¢Fe3+µÄ“ß»Æ×÷ÓĆ£¬³£ĪĀĻĀæɽ« SO2 ×Ŗ»ÆĪŖ SO42-£¬“Ó¶ųŹµĻÖ¶Ō SO2 µÄÖĪĄķ”£ŅŃÖŖŗ¬ SO2 µÄ·ĻĘųĶØČėŗ¬ Fe2+”¢Fe3+µÄČÜŅŗŹ±£¬ĘäÖŠŅ»øö·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ 4Fe2+ + O2 + 4H+ = 4Fe3+ + 2H2O£¬ŌņĮķŅ»·“Ó¦µÄ Ąė×Ó·½³ĢŹ½ĪŖ__________”£
£Ø3£©ÓĆ»īŠŌĢ滹Ō·Ø“¦ĄķµŖŃõ»ÆĪļ”£ÓŠ¹Ų·“Ó¦ĪŖ C(s) + 2NO(g) ![]() N2(g) + CO2(g)”£Ä³ŃŠ¾æŠ”×éĻņĆܱյÄÕęæÕ ČŻĘ÷ÖŠ(¼ŁÉčČŻĘ÷Ģå»ż²»±ä£¬¹ĢĢåŹŌŃłĢå»żŗöĀŌ²»¼Ę)¼ÓČė NO ŗĶ×ćĮæµÄ»īŠŌĢ棬ŌŚŗćĪĀ(T1”ę)Ģõ¼žĻĀ·“Ó¦£¬·“Ó¦½ųŠŠµ½²»Ķ¬Ź±¼ä²āµĆø÷ĪļÖŹµÄÅضČČēĻĀ£ŗ
N2(g) + CO2(g)”£Ä³ŃŠ¾æŠ”×éĻņĆܱյÄÕęæÕ ČŻĘ÷ÖŠ(¼ŁÉčČŻĘ÷Ģå»ż²»±ä£¬¹ĢĢåŹŌŃłĢå»żŗöĀŌ²»¼Ę)¼ÓČė NO ŗĶ×ćĮæµÄ»īŠŌĢ棬ŌŚŗćĪĀ(T1”ę)Ģõ¼žĻĀ·“Ó¦£¬·“Ó¦½ųŠŠµ½²»Ķ¬Ź±¼ä²āµĆø÷ĪļÖŹµÄÅضČČēĻĀ£ŗ
ÅضČ(mol/L) | NO | N2 | CO2 |
0 | 1.00 | 0 | 0 |
10 | 0.58 | 0.21 | 0.21 |
20 | 0.40 | 0.30 | 0.30 |
30 | 0.40 | 0.30 | 0.30 |
40 | 0.32 | 0.34 | 0.17 |
50 | 0.32 | 0.34 | 0.17 |
¢Ł10”«20 min ŅŌ¦Ō(N2)±ķŹ¾µÄ·“Ó¦ĖŁĀŹĪŖ__________”£
¢ŚøĆ·“Ó¦µÄĘ½ŗā³£Źż±ķ“ļŹ½ K=________”£øł¾Ż±ķÖŠŹż¾Ż£¬¼ĘĖć T1 ”ꏱøĆ·“Ó¦µÄĘ½ŗā³£ŹżĪŖ__________(±£ĮōĮ½Ī»Š”Źż)”£
¢ŪŅ»¶ØĪĀ¶ČĻĀ£¬Ėę×Å NO µÄĘšŹ¼ÅضČŌö“ó£¬Ōņ NO µÄĘ½ŗā×Ŗ»ÆĀŹ__________ (
¢ÜĻĀĮŠø÷ĻīÄÜ×÷ĪŖÅŠ¶ĻøĆ·“Ó¦“ļµ½Ę½ŗāµÄŹĒ__________ (ĢīŠņŗÅ)”£
A£®»ģŗĻĘųĢåµÄĆܶȱ£³Ö²»±ä
B£®¦ŌÕż(NO) = 2¦ŌÄę(CO2)
C£®ČŻĘ÷ÄŚŃ¹Ēæ±£³Ö²»±ä
D£®ČŻĘ÷ÄŚ N2 µÄĢå»ż·ÖŹż±£³Ö²»±ä
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ(1)Ķ¬ĪĀĶ¬Ń¹ĻĀ£¬Ķ¬Ģå»żµÄ¼×Ķé(CH4)ŗĶ¶žŃõ»ÆĢ¼·Ö×ÓŹżÖ®±ČĪŖ__________£¬ĪļÖŹµÄĮæÖ®±ČĪŖ__________£¬Ō×Ó×ÜŹżÖ®±ČĪŖ__________£¬ÖŹĮæÖ®±ČĪŖ__________£¬ĆܶČÖ®±ČĪŖ__________”£
(2)ŌŚ±ź×¼×“æöĻĀ£¬4 g H2”¢11.2 L O2”¢1 mol H2OÖŠ£¬Ėłŗ¬·Ö×ÓŹż×ī¶ąµÄŹĒ________£¬ŗ¬Ō×ÓŹż×ī¶ąµÄŹĒ________£¬ÖŹĮæ×ī“óµÄŹĒ________£¬Ģå»ż×īŠ”µÄŹĒ________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŌŚÖÜĘŚ±ķÖŠ£¬µŚ3”¢4”¢5”¢6ÖÜĘŚŌŖĖŲµÄŹżÄæ·Ö±šŹĒ£Ø £©
A. 8Ӣ18Ӣ32Ӣ32 B. 8Ӣ18Ӣ18Ӣ32
C. 8Ӣ18Ӣ18Ӣ18 D. 8Ӣ8Ӣ18Ӣ18
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŌŚĒæĖįŠŌĪŽÉ«ČÜŅŗÖŠ£¬ĻĀĮŠĄė×Ó×éÄÜ“óĮæ¹²“ęµÄŹĒ
A. Na+ӢK+ ӢOH-ӢCl- B. Na+ӢCu2+ӢSO42-ӢNO3-
C. K+ӢMg2+ӢSO42-ӢCl- D. Ba2+ӢHCO3-ӢNO3-ӢK+
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com