
| 离子晶体 | 原子晶体 | 分子晶体 | |
| A | NaOH | Ar | SO2 |
| B | H2SO4 | 晶体硅 | S |
| C | CH3COONa | 水晶 |  |
| D | Ba(OH)2 | 金刚石 | 玻璃 |
| A. | A | B. | B | C. | C | D. | D |
分析 离子晶体是由阴、阳离子通过离子键形成的晶体,常见离子晶体有:常见的有强碱、活泼金属氧化物、大多数盐类等;
原子晶体是原子之间通过共价键形成的晶体,常见的原子晶体有:一些非金属单质,若金刚石、硼、硅、锗等;一些非金属化合物,如二氧化硅、碳化硅、氮化硼等;
分子晶体是分子间通过分子间作用力(包括范德华力和氢键)构成的晶体,常见的分子晶体有:所有非金属氢化物、部分非金属单质(金刚石、晶体硅等除外)、部分非金属氧化物(二氧化硅等除外)、几乎所有的酸、绝大多数的有机物晶体、所有常温下呈气态的物质、常温下呈液态的物质(除汞外)、易挥发的固态物质等.
解答 解:A、NaOH属于离子晶体,Ar属于分子晶体,SO2属于分子晶体,故A错误;
B、H2SO4属于分子晶体,晶体硅属于原子晶体,S属于分子晶体,故B错误;
C、CH3COONa属于离子晶体,水晶(SiO2)属于原子晶体,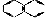 属于分子晶体,故C正确;
属于分子晶体,故C正确;
D、Ba(OH)2属于离子晶体,金刚石属于原子晶体,玻璃属于玻璃态物质,是非晶体,故D错误;
故选C.
点评 本题考查晶体类型判断,难度不大,掌握常见物质所属晶体类型,识记常见的原子晶体即可解答,注意石墨的晶体结构与玻璃态物质.


科目:高中化学 来源: 题型:选择题
| A. | 钢铁制品的腐蚀常以析氢腐蚀为主 | |
| B. | 厨房中常用碳酸钠溶液洗涤餐具上的油污 | |
| C. | 明矾用于水的杀菌消毒 | |
| D. | 新型材料聚酯纤维、光导纤维都属于有机高分子材料 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CaCO3(s)=CaO(s)+CO2(g)室温下不能自发进行,说明该反应的△H<0 | |
| B. | 镀铜铁制品镀层受损后,铁制品不易生锈 | |
| C. | 加热0.1mol/LNa2CO3溶液,CO32-的水解程度和溶液的pH均增大 | |
| D. | 对于乙酸与乙醇的酯化反应(△H<0),加入少量浓硫酸并加热,该反应的反应速率和平衡常数均增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将一小块金属钠投入稀硫酸铜溶液中会有红色固体析出 | |
| B. | 向0.4mol浓盐酸中加入足量的MnO2,加热,可收集(标准状况下)2.24LCl2 | |
| C. | 向足量的盐酸和氢氧化钠溶液中各加入等质量的Al粉,消耗盐酸与氢氧化钠溶液的物质的量之比为3:1 | |
| D. | 150 mL 1 mol•L-1NaCl溶液与75 mL 1 mol•L-1 Na2CO3溶液中Na+物质的量浓度相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 实验步骤 | 实验现象 | 实验结论 |
Ⅰ.取第一份溶液和适量稀盐酸加入下列装置的试管中,把澄清的石灰水加入烧杯中 | 导管口有气泡, | 证明含有CO32- |
| Ⅱ.取第二份溶液,先滴加稀盐酸后加 | 证明含有SO42- | |
| Ⅲ.取第三份溶液加入过量BaCl2溶液,过滤,除去SO42-和CO32-,再滴加AgNO3溶液和稀硝酸 | 有白色沉淀生成 | 证明含有Cl- |
| Ⅳ.取第四份溶液进行焰色反应 | 透过蓝色钴玻璃火焰呈紫色 | 证明含有K+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. |
| B. |
| C. |
| D. |
|
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
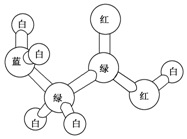 某期刊封面上有如下一个分子的球棍模型图,图中“棍”代表单键或双键或三键.不同颜色的球代表不同元素的原子,该模型图可代表一种( )
某期刊封面上有如下一个分子的球棍模型图,图中“棍”代表单键或双键或三键.不同颜色的球代表不同元素的原子,该模型图可代表一种( )| A. | 卤代羧酸 | B. | 酯 | C. | 氨基酸 | D. | 乙醇钠 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com