
 上世纪60年代,第一个稀有气体化合物Xe[PtF6]被合成出来后,打破了“绝对惰性”的观念.在随后的几年内,科学家又相继合成了氙的氟化物、氧化物等.
上世纪60年代,第一个稀有气体化合物Xe[PtF6]被合成出来后,打破了“绝对惰性”的观念.在随后的几年内,科学家又相继合成了氙的氟化物、氧化物等.分析 (1)Ni的原子序数为28,根据能量最低原理和洪特规则书写电子排布式;
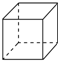
(2)铜的堆积模型为最紧密堆积,配位数为12,铜原子位于顶点和面心,与二氧化碳分子晶胞结构相似;
(3)XeO3分子中含有3个δ键和一个孤电子对,为三角锥形分子,结构不对称.
解答 解:(1)Ni的原子序数为28,根据能量最低原理和洪特规则可写出基态Ni原子核外电子排布式为1s22s22p63s23p63d84s2,
故答案为:1s22s22p63s23p63d84s2;
(2)铜的堆积模型为最紧密堆积,配位数为12,铜原子位于顶点和面心,与二氧化碳分子晶胞结构相似,
故答案为:正方体的八个顶点和六个面心;
(3)XeO3分子中含有3个δ键和一个孤电子对,为三角锥形分子,结构不对称,为极性分子,故答案为:极性;
点评 本题考查较为综合,涉及电子排布式的书写、晶胞结构、分子的极性等知识,题目难度中等,本题注意常见金属的堆积模型,为易错点,也是易忽视的地方.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:解答题
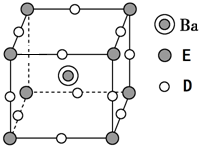 有原子序数依次增大的A、B、C、D、E、F、G 七种元素,A 是短周期中族序数等于周期数的非金属元素;B 元素的原子既不易失去也不易得到电子,其基态原子中每种能级电子数相同;D 的最外层电子数与电子层数之比为3:1;E是地壳中含量第二多的非金属元素;D、F同族; G 元素原子序数为24.
有原子序数依次增大的A、B、C、D、E、F、G 七种元素,A 是短周期中族序数等于周期数的非金属元素;B 元素的原子既不易失去也不易得到电子,其基态原子中每种能级电子数相同;D 的最外层电子数与电子层数之比为3:1;E是地壳中含量第二多的非金属元素;D、F同族; G 元素原子序数为24.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子晶体中的各相邻原子都以共价键相结合 | |
| B. | 金属导电的原因是在外电场作用下金属产生自由电子,电子定向运动 | |
| C. | 分子晶体的熔沸点很低,常温下都呈液态或气态 | |
| D. | 离子晶体中每个离子周围均吸引着6个带相反电荷的离子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 键断裂.如RCH═CHR′可氧化成RCHO和R′CHO,下列烯烃中,经氧化可得到乙醛和丁醛的是( )
键断裂.如RCH═CHR′可氧化成RCHO和R′CHO,下列烯烃中,经氧化可得到乙醛和丁醛的是( )| A. | 1-己烯 | B. | 2-己烯 | C. | 3-已烯 | D. | 2-甲基-2-戊烯 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 一个可逆反应达到的平衡状态就是这个反应在该条件下所能达到的限度 | |
| B. | 当一个可逆反应达到平衡状态时,正反应速率和逆反应速率相等,都等于0 | |
| C. | 平衡状态是一种静止的状态,因为反应物和生成物的浓度已经不再改变 | |
| D. | 化学反应的限度不可以通过改变条件而改变 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na+<Mg2+<Al3+<K+ | B. | S2->Cl->K+>Ca2+ | ||
| C. | O2->S2->Cl->Br- | D. | F->Li+>Na+>S2- |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 用反应物A表示该反应的反应速率为0.6 mol•L-1•min-1 | |
| B. | 用反应物B表示该反应的反应速率为1.8 mol•L-1•min-1 | |
| C. | 反应达到平衡时$\frac{2}{3}$v(B)正=v(C)逆 | |
| D. | 升高温度可加快正反应的速率,同时降低逆反应的速率 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
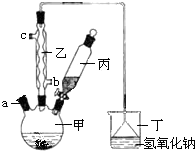 溴苯是一种化工原料,实验室用以下甲、乙、丙、丁等仪器组合,合成溴苯的装置示意图(其余辅助仪器略去)及有关数据如下,按要求回答下列问题:
溴苯是一种化工原料,实验室用以下甲、乙、丙、丁等仪器组合,合成溴苯的装置示意图(其余辅助仪器略去)及有关数据如下,按要求回答下列问题:| 苯 | 溴 | 溴苯 | |
| 密度/g•cm-3 | 0.88 | 3.10 | 1.50 |
| 沸点/°C | 80 | 59 | 156 |
| 水中溶解度 | 微溶 | 微溶 | 微溶 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 放热反应 | B. | 吸热反应 | C. | 氧化还原反应 | D. | 可逆反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com