
�ӵ�ʳ���м���ĵ������һ�ְ�ɫ�ᾧ��ĩ�����ܽ�����¶�Ӱ��ܴ������¶ȵ����߶����������º��ȶ��������������µ������һ�ֽ�ǿ��������������⻯��Ȼ�ԭ�����ʷ�����Ӧ��
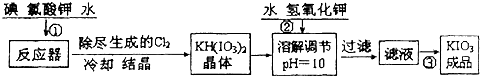
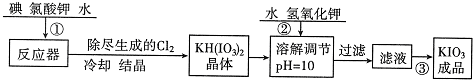
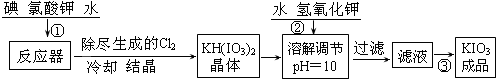
��1��Ϊ����ijʳ�����Ƿ���KIO3��ijͬѧȡʳ����Ʒ��ȫ�ܽ���ˮ�У�Ȼ������������ữ�ĵ���KI��Һ�������Һ����ɫ����Ӧ�����ӷ���ʽΪ ��
��2��KIO3Ҳ���õ��ķ����Ƶã���ԭ������ʯīΪ�������Բ����Ϊ��������һ���¶Ⱥ͵����µ��KI��Һ���ܷ�Ӧ����ʽΪKI+3H2O=KIO3+3H2�����������ĵ缫��Ӧʽ�ֱ�Ϊ������ ������

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
| �¶�/�� | 20 | 40 | 60 | 80 |
| KIO3g/100gˮ | 8.08 | 12.6 | 18.3 | 24.8 |
| O | 2- 3 |
| O | 2- 6 |
| 1270 |
| 3W |
| 1270 |
| 3W |
| �������� | ʵ������ |
| ȡ1g������NaCl����3mLˮ�����Һ�� | ��Һ�ޱ仯 |
| ����5�ε�����Һ��1mL 0.1mol/L KI��Һ���� | ��Һ�ޱ仯 |
| Ȼ���ٵ���1��1mol/L��H2SO4���� | ��Һ����ɫ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
| �¶�/�� | 20 | 40 | 60 | 80 |
| KIO3/100gH2O | 8.08 | 12.6 | 18.3 | 24.8 |
| 1270 |
| 3w |
| 423.33 |
| w |
| 1270 |
| 3w |
| 423.33 |
| w |
| ʵ�鲽�� | ʵ����� | ʵ������ |
| ����1 | ȡ1g������NaCl����3mLˮ�����Һ�� | ��Һ�ޱ仯 |
| ����2 | ����5�ε�����Һ��1mL0.1 mol?L-1KI��Һ���� | ��Һ�ޱ仯 |
| ����3 | Ȼ���ٵ���1��1 mol?L-1��H2SO4���� | ��Һ����ɫ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
| �¶�/�� | 20 | 40 | 60 | 80 |
| KIO3g/100gH2O | 8.08 | 12.6 | 18.3 | 24.8 |
| �� �� �� �� | ʵ������ |
| ȡ1g������NaCl����3mLˮ�����Һ�� | ��Һ�ޱ仯 |
| ����5�ε�����Һ��1mL 0.1mol/L KI��Һ���� | ��Һ�ޱ仯 |
| Ȼ���ٵ���1��1mol/L��H2SO4���� | ��Һ����ɫ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
�ӵ�ʳ���м���ĵ������һ�ְ�ɫ�ᾧ��ĩ�������º��ȶ���������560�濪ʼ�ֽ⡣�����������µ������һ�ֽ�ǿ��������������⻯��������εȻ�ԭ�����ʷ�Ӧ��
������1����ҵ��������ص��������£�
��1����֪����ٷ�Ӧ�������ķ�Ӧ�У����ɵ����ֻ�ԭ�������õ�������ͬ����д����Ӧ���з�����Ӧ�Ļ�ѧ����ʽ���������� ������������������������������ ����
��2�������±�����ص��ܽ�ȣ������۵õ�����ؾ��壬�㽨��ķ��������� ����
| �¶�/�� | 20 | 40 | 60 | 80 |
| KIO3g/100gˮ | 8.08 | 12.6 | 18.3 | 24.8 |
������2����֪��KIO3��5KI��3H2SO4=3K2SO4��3I2��3H2O�� I2��2S2O32��=2I����S4O62����
��1������ӵ�ʳ���еĵ�Ԫ�أ�ѧ�������õ������⻯�������������·�����Ӧ�������Ȼ�̼����ⵥ��ʱ������������������ ���������� ��
��2���ⶨ�ӵ�ʳ���е�ĺ�����ѧ������Ƶ�ʵ�鲽�����£�
a��ȷ��ȡw gʳ�Σ�����������ˮʹ����ȫ�ܽ⣻
b����ϡ�����ữ������Һ���������KI��Һ��ʹKIO3��KI��Ӧ��ȫ��
c���Ե���Ϊָʾ������μ������ʵ���Ũ��Ϊ2.0��10��3mol/L��Na2S2O3��Һ10.0mL
ǡ�÷�Ӧ��ȫ����ӵ�ʳ����Ʒ�еĵ�Ԫ�غ����� mg/kg���Ժ�w�Ĵ���ʽ��ʾ����
��3��ѧ�����ֶԴ�����NaCl������KIO3������������ʵ�飺
| �������� | ʵ������ |
| ȡ1g������NaCl����3mLˮ�����Һ�� | ��Һ�ޱ仯 |
| ����5�ε�����Һ��1mL 0.1mol/L KI��Һ���� | ��Һ�ޱ仯 |
| Ȼ���ٵ���1��1mol/L��H2SO4���� | ��Һ����ɫ |
�� ���Ʋ�ʵ���в�����ɫ����Ŀ���ԭ�������ӷ���ʽ��ʾ ��
�� ����ѧ������ʵ���������ѧ���ҵ�ʵ����������Ҫ���ۣ� ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com