
分析 A、B、C、D、E、F六种短周期元素的原子序数依次增大,D元素原子的最外层电子数比次外层电子数少4,则D为Si元素;E元素原子的次外层电子数比最外层电子数多2,则E是S元素,F有最高价氧化物的水化物,则F是主族元素,原子序数大于S,所以F是Cl元素;
A、C、F三种原子的最外层共有11个电子,且这三种元素的最高价氧化物对应的水化物之间两两皆能反应,均生成盐和水,C为Al元素,A最外层电子数=11-7-3=1,A为Na,则B为Mg,结合题目分析解答.
解答 解:A、B、C、D、E、F六种短周期元素的原子序数依次增大,D元素原子的最外层电子数比次外层电子数少4,则D为Si元素;E元素原子的次外层电子数比最外层电子数多2,则E是S元素,F有最高价氧化物的水化物,则F是主族元素,原子序数大于S,所以F是Cl元素;
A、C、F三种原子的最外层共有11个电子,且这三种元素的最高价氧化物对应的水化物之间两两皆能反应,均生成盐和水,C为Al元素,A最外层电子数=11-7-3=1,A为Na,则B为Mg,
(1)A、B、C、D、E、F六种元素的名称分别为钠、镁、铝、硅、硫、氯,
故答案为:钠;镁;铝;硅;硫;氯;
(2)D的氧化物是二氧化硅、A的最高价氧化物对应水化物是NaOH,二者反应生成硅酸钠和水,反应方程式为SiO2+2NaOH=Na2SiO3+H2O,故答案为:SiO2+2NaOH=Na2SiO3+H2O;
(3)A、C两种元素最高价氧化物对应水化物分别是NaOH、Al(OH)3,二者反应的离子方程式为Al(OH)3+2OH-=AlO2-+2H2O,
故答案为:Al(OH)3+2OH-=AlO2-+2H2O.
点评 本题考查位置结构性质相互关系及应用,正确推断元素是解本题关键,以原子结构、物质性质为突破口进行推断,知道氢氧化铝的两性,题目难度不大.


科目:高中化学 来源: 题型:选择题
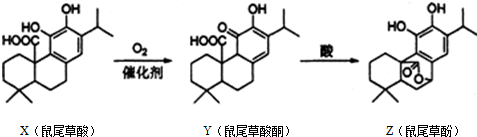
| A. | X、Y、Z属于芳香族化合物 | |
| B. | X、Y、Z均能与FeCl3溶液发生显色反应 | |
| C. | 1 mol X或1mol Z与NaOH溶液反应,均最多消耗3molNaOH | |
| D. | X、Y、Z均能与溴的四氯化碳溶液发生加成反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 石油裂解、煤的气化、海水制镁都包含化学变化 | |
| B. | 福尔马林用于制备标本是利用了其使蛋白质变性的性质 | |
| C. | 红葡萄酒储藏时间长后变香可能是因为乙醇发生了酯化反应 | |
| D. | 含钙、钡、铁等金属元素的物质有绚丽的颜色,可用于制造焰火 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 淀粉、葡萄糖、脂肪和蛋白质在一定条件下都能发生水解反应 | |
| B. | 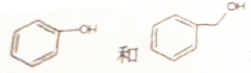 是同系物 是同系物 | |
| C. | 苯、乙烯都能使溴水褪色,但其原理不同 | |
| D. | 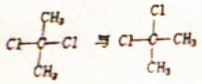 互为同分异构体 互为同分异构体 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 某芳香烃的分子式为C10H14,它不能使溴水褪色,但可使酸性KMnO4溶液褪色,且分子结构中只有一个烷基,符合条件的烃有3种 | |
| B. | 某有机化合物完全燃烧生成等物质的量的CO2和H2O,则该有机物的分子式一定CnH2n | |
| C. | 甲烷、甲醛、甲酸都不存在同分异构体,则甲醚(CH3OCH3)也无同分异构体 | |
| D. | HOCH2COOH既可发生取代反应,也可发生加聚反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 太阳能电池板材料除单晶硅外,还有铜、铟、镓、硒等化学物质.
太阳能电池板材料除单晶硅外,还有铜、铟、镓、硒等化学物质.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com