
(1)1s22s22p63s23p5 (2)[Kr]4d105s25p2 (3)[Ar]3d34s2
(4) [Ar]3d104s1 (5) [Ar]4s1
解析:(1)(2)(5)的价电子排布符合主族元素价电子的排布特征,相应元素都是主族元素,根据它们最高能级组中ns、np两能级上填充的电子数可以确定它们分别属于p区、p区、s区,分别位于ⅦA族、ⅣA族、ⅠA族。(3)(4)的价电子排布符合副族元素价电子的排布特征,相应元素都是副族元素,根据它们最高能级组中(n-1)d、ns两能级上填充的电子数可以确定它们分别属于d区、ds区,分别位于ⅤB族、ⅠB族。根据电子排布式中主量子数的最大值可确定(1)(2)(3)(4)(5)分别位于第三周期、第五周期、第四周期、第四周期、第四周期。
答案:
元素 | 主族还是副族 | 区 | 周期 | 族 |
(1) | 主 | P | 三 | ⅦA |
(2) | 主 | P | 五 | ⅣA |
(3) | 副 | D | 四 | ⅤB |
(4) | 副 | Ds | 四 | ⅠB |
(5) | 主 | S | 四 | ⅠA |


 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案科目:高中化学 来源: 题型:


| ||
| ρg?cm-3 |
| ||
| ρg?cm-3 |

查看答案和解析>>
科目:高中化学 来源:黄冈中学 高一化学(下册)、§5.3元素周期表(2) 题型:021
下列表示核外各电子层上的电子数,其中表示的元素是主族元素的是
A.2、8、18、3
B.2、8、18、2
C.2、8、18、18、8、1
D.2、8、18、18、1
查看答案和解析>>
科目:高中化学 来源:山东省高青一中2009-2010学年度高一上学期期末模块检测考试化学试题 题型:022
阅读下面的元素周期表,按要求回答问题:
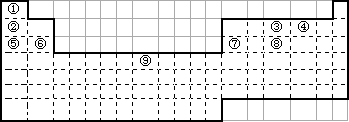
(1)在上面元素周期表中画出金属元素与非金属元素的分界线.
(2)元素⑨在元素周期表中位于________周期________族,它属于________元素(填写“主族”、“副族”或“过渡”).
(3)元素①、④、⑤所形成的化合物中含有的化学键类型是________.
(4)比较元素⑥与元素⑦的金属性:⑥________⑦(填“<”“>”“=”),并设计一个实验加以证明:________
查看答案和解析>>
科目:高中化学 来源:同步题 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com