
| ���� ���� | ��A | ��A | ��A | ��A | ��A | ��A | ��A | 0 |
| 2 | C | N | O | |||||
| 3 | Na | Mg | Si | S | Cl | Ar | ||
| 4 | Ca |
���� ��1��ͬ����������ҽ����Լ�����ͬ�������϶��½�������ǿ���ڽ����˳�����Խ��ǰ��������Խǿ��
��2���ǽ�����Խǿ����ۺ����������Խǿ��
��3��ͬ�����������ԭ�Ӱ뾶��С��
��4����������ͨ�����ڹ��ά��
��5����������Ȼ�þ����þ��������
��� �⣺��1��ͬ����������ҽ����Լ�����ͬ�������϶��½�������ǿ���ڽ����˳�����Խ��ǰ��������Խǿ��������Ԫ����Ca�Ľ����ԣ��ʴ�Ϊ���ƣ�
��2������������Cl�ǽ�������ǿ����HClO4��������ǿ���ʴ�Ϊ��HClO4��
��3��ͬ�����������ԭ�Ӱ뾶��С����ԭ�Ӱ뾶N��C���ʴ�Ϊ��N��
��4����������ͨ�����ڹ��ά���ʴ�Ϊ�����ά��
��5����������Ȼ�þ����þ����������Ӧ����ʽΪ��MgCl2$\frac{\underline{\;���\;}}{\;}$Mg+Cl2�����ʴ�Ϊ��MgCl2$\frac{\underline{\;���\;}}{\;}$Mg+Cl2����
���� ���⿼��Ԫ�����ڱ���Ԫ�������ɣ��Ƚϻ��������ض�Ԫ�������ɵĿ��飬ע��Ի���֪ʶ���������գ�


 ���Ͱ�ͨ�������Сѧ��ʱͬ�����ϵ�д�
���Ͱ�ͨ�������Сѧ��ʱͬ�����ϵ�д� ���Ͱ�ͨ������ϵ�д�
���Ͱ�ͨ������ϵ�д� �ٷ�ѧ����ҵ��������ϵ�д�
�ٷ�ѧ����ҵ��������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
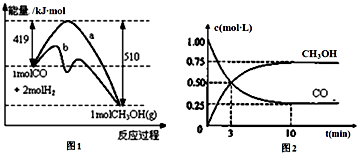 ��ҵ����CO����ȼ�ϼ״���һ���¶Ⱥ��ݻ������·�����Ӧ��CO��g��+2H2��g��?CH3OH��g����ͼ1��ʾ��Ӧ�е������仯��ͼ2��ʾһ���¶��£������Ϊ1L���ܱ������м���2mol
��ҵ����CO����ȼ�ϼ״���һ���¶Ⱥ��ݻ������·�����Ӧ��CO��g��+2H2��g��?CH3OH��g����ͼ1��ʾ��Ӧ�е������仯��ͼ2��ʾһ���¶��£������Ϊ1L���ܱ������м���2mol�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 150mL 1mol/L��AlCl3 | B�� | 75mL 2mol/L��Al��NO3��3 | ||
| C�� | 50mL 3mol/L��AlCl3 | D�� | 50mL 3mol/L��AlBr3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 14C��������������������14C��12C��Ϊͬ�������� | |
| B�� | ʳ��һ��������֬�ܴٽ������ijЩά���ص����� | |
| C�� | ��ѪҺ���������˽�������� | |
| D�� | ���ø����������ҩ�ý��һ�����彡�����Σ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��
��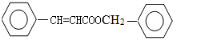 ��
��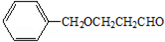 B��
B�� 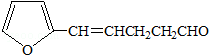
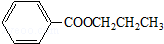
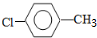 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
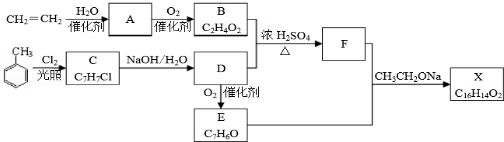
 �����A��B��������Ԫ����ɣ�BΪ���Բ��������A�������C��Ӧת��ΪB�����ӷ���ʽΪAlO2-+CO2+2H2O=Al��OH��3��+HCO3-��
�����A��B��������Ԫ����ɣ�BΪ���Բ��������A�������C��Ӧת��ΪB�����ӷ���ʽΪAlO2-+CO2+2H2O=Al��OH��3��+HCO3-���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 2��3 | B�� | 1��2 | C�� | 1��3 | D�� | 3��2 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com