
下列实验中,可以加快反应速率的是( )
A.钠与水反应时,增加水的量
B.锌与稀硫酸反应时,加入少量CuSO4固体
C.用18mol/L的硫酸溶液代替2mol/L硫酸溶液常温下与铝反应
D.锌与稀硫酸反应时,加入少量醋酸钠固体
科目:高中化学 来源:2017届新疆兵团农二师华山中学高三上学前考试化学试卷(解析版) 题型:实验题
正丁醚常用作有机反应的溶剂。实验室制备正丁醚的反应和主要实验装置如下:2CH3CH2CH2CH2OH (CH3CH2CH2CH2)2O+H2O,反应物和产物的相关数据如下表:
(CH3CH2CH2CH2)2O+H2O,反应物和产物的相关数据如下表:
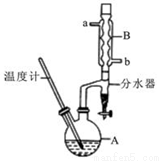

①将6 mL浓硫酸和37 g正丁醇,按一定顺序添加到A中,并加几粒沸石。
②加热A中反应液,迅速升温至135℃,维持反应一段时间。
③分离提纯:待A中液体冷却后将其缓慢倒入盛有70 mL水的温度分液漏斗中,振摇后静置,分液得粗产物。
④粗产物依次用40 mL水、20 mL NaOH溶液和40 mL水洗涤,分液后加入约3g无水氯化钙颗粒,静置一段时间后弃去氯化钙。
⑤将上述处理过的粗产物进行蒸馏,收集馏分,得纯净正丁醚11g。请回答:
(1)步骤①中浓硫酸和正丁醇的添加顺序为:应先加 。
(2)加热A前,需先从 (填“a”或“b”)口向B中通入水。
(3)步骤③的目的是初步洗去 ,振摇后静置,粗产物应 (填“上”或“下”)口倒出。
(4)步骤⑤中,加热蒸馏时应收集 (填选项字母)左右的馏分。
A.100℃ B.117℃ C.135℃ D.142℃
(5)反应过程中会观察到分水器中收集到液体物质,且分为上下两层,随着反应的进行,分水器中液体逐渐增多至充满时,上层液体会从左侧支管自动流回A。分水器中上层液体的主要成分为 ,下层液体的主要成分为 。
(6)本实验中,正丁醚的产率为 (精确到1%)。
查看答案和解析>>
科目:高中化学 来源:2017届湖南省高三上8月单元测化学试卷(解析版) 题型:选择题
下列反应中前者属于取代反应,后者属于加成反应的是
A.甲烷与氯气混合后光照反应;乙烯使酸性高锰酸钾溶液褪色
B.乙烯与溴的四氯化碳溶液反应;苯与氢气在一定条件下反应生成环己烷
C.苯与浓硝酸和浓硫酸的混合液加热反应;乙烯与水在一定条件下生成乙醇的反应
D.乙醇、乙酸和浓硫酸共热反应;乙醇在Cu的催化作用下和氧气反应
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河南省五岳八校高一下期末联考化学试卷(解析版) 题型:选择题
下列冶炼金属的原理不正确的是()
A.电解饱和食盐水制备金属钠 B.加热分解Ag2O制备金属银
C.Fe2O3与CO高温下反应制备金属铁 D.Cu2S与O2高温下反应制备金属铜
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河南省五岳八校高一下期末联考化学试卷(解析版) 题型:选择题
下列各组物质中,互为同分异构体的是( )
A.淀粉和纤维素 B.甲烷和乙烷 C.12C和14C D.蔗糖和麦芽糖
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河南省五岳八校高二下期末联考化学试卷(解析版) 题型:实验题
空气吹出法工艺,是目前“海水提溴”的最主要方法之一。其工艺流程如下:
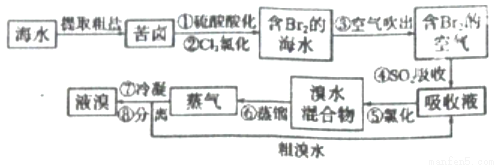
(1)步骤①中叫硫酸酸化可提高Cl2的利用率,理由是 。
(2)步骤④利用了SO2的还原性,反应的离子方程式为 。
(3)步骤⑥的蒸馏过程中,温度应控制在80〜90℃。温度过高或过低都不利于生产,请解释原因_______ 。
(4)步骤⑧中溴蒸气冷凝后得到液溴与溴水的混合物,可利用它们的相对密度相差很大的特点进行分离。分离仪器的名称是 。
(5)步骤①、②之后并未直接用“含Br2的海水”进行蒸馏得到液溴,而是经过“空气吹出”、“SO2吸收”、“氯化”后再蒸馏,这样操作的意义是 。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河南省五岳八校高二下期末联考化学试卷(解析版) 题型:选择题
萤火虫的发光是荧光素在催化作用下发生复杂的生化反应并释放光能,其原理可以简单表示如下:
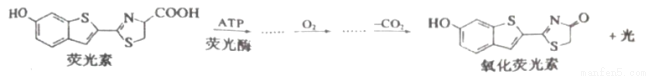
关于荧光素及氧化荧光素的叙述,正确的是 ( )
A.互为同系物 B.均可发生硝化反应
C.均可与碳酸氢钠反应 D.均最多有7个碳原子共平面
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省唐山市高一下期末化学试卷(解析版) 题型:选择题
一种基于酸性燃料电池原理设计的酒精检测仪,负极上的反应为:
CH3CH2OH– 4e—+ H2O = CH3COOH + 4H+。下列有关说法正确的是
A.电池反应的化学方程式为:CH3CH2OH + O2 = CH3COOH + H2O
B.检测时,电解质溶液中的 H+向负极移动
C.若有 0.4 mol 电子转移,则在标准状况下消耗 4.48 L 氧气
D.正极上发生的反应为:O2 + 4e—+ 2H2O = 4OH—
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省唐山市高二下期末化学试卷(解析版) 题型:选择题
以莽草酸为原料,经多步反应可制取对羟基苯甲酸。莽草酸、对羟基苯甲酸的结构简式如图。下列说法正确的是

A.莽草酸、对羟基苯甲酸都属于芳香族化合物
B.1mol莽草酸与NaOH溶液反应,最多消耗4 mol NaOH
C.利用FeCl3溶液可鉴别莽草酸和对羟基苯甲酸
D.对羟基苯甲酸较稳定,在空气中不易被氧化
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com