
| A. | 二者的分子个数之比为16:17 | |
| B. | 二者的原子个数之比为17:16 | |
| C. | 二者的氢原子个数之比为17:12 | |
| D. | 同温同压下两种气体的体积之比为16:17 |
分析 根据n=$\frac{m}{M}$可知,质量相等时CH4和NH3的物质的量与摩尔质量成反比,则CH4和NH3的物质的量之比=17g/mol:16g/mol=17:16,然后根据N=nNA、V=nVm分析解答.
解答 解:根据n=$\frac{m}{M}$可知,质量相等时CH4和NH3的物质的量与摩尔质量成反比,则CH4和NH3的物质的量之比=17g/mol:16g/mol=17:16,
A.根据N=nNA可知,分子数之比等于分子的物质的量之比,则CH4和NH3的分子数之比=17:16,故A错误;
B.根据N=nNA可知,CH4和NH3含有原子个数之比等于原子的物质的量之比=(17×5):(16×4)=85:64,故B错误;
C.根据N=nNA可知,CH4和NH3含有H原子个数之比等于H原子的物质的量之比=(17×4):(16×3)=17:12,故C正确;
D.同温同压下气体摩尔体积相同,根据n=nVm可知同温同压下等质量的CH4和NH3体积之比=物质的量之比=17:16,故D错误;
故选C.
点评 本题考查了物质的量的计算,题目难度不大,明确物质的量与其它物理量之间的关系即可解答,试题侧重基础知识的考查,有利于提高学生的分析能力及化学计算能力.


 开心练习课课练与单元检测系列答案
开心练习课课练与单元检测系列答案 开心试卷期末冲刺100分系列答案
开心试卷期末冲刺100分系列答案 双基同步导航训练系列答案
双基同步导航训练系列答案科目:高中化学 来源: 题型:选择题
| A. | ①②④ | B. | ②③④ | C. | ② | D. | ②⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
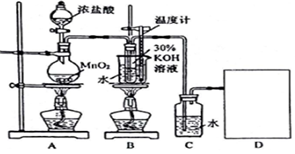
| 实验 编号 | 试剂及其用量 | |||
| 0.2mol•L-1kJ/mL | KClO3(s)/g | 6.0mol•L-1H2SO4/mL | H2O/mL | |
| 1 | 1.0 | 0.1 | 0 | a |
| 2 | 1.0 | 0.1 | 3.0 | b |
| 3 | 1.0 | 0.1 | 6.0 | c |
| 4 | 1.0 | 0.1 | 9.0 | 0 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
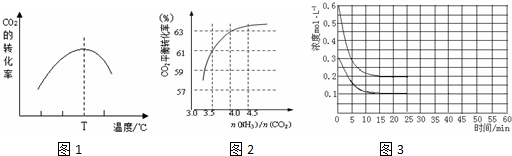
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
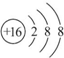 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加活性炭吸附水中小顆粒物,净化水质的方法属于物理方法 | |
| B. | 医用消毒洒精中乙醇的浓度为95% | |
| C. | 漂白粉长期放置会被空气中的氧气氧化而变质 | |
| D. | 黑火药是我国古代四大发明之一,配方为“一硫二硝三木炭”,“硝“是指硝酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
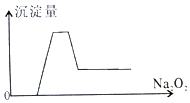 有一透明溶液,取出少量滴入BaCl2溶液,有白色沉淀生成;另取一定体积的该溶液加入过量Na2O2,有无色有刺激性味气体产生,同时有白色沉淀生成,其沉淀量(纵坐标)与加入Na2O2的量(横坐标)的关系如图所示,根据以上判断在该溶液中一定存在的离子是( )
有一透明溶液,取出少量滴入BaCl2溶液,有白色沉淀生成;另取一定体积的该溶液加入过量Na2O2,有无色有刺激性味气体产生,同时有白色沉淀生成,其沉淀量(纵坐标)与加入Na2O2的量(横坐标)的关系如图所示,根据以上判断在该溶液中一定存在的离子是( )| A. | ①②③④⑦ | B. | ①③④⑦ | C. | ①②③⑤⑦ | D. | ①③④⑧ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该工艺中MgO可循环利用 | |
| B. | 理论上 1mol NH4Cl制得Cl2的体积一定为11.2L | |
| C. | 在800~1000℃条件下,O2的还原性强于Cl2的还原性 | |
| D. | 若反应2NH3+MgCl2+H2O═2NH4Cl+MgO能自发进行,则该反应△H>0 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2S溶液中只存在2个电离平衡 | |
| B. | c(OH-)=$\sqrt{{K}_{w}}$的溶液一定呈中性 | |
| C. | 加热碳酸钠溶液可证明其水解是吸热反应 | |
| D. | 常温下,在AlPO4和FePO4的饱和溶液中滴加少量Na3PO4溶液,Ksp(AlPO4)和Ksp(FePO4)将减小 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com