
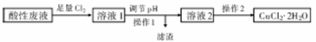
铜及其化合物在日常生活中应用广泛。某研究性学习小组欲从氯化铁溶液腐蚀印刷电路极后的酸性废液中(含FeCl3、FeCl2含CuCl2)制备氯化铜晶体(CuCl2·2H2O),设计路线如下:
回答下列问题:
(1)检验酸性废液中含有Fe3+,常用的试剂是 (填化学式);酸性废液中加入足量Cl2,反应的化学方程式为 。
(2)操作1的名称是 ;调节溶液的pH时适宜选用下列试剂中的 ;
A.NaOH溶液 B.Na2CO3 C.氨水 D.CuO
若调节溶液的pH为4时,溶液中残留的Fe3+物质的量浓度为 (已知25℃时,Kap[Fe(OH)3]=4×10-38).
(3)操作2需在氯化氢气流中经过加热浓缩、 、过滤、洗涤、干燥。在氯化氢气流中进行操作的原因是 (结合离子方程式并简要说明)。
(4)若在溶液2中通入一定量的SO2,加热,则生成CuCl沉淀,该反应的离子方程式为 。
(5)该小组设想以铜棒和石墨棒为电极,以KI溶液为电解液,利用电解来制取碘化亚铜,
已知:2Cu2++4I-=2CuI↓+I2.若按其设想,铜棒应连接电源的 (填“正”或“负”)极;阴极发生的电极反应式为 。
科目:高中化学 来源:2016-2017学年河北省高二上开学测化学试卷(解析版) 题型:选择题
类推思维是化学解题中常用的一种思维方法,下列有关离子方程式的类推正确的是)
已知 | 类推 | |
A | 将Fe加入CuSO4溶液中 Fe+Cu2+=Cu+Fe2+ | 将Na加入到CuSO4溶液中 2Na+Cu2+=Cu+2Na+ |
B | 向稀硫酸加入NaOH溶液至中性 H++OH-=H2O | 向H2SO4溶液加入Ba(OH)2溶液至中性 H++OH-=H2O |
C | 向氯化铝溶液中加入足量NaOH溶液 Al3++4OH-=AlO2-+2H2O | 向氯化铝溶液中加入足量氨水 Al3++4NH3•H2O=AlO2-+2H2O+4NH4+ |
D | 向Ca(OH)2溶液中通入过量CO2 CO2+OH-=HCO3- | 向Ca(OH)2溶液中通入过量SO2 SO2+OH-=HSO3- |
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖南省高二上开学测化学试卷(解析版) 题型:选择题
某气态烷烃与烯烃的混合气9g,其密度为相同状况下氢气密度的11.2 倍,将混合气体通过足量的溴水,溴水增重4.2g ,则原混合气体的组成为( )
A.乙烷与丙烯 B.甲烷与乙烯 C.甲烷与丙烯 D.甲烷与丁烯
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖南省高二上第二次月考化学试卷(解析版) 题型:选择题
下列说法正确的是
A.对于相同浓度的弱酸HX和HY(前者的Ka较小)溶液,加水稀释相同倍数时,HY溶液的pH改变值小于HX溶液的pH改变值
B.在NH3·H2O和NH4Cl浓度均为0.1 mol·L-1的体系中,外加少量酸或碱时,溶液的pH可保持基本不变
C.在NaH2PO4水溶液中存在关系:c(H3PO4)+c(H+)=c(HPO42-)+c(PO43-)+c(OH-)
D.沉淀溶解平衡AgI Ag++I-的平衡常数为8.5×10-17,说明难溶盐AgI是弱电解质
Ag++I-的平衡常数为8.5×10-17,说明难溶盐AgI是弱电解质
查看答案和解析>>
科目:高中化学 来源:2017届云南省高三第一次摸底化学试卷(解析版) 题型:推断题
[化学—选修5:有机化学基础]
甲基丁炔醇(简写为MB),用作医药和香料中间体,酸蚀抑制剂、镀镍或镀铜的上光剂等。MB的一种人工合成路线设计如下:
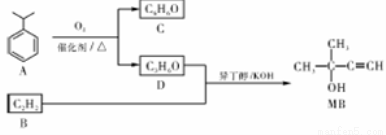
已知:①C的溶液中滴加FeCl3溶液后显紫色
②D的核磁共振氢谱显示只有一种化学环境的氢
③R2COR2+HC=CR3 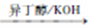
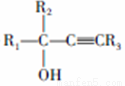
回答下列问题:
(1)A氧化时,理论上生成C和D的物质的量之比为 。
(2)B、C的结构简式分别为 、 ,D的官能团名称为 。
(3)B+D→MB的反应类型为 ;用系统命名法,MB的化学名称为 。
(4)B+D→MB的反应时间不宜超过两个小时,否则MB与D发生二次反应使产率降低,MB与D反应的化学方程式为 。
(5)某有机物E和A的芳香烃异构体,E的可能结构共有 种(不考虑立体异构),写出其中只有两种不同化学环境的氢,数目比为3:1的异构体的结构简式 。
(6)已知:端炔化合物在一定条件下可发生偶联反应,如:
2R-C≡CH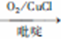 R-C≡C-C≡C-R
R-C≡C-C≡C-R
写出由2-丙醇和乙炔为初始原料(其他有机溶剂、无机试剂任选)合成2,7-二甲基-3,5-辛二炔-2,7-二醇(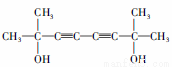 ,医药中间体,材料中间体)的合成路线。
,医药中间体,材料中间体)的合成路线。
合成路线流程图示例如下:
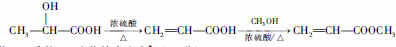
查看答案和解析>>
科目:高中化学 来源:2017届江苏省高三上学期摸底考试化学试卷(解析版) 题型:推断题
有机物H是一种新型大环芳酰胺的合成原料,可通过以下方法合成:
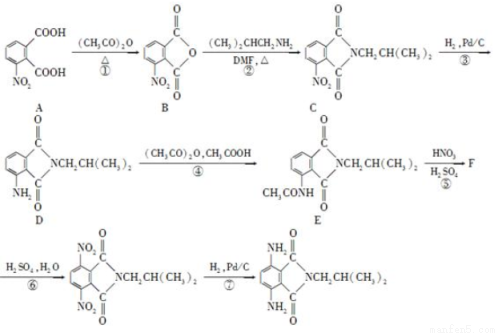
已知:①苯胺(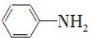 )有还原性,易被氧化;
)有还原性,易被氧化;
②硝基苯直接硝化主要产物为二硝基苯。
(1)写出A中含氧官能团的名称: 。
(2)④的反应类型为 ;F的结构简式为 。
(3)流程中设计步骤④和⑥的目的是 。
(4)写出一种符合下列条件的化合物C的同分异构体的结构简式 。
①分子中含有2个苯环;②能与FeCl3溶液发生显色反应;③分子中有3种不同化学环境的氢子。
(5)对苯二胺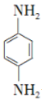 是一种重要的染料中间体。根据已有知识并结合相关信息,写出以苯、(CH3CO)2O及CH3COOH为主要有机原料制备对苯二胺的合成路线流程图(无机试剂任用)。合成路线流程图示例如下:
是一种重要的染料中间体。根据已有知识并结合相关信息,写出以苯、(CH3CO)2O及CH3COOH为主要有机原料制备对苯二胺的合成路线流程图(无机试剂任用)。合成路线流程图示例如下: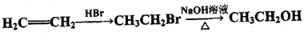
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省高二上学期摸底化学试卷(解析版) 题型:推断题
A、B、C、D、E五种短周期元素,A、B同主族,C、D同周期,B、E同周期。气体A2与气体C2混合后点燃能够发生爆炸,且产物在常温常压下是一种无色无味的液体。B、C、E简单离子的核外电子排布相同。E的最高价氧化物可与B的最高价氧化物的水化物反应生成一种易溶于水的的盐,D能形成自然界硬度最大的单质。请根据上述所提供的信息回答下列问题。
(1)写出A、B两种元素的元素名称:A________、B________写出D的最高价氧化物的电子式 。
(2)写出由B和C两元素形成的原子个数比为1:1的化合物F的电子式 ,其存在的化学键是
(3)写出F和A2C反应的离子方程式:____________________。
(4)用电子式表示B2C形成的过程:______________________。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年广东省汕头市高二上学期入学考试化学试卷(解析版) 题型:选择题
元素X的原子核内只有1个质子.元素Y的阳离子电子层结构和氖原子电子层结构相同,Y、Z和E在周期表里位于同一周期.X和E、Z分别能形成气态氢化物XE和X2Z,它们的水溶液是酸.Z跟Y能形成离子化合物Y2Z.与氖同周期的元素F的气态氢化物FX3,其水溶液能使酚酞试液变红.则X、Y、Z、E、F的元素符号是
A. H、Na、S、Cl、N B. H、Na、S、Br、P
C. H、Li、O、F、N D. H、Mg、S、O、N
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com