
| A�� | ��������������ʴʱ������ʴ�����ʺ�����Ũ���� | |
| B�� | ��״���£�2.24LCCl4�����й��ۼ�����ĿΪ0.4��6.02��1023 | |
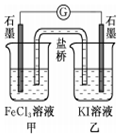
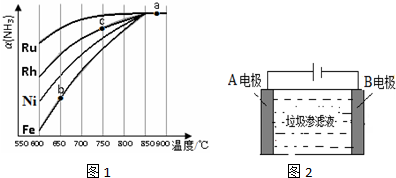
| C�� | �����ʺϵ�����������Ӧ2Fe3++2I-�T2Fe2++I2��Ƴ���ͼ��ʾ��ԭ��أ�������֭����Ϊ����ڼ�������FeCl2���壬������ʯī�缫Ϊ���� | |
| D�� | ��ʢ��2mL����H2S��Һ����֧�Թ��зֱ�μ�1��Ũ�Ⱦ�Ϊ0.1mol/L��ZnSO4��Һ��CuSO4��Һ����CuS���ɶ���ZnS���ɣ���Ksp��CuS����Ksp��ZnS�� |
���� A����������������ʴʱ������Ũ��Խ��ʴ������Խ�죻
B����״�������Ȼ�̼�������壻
C������2Fe3++2I-�T2Fe2++I2��֪����Ԫ�صĻ��ϼ۽��ͣ���Ԫ�صĻ��ϼ����߷�����
D�������ܶȻ�ԽСԽ���׳���������
��� �⣺A����������������ʴʱ������Ũ��Խ��ʴ������Խ�죬��ʴ�����ʺ�����Ũ���йأ���A����
B����״���£����Ȼ�̼�������壬2.24LCCl4���ʵ�������0.1mol����B����
C������2Fe3++2I-�T2Fe2++I2��֪����Ԫ�صĻ��ϼ۽��ͣ�����Ԫ�صĻ��ϼ����ߣ���ͼ�м��ձ�������FeCl3���壬��ʯī���������������ձ��е�ʯī����������C����
D����CuS���ɶ���ZnS���ɣ���˵��CuS���ܽ�Ƚ�С������Ksp��CuS����Ksp��ZnS������D��ȷ��
��ѡD��
���� ���⿼���Ϊ�ۺϣ��漰������ʴ��ԭ��ص�����Լ��ܶȻ��Ĵ�С�Ƚϵ�֪ʶ����Ŀ�ѶȲ���������ѧ�������Ӧ��������



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | H2SO4 | B�� | NaOH | C�� | Na2SO4 | D�� | CuCl2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | MgCO3���Գ�ȥMgCl2������Һ�е�Fe3+ | |
| B�� | ʵ����NaHSO3��Һ��pH��7��˵����H2SO3��ǿ�� | |
| C�� | ͨ����ѧ�仯���ԡ���ʯ�ɽ𡱣����ɽ����ת���ɽ��� | |
| D�� | 2.24LNO��1.12O2��ַ�Ӧ����������ԭ����Ŀһ��Ϊ0.3��6.02��1023 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ʯ�Ҿ�����ˮ�ԣ������ڸ������� | |
| B�� | ��ȩ��ʹ�����ʱ��ԣ���������ʳƷ������ | |
| C�� | ̿����ǿ��ԭ�ԣ�������ұ���ơ��صȽ��� | |
| D�� | ̼��������Һ���������ԣ���������θ���кͼ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| ѡ�� | ʵ����������� | ���� |
| A | ��Fe��NO3��2����ϡH2SO4�μ�KSCN��Һ�� ��Һ��ɺ�ɫ | Fe��NO3��2��һ����Fe3+ |
| B | ��ú����ȡ��һС���ƣ�����ֽ���������ú�ͣ� ������ˮ�Ҵ��У��������� | Na���û����������е��� |
| C | ��ij����ͨ��Ʒ����Һ����Һ��ɫ | ����һ����SO2 |
| D | ��NaAlO2��Һ�е���NaHCO3��Һ��������ɫ���� | AlO2-���H+��������CO32-ǿ |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
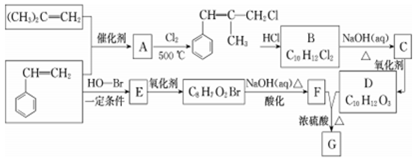
 ��G�Ľṹ��ʽΪ
��G�Ľṹ��ʽΪ ��
��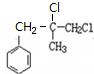 +2NaOH$��_{��}^{H_{2}O}$
+2NaOH$��_{��}^{H_{2}O}$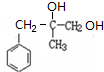 +2NaCl��
+2NaCl��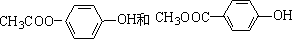 ��
��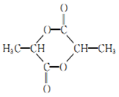 �ĺϳ�·�ߣ�
�ĺϳ�·�ߣ�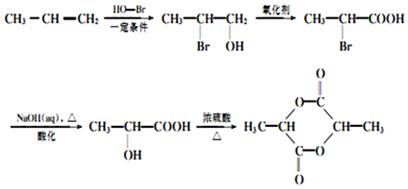 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
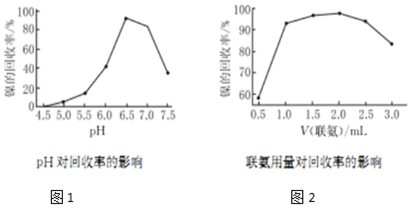
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����ǻ�ѧ�仯����С������ | |
| B�� | һ��ԭ�ӵ�ԭ�Ӻ˶��������ӡ����ӹ��ɵ� | |
| C�� | ���ӵ������ܱ�ԭ�������� | |
| D�� | ���ӡ�ԭ�ӡ����Ӷ���ֱ�ӹ������� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com